
Plutonium
Renseignements g??n??raux
Enfants SOS offrent un chargement complet de la s??lection pour les ??coles pour une utilisation sur les intranets des ??coles. Avec enfants SOS vous pouvez choisir de parrainer des enfants dans plus de cent pays
| Plutonium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
94 Pu | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apparence | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
blanc argent??, ternir au gris fonc?? dans l'air  | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propri??t??s g??n??rales | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nom, symbole, nombre | plutonium, Pu, 94 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Prononciation | / p l U t oʊ n Je ə m / ploo- HO -neE-əm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ??l??ment Cat??gorie | actinides | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Groupe, p??riode, bloc | n / a, 7, fa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poids atomique standard | (244) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuration ??lectronique | [ Rn ] 5f 6 7s 2 2, 8, 18, 32, 24, 8, 2  | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Histoire | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| D??couverte | Glenn T. Seaborg, Arthur Wahl, Joseph W. Kennedy, Edwin McMillan (1940-1) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propri??t??s physiques | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phase | solide | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densit?? (?? proximit?? rt) | 19,816 g ?? cm -3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Liquid densit?? au mp | 16,63 g ?? cm -3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point de fusion | 912,5 K , 639,4 ?? C, 1182,9 ?? F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point d'??bullition | 3505 K, 3228 ?? C, 5842 ?? F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| La chaleur de fusion | 2,82 kJ ?? mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chaleur de vaporisation | 333,5 kJ ?? mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacit?? thermique molaire | 35,5 J ?? mol -1 ?? K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| La pression de vapeur | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propri??t??s atomiques | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ??tats d'oxydation | 8, 7, 6, 5, 4, 3, 2, 1 ( l'oxyde amphot??re) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ??lectron??gativit?? | 1,28 (??chelle de Pauling) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ??nergies d'ionisation | 1e: 584,7 kJ ?? mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon atomique | 159 h | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon covalente | 187 ?? 13 heures | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscellan??es | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Crystal structure | monoclinique  | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ordre magn??tique | paramagn??tique | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| R??sistivit?? ??lectrique | (0 ?? C) 1,460 μΩ ?? m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivit?? thermique | 6,74 W ?? m -1 ?? K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dilatation thermique | (25 ?? C) 46,7 um ?? m -1 ?? K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vitesse du son | 2260 m ?? s -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Le module d'Young | 96 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Module de cisaillement | 43 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Coefficient de Poisson | 0,21 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Num??ro de registre CAS | 7440-07-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| La plupart des isotopes stables | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Article d??taill??: Isotopes du plutonium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Le plutonium est un transuraniens radioactive ??l??ment chimique avec le symbole Pu et de num??ro atomique 94. Ce est un actinide m??tallique d'aspect gris argent?? que ternit lorsqu'il est expos?? ?? l'air, et la formation d'un rev??tement mat lorsque oxyd??e. L'??l??ment pr??sente normalement six allotropes et quatre ??tats d'oxydation . Il r??agit avec le carbone , les halog??nes , l'azote et le silicium . Lorsqu'ils sont expos??s ?? l'air humide, il forme oxydes et hydrures qui ??largissent l'??chantillon jusqu'?? 70% en volume, qui ?? son tour se ??cailler sous forme de poudre qui peut se enflammer spontan??ment. C'est radioactifs et peuvent se accumuler dans le os. Ces propri??t??s rendent la manipulation de plutonium dangereux.
Le plutonium est le plus lourd ??l??ment primordial du fait de sa plus stable isotopes, plutonium-244, dont la demi-vie d'environ 80 millions d'ann??es, ce est juste assez longtemps pour que l'??l??ment que l'on trouve en quantit??s infimes dans la nature. Le plutonium est surtout un sous-produit de r??actions nucl??aires dans les r??acteurs o?? certains des neutrons lib??r??s par la fission processus conversion de l'uranium-238 noyaux en plutonium.
Les deux plutonium-239 et plutonium 241 sont fissiles, ce qui signifie qu'ils peuvent maintenir un r??action nucl??aire en cha??ne, conduisant ?? des applications dans des armes nucl??aires et les r??acteurs nucl??aires. Plutonium-240 pr??sente un taux ??lev?? de fission spontan??e, soulevant la flux de neutrons de tout ??chantillon contenant. La pr??sence de plutonium-240 limite la facilit?? d'utilisation d'un ??chantillon d'armes ou de combustible du r??acteur, et d??termine son grade.
Plutonium-238 a une demi-vie de 88 ans et ??met des particules alpha. Il se agit d'une source de chaleur en g??n??rateurs thermo??lectriques radio-isotopes, qui sont utilis??s pour alimenter certains engin spatial. isotopes de plutonium sont co??teux et peu pratique ?? s??parer, afin isotopes particuliers sont g??n??ralement fabriqu??s dans les r??acteurs sp??cialis??s.
Une ??quipe dirig??e par Glenn T. Seaborg et Edwin McMillan au Universit?? de Californie, Berkeley laboratoire abord synth??tis?? plutonium en 1940 en bombardant l'uranium-238 avec deut??rons. Des traces de plutonium ont ??t?? d??couverts ult??rieurement dans la nature. Produire du plutonium en quantit??s utiles pour la premi??re fois, ce ??tait une partie importante de la Projet Manhattan pendant la Seconde Guerre mondiale , qui a d??velopp?? les premi??res bombes atomiques. La premi??re essai nucl??aire, " Trinity "(Juillet 1945), et la deuxi??me bombe atomique utilis??e pour d??truire une ville ( Nagasaki, au Japon, en Ao??t 1945), " Fat Man ", avaient tous deux noyaux de plutonium-239. Exp??riences d'irradiation humaines ??tudient plutonium ont ??t?? men??es sans consentement ??clair??, et plusieurs accidents de criticit??, dont certains mortels, se sont produits pendant et apr??s la guerre. ??limination des d??chets de plutonium les centrales nucl??aires et d??mant??lement des armes nucl??aires construits pendant la guerre froide est un nucl??aire-prolif??ration et le souci de l'environnement. D'autres sources de plutonium dans l'environnement sont retomb??es de nombreux essais nucl??aires hors-terre (maintenant interdit).
Caract??ristiques
Propri??t??s physiques
Plutonium, comme la plupart des m??taux, a un aspect argent?? brillant au d??but, un peu comme le nickel , mais il oxyde tr??s rapidement ?? un gris terne, bien jaune et vert olive sont ??galement signal??s. ?? la salle du plutonium de temp??rature est dans sa forme α (alpha). Ce, la forme structurelle la plus courante de l'??l??ment ( allotrope ), est ?? peu pr??s aussi dur et cassant comme fonte grise sauf se il est alli?? avec d'autres m??taux pour la rendre douce et ductile. Contrairement ?? la plupart des m??taux, il ne est pas un bon conducteur de chaleur ou ??lectricit??. Il a un faible point de fusion (640 ?? C) et un inhabituellement ??lev?? d'??bullition (3228 ?? C).
D??sint??gration alpha, la lib??ration d'un de haute ??nergie h??lium noyau, est la forme la plus commune de la d??sint??gration radioactive du plutonium. Une masse de 5 kg de Pu 239 contient environ 12,5 ?? 10 24 atomes. Avec une demi-vie de 24100 ann??es, environ 11,5 ?? 10 12 atomes de ses d??composer chaque seconde en ??mettant un 5,157 MeV particule alpha. Cela ??quivaut ?? 9,68 watts de puissance. La chaleur produite par la d??c??l??ration des particules alpha, il est chaude au toucher.
La r??sistivit?? est une mesure de la force avec un mat??riau se oppose ?? l'??coulement de courant ??lectrique. La r??sistivit?? du plutonium ?? la temp??rature ambiante est tr??s ??lev?? pour un m??tal, et ce est encore plus ??lev?? avec des temp??ratures plus basses, ce qui est inhabituel pour les m??taux. Cette tendance se poursuit jusqu'?? 100 K , en dessous de laquelle la r??sistivit?? diminue rapidement pour les ??chantillons frais. R??sistivit?? commence alors ?? augmenter avec le temps ?? environ 20 K en raison de d??g??ts d'irradiation, le taux dict?? par la composition isotopique de l'??chantillon.
En raison de l'auto-irradiation, un ??chantillon de treillis de plutonium dans toute sa structure cristalline, ce qui signifie l'agencement ordonn?? de ses atomes est perturb?? par le rayonnement dans le temps. Auto-irradiation peut aussi conduire ?? recuit qui se oppose ?? certains de la fatigue des effets que l'augmentation de temp??rature sup??rieure ?? 100 K.
Contrairement ?? la plupart des mat??riaux, plutonium augmentation de la densit?? quand elle fond, de 2,5%, mais le m??tal liquide pr??sente une diminution lin??aire de la densit?? avec la temp??rature. Pr??s du point de fusion, le plutonium liquide a ??galement tr??s ??lev?? la viscosit?? et la tension superficielle par rapport aux autres m??taux.
Allotropes

Le plutonium a normalement six allotropes et forme septi??me (zeta, ζ) ?? haute temp??rature dans une plage de pression limit??e. Ces allotropes, qui sont diff??rentes modifications structurelles ou des formes d'un ??l??ment, ont tr??s similaire ??nergies internes mais en faisant varier de mani??re significative la densit?? et structures cristallines. Cela rend plutonium tr??s sensibles aux changements de temp??rature, de pression, ou de la chimie, et permet des changements de volume suivantes dramatiques transitions de phase d'une forme allotropique ?? l'autre. Les densit??s des diff??rentes formes allotropiques varient de 16,00 g / cm 3 ?? 19,86 g / cm 3.
La pr??sence de ces nombreux allotropes fait usinage plutonium tr??s difficile, car il change d'??tat tr??s facilement. Par exemple, la forme de α existe ?? temp??rature ambiante dans le plutonium non alli??. Il a des caract??ristiques d'usinage similaires ?? fonte mais les changements ?? la mati??re plastique et la forme de β mall??able (b??ta) ?? des temp??ratures l??g??rement plus ??lev??es. Les raisons pour lesquelles le diagramme de phase complexe ne sont pas enti??rement comprises. Le formulaire de α a une faible sym??trie structure monoclinique, d'o?? sa fragilit??, de traction et faible conductivit?? thermique.
Plutonium sous forme de δ existe normalement dans l'intervalle 310 ?? C ?? 452 ?? C, mais est stable ?? la temp??rature ambiante lorsqu'il est alli?? avec un faible pourcentage de gallium , aluminium , ou de c??rium , l'am??lioration de l'ouvrabilit?? et lui permettant d'??tre soud?? . La forme de delta a caract??re plus typique m??tallique, et est ?? peu pr??s aussi fort et mall??able que l'aluminium. Dans armes de fission, l'explosif des ondes de choc servant ?? comprimer un noyau de plutonium sont ??galement provoquer une transition de phase de l'habituel delta plutonium ?? la forme alpha plus dense, en aidant ?? r??aliser de mani??re significative supercritique. La phase de ε, la temp??rature la plus ??lev??e allotrope solide, pr??sente anormalement ??lev??e atomique autodiffusion rapport ?? d'autres ??l??ments.
Fission nucl??aire

Le plutonium est un marqueur radioactif actinides m??tal dont isotopes , plutonium-239, est l'un des trois primaires isotopes fissiles ( l'uranium-233 et uranium-235 sont les deux autres); plutonium 241 est aussi tr??s fissile. Pour ??tre consid??r?? comme fissiles, un isotope de noyau atomique doit ??tre en mesure de briser ou de la fission lorsqu'il a ??t?? frapp?? par un ralentir les neutrons d??placement et de lib??rer suffisamment de neutrons suppl??mentaires pour soutenir la r??action nucl??aire en cha??ne en divisant autres noyaux.
Pur plutonium-239 peut avoir une facteur de multiplication (K eff) sup??rieur ?? un, ce qui signifie que si le m??tal est pr??sent en quantit?? suffisante et avec une g??om??trie appropri??e (par exemple, une sph??re de taille suffisante), il peut former un masse critique. Au cours de la fission, une fraction de la ??nergie, qui contient un noyau ensemble de liaison, est lib??r??e en grande quantit?? d'??nergie ??lectromagn??tique et cin??tique (une grande partie de celle-ci ??tant rapidement convertie en ??nergie thermique). Fission d'un kg de plutonium-239 peut produire une explosion ??quivalente ?? 21 000 tonnes de TNT. Ce est cette ??nergie qui fait du plutonium-239 utile dans des armes nucl??aires et r??acteurs.
La pr??sence de l'isotope plutonium 240 dans un ??chantillon limite son potentiel de bombe nucl??aire, le plutonium-240 est relativement ??lev??e taux de fission spontan??e (~ 440 fissions par seconde par gramme-plus de 1000 neutrons par seconde par gramme), l'augmentation des niveaux de fond de neutrons et en augmentant ainsi le risque de pr??d??tonation. Le plutonium est identifi?? comme ??tant soit armes de qualit??, qualit?? de carburant, ou de qualit?? r??acteur de puissance en fonction du pourcentage de plutonium-240 qu'il contient. Plutonium de qualit?? militaire contient moins de 7% de plutonium-240. plutonium de qualit?? de carburant contient de 7% ?? moins de 19%, et le grade de r??acteur de puissance contient 19% ou plus de plutonium-240. Supergrade plutonium, avec moins de 4% de plutonium-240, est utilis?? dans US Navy armes stock??es ?? proximit?? d'exp??dier et les ??quipages de sous-marins, en raison de sa radioactivit?? inf??rieure. L'isotope plutonium 238 ne est pas fissiles, mais peut subir la fission nucl??aire facilement avec neutrons rapides ainsi que d??sint??gration alpha.
Isotopes et la synth??se

Vingt isotopes radioactifs du plutonium ont ??t?? caract??ris??s. La plus longue dur??e sont le plutonium-244, avec une demi-vie de 80,8 millions ann??es, le plutonium-242, avec une demi-vie de 373300 ann??es, et le plutonium-239, avec une demi-vie de 24110 ann??es. Tous les isotopes radioactifs restants ont des demi-vies qui sont moins de 7000 ans. Cet ??l??ment a ??galement huit ??tats m??tastables, bien qu'aucun sont stables et tous ont des demi-vies moins d'une seconde.
Les isotopes de gamme de plutonium nombre de masse de 228 ?? 247. Le primaire modes de d??sint??gration des isotopes avec des num??ros de masse inf??rieure ?? isotope le plus stable, le plutonium-244, le sont fission spontan??e et ??mission α, formant principalement de l'uranium (92 protons ) et neptunium (93 protons) isotopes produits de d??sint??gration (en n??gligeant la vaste gamme de noyaux filles cr????s par des processus de fission). Le mode de d??sint??gration des isotopes primaires avec des nombres de masse plus ??lev??s que le plutonium-244 est ??missions β, principalement formant am??ricium (95 protons) isotopes produits de d??sint??gration. Le plutonium-241 est le isotope parent de la s??rie de d??sint??gration de neptunium, am??ricium d??composition-241 via β ou ??mission d'??lectrons.
Le plutonium-238 et 239 sont les isotopes les plus largement synth??tis??es. Le plutonium-239 est synth??tis?? par la r??action suivante utilisant de l'uranium (U) et de neutrons (n) par d??sint??gration b??ta (β -) avec neptunium (Np) comme interm??diaire:
Les neutrons de la fission de l'uranium-235 sont captur?? par l'uranium-238 noyaux pour former l'uranium-239; une d??sint??gration b??ta convertit un neutron en proton pour former Np-239 (demi-vie 2,36 jours) et une autre d??sint??gration b??ta forme plutonium-239. Les travailleurs sur le Tube Alloys projet avait pr??dit cette r??action th??oriquement en 1940.
Le plutonium-238 est synth??tis?? en bombardant l'uranium-238 avec deutons (D, les noyaux de fortes hydrog??ne ) dans la r??action suivante:
Dans ce processus, un deut??ron frapper uranium 238 produit deux neutrons et neptunium 238, qui se d??sint??gre spontan??ment en ??mettant des particules b??ta n??gatives pour former le plutonium-238.
Propri??t??s thermiques et de fission Decay
isotopes de plutonium subissent une d??sint??gration radioactive, qui produit La chaleur de d??sint??gration. Diff??rents isotopes produisent diff??rentes quantit??s de chaleur par unit?? de masse. La chaleur de d??sint??gration est g??n??ralement r??pertori?? comme watt / kg, ou milliwatts / g. En cas de gros morceaux de plutonium (par exemple, une fosse d'arme) et le retrait de chaleur insuffisante l'auto-??chauffement qui en r??sulte peut ??tre importante. Tous les isotopes produisent un son faible gamma sur la pourriture.
| Isotope | mode Decay | Demi-vie (ann??es) | la puissance r??siduelle (W / kg) | Neutrons de fission spontan??e (1 / (g ?? s)) | Commentaire |
|---|---|---|---|---|---|
| 238 Pu | alpha 234 U | 87,74 | 560 | 2600 | Tr??s forte chaleur de d??sint??gration. M??me en petites quantit??s peut causer l'auto-??chauffement important. Utilis?? seul dans g??n??rateurs thermo??lectriques radio-isotopes. |
| 239 Pu | alpha 235 U | 24100 | 1,9 | 0,022 | L'isotope fissile principale en usage. |
| 240 Pu | alpha 236 U, fission spontan??e | 6560 | 6,8 | 910 | L'impuret?? principale dans des ??chantillons de l'isotope 239 Pu. La note de plutonium est g??n??ralement r??pertori?? comme pourcentage de 240 Pu. Hautes entrave de fission spontan??s utilisent des armes nucl??aires. |
| 241 Pu | b??ta-moins, ?? 241 Am | 14,4 | 4.2 | 0,049 | Se d??sint??gre en am??ricium 241; son accumulation pr??sente un risque d'irradiation dans les ??chantillons plus ??g??s. |
| 242 Pu | alpha 238 U | 376000 | 0,1 | 1700 |
Am??ricium 241, le produit de d??sint??gration du plutonium-241, a une demi-vie de 430 ann??es, 1,2 fissions spontan??es par gramme par seconde, et la d??composition thermique de 114 watts par kilogramme. Comme sa d??sint??gration produit des rayons gamma de haute p??n??tration, sa pr??sence dans le plutonium, d??termin?? par la concentration initiale de plutonium-241 et l'??ge de l'??chantillon, augmente l'exposition aux rayonnements des structures et du personnel environnantes.
Les compos??s et la chimie

A temp??rature ambiante, le plutonium pur est de couleur argent??e, mais gagne un ternir lorsqu'il est oxyd??. L'??l??ment affiche quatre ioniques communes ??tats d'oxydation dans solution aqueuse et une rare:
- Pu (III), que Pu 3+ (bleu lavande)
- Pu (IV), que Pu 4+ (brun jaune)
- Pu (V), comme PuO +
2 (rose p??le) - Pu (VI), comme PuO 2 +
2 (orange rose) - Pu (VII), comme PuO 3-
5 (vert) -le ion heptavalent est rare
La couleur repr??sent??e par des solutions de plutonium d??pend ?? la fois l'??tat d'oxydation et de la nature de l'acide anion . Ce est l'anion d'acide qui influe sur le degr?? de atomes complexant-faire se connectent ?? un atome central, de l'esp??ce de plutonium.
Plutonium m??tallique est produit par r??action t??trafluorure de plutonium avec du baryum , calcium ou lithium ?? 1200 ?? C. Il est attaqu?? par les acides , l'oxyg??ne et la vapeur mais pas par alcalis et se dissout facilement dans concentr?? chlorhydrique , iodhydrique et les acides perchlorique. Le m??tal en fusion doit ??tre conserv?? dans un ou un vide atmosph??re inerte pour ??viter une r??action avec l'air. ?? 135 ?? C le m??tal se enflamme ?? l'air et va exploser se il est plac?? dans le t??trachlorure de carbone .

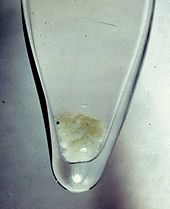
Le plutonium est un m??tal r??actif. Dans l'air humide ou humide argon , le m??tal se oxyde rapidement, produisant un m??lange de oxydes et hydrures. Si le m??tal est expos?? suffisamment longue pour une quantit?? limit??e de vapeur d'eau, un rev??tement de surface en poudre de PuO 2 est form??. Aussi est form?? plutonium, mais un exc??s de l'hydrure de formes de vapeur d'eau seulement PuO 2.
Gr??ce ?? ce rev??tement, le m??tal est le pyrophore, ce qui signifie qu'il peut se enflammer spontan??ment, afin de plutonium m??tal est g??n??ralement trait??e dans une atmosph??re inerte et sec de l'azote ou de l'argon. L'oxyg??ne retarde les effets de l'humidit?? et agit en tant que agent de passivation.
Plutonium montre ??normes, et r??versibles, les taux de r??action avec l'hydrog??ne pur, formant plutonium hydrure. Il r??agit ??galement facilement avec l'oxyg??ne, en formant PuO et PuO 2, ainsi que les oxydes interm??diaires; oxyde de plutonium remplit 40% plus de volume que le plutonium m??tal. Plutonium donne naissance ?? des compos??s tels que PUX 3 o?? X peut ??tre F, Cl, Br ou I quand il r??agit avec les atomes d'halog??ne ; PuF 4 est ??galement consid??r??. Les oxyhalog??nures suivantes sont respect??es: PuOCl, PuOBr et Puoi. Il r??agit avec le carbone pour former PUC, azote pour former PuN et silicium pour former PUSI 2.
Les creusets utilis??s pour contenir plutonium doivent ??tre capables de r??sister ?? son fortement des propri??t??s r??ductrices. Les m??taux r??fractaires tels que le tantale et le tungst??ne , ainsi que les oxydes plus stables, borures, carbures, nitrures et siliciures peuvent tol??rer. Fusion dans un Four ?? arc ??lectrique peut ??tre utilis?? pour produire de petits lingots de m??tal sans avoir besoin d'un creuset.
Le c??rium est utilis?? comme un milieu simulant chimique du plutonium pour le d??veloppement de confinement, extraction, et d'autres technologies.
Structure ??lectronique
Le plutonium est un ??l??ment dans lequel la ??lectrons 5f sont la fronti??re de transition entre d??localis??e et localis??e; il est donc consid??r?? comme l'un des ??l??ments les plus complexes. Le comportement anormal de plutonium est caus??e par sa structure ??lectronique. La diff??rence d'??nergie entre les sous-couches 6d et 5f est tr??s faible. La taille de l'enveloppe de 5f est juste assez pour permettre ?? des ??lectrons pour former des liaisons dans le r??seau, sur la limite entre tr??s localis??e et le comportement de collage. La proximit?? des niveaux d'??nergie conduit ?? des configurations d'??lectrons de faible ??nergie avec plusieurs niveaux d'??nergie ??gales proches. Cela conduit ?? 5f n 7s deux concurrentes et 5f n-1 7s 2 6d une configurations, ce qui provoque la complexit?? de son comportement chimique. La nature hautement directionnel des orbitales 5f est responsable de liaisons covalentes directionnels dans les mol??cules complexes et de plutonium.
Alliages
Le plutonium peut former alliages et compos??s interm??diaires avec la plupart des autres m??taux. Les exceptions comprennent le lithium , sodium , potassium , rubidium et c??sium des m??taux alcalins ; et magn??sium , calcium , strontium et baryum des m??taux alcalino-terreux ; et l'europium et l'ytterbium de la des m??taux des terres rares. Exceptions partielles comprennent les m??taux r??fractaires chrome , le molybd??ne , le niobium , le tantale et le tungst??ne , qui sont solubles dans le plutonium liquide, mais insoluble ou seulement l??g??rement soluble dans l'plutonium solide. Le gallium , l'aluminium , l'am??ricium , le scandium et c??rium peut stabiliser la phase δ de plutonium pour la temp??rature ambiante. Silicon , l'indium , le zinc et le zirconium permettent la formation de l'??tat de δ m??tastable lorsqu'il est refroidi rapidement. Des quantit??s ??lev??es de hafnium , l'holmium et le thallium permet ??galement retenir une partie de la phase δ ?? la temp??rature ambiante. Le neptunium est le seul ??l??ment qui peut stabiliser la phase α ?? des temp??ratures plus ??lev??es.
alliages de plutonium peuvent ??tre produites par addition d'un m??tal fondu pour le plutonium. Si le m??tal d'alliage est suffisamment r??ducteur, le plutonium peut ??tre ajout?? sous la forme d'oxydes ou halog??nures. La phase de δ plutonium gallium et le plutonium-alliages d'aluminium sont produites en ajoutant plutonium (III) le fluorure de gallium ou de l'aluminium en fusion, qui a l'avantage d'??viter le contact direct avec plutonium m??tal hautement r??actif.
- Plutonium-gallium est utilis?? pour stabiliser la phase δ de plutonium, en ??vitant l'α-phase et questions connexes α-δ. Son utilisation principale est en fosses de implosion armes nucl??aires.
- Le plutonium-aluminium est une alternative ?? l'alliage Pu-Ga. Ce est l'??l??ment d'origine consid??r?? pour la stabilisation de phase δ, mais sa tendance ?? r??agir avec les particules alpha et la lib??ration des neutrons diminue sa facilit?? d'utilisation pour les puits d'armes nucl??aires. Le plutonium alliage d'aluminium peut ??galement ??tre utilis?? en tant que composant de combustible nucl??aire.
- Alliage de plutonium-gallium-cobalt (PuCoGa 5) est un supraconducteur non conventionnel, montrant la supraconductivit?? inf??rieur ?? 18,5 kelvin , un ordre de grandeur plus ??lev?? que le plus ??lev?? entre syst??mes de fermions lourds, et a de grandes courant critique.
- Le plutonium alliage de zirconium peut ??tre utilis?? comme combustible nucl??aire.
- Plutonium-c??rium et le plutonium-c??rium-alliages de cobalt sont utilis??s comme combustibles nucl??aires.
- Le plutonium-uranium, avec environ 15 ?? 30 mol.% De plutonium, peut ??tre utilis?? comme combustible nucl??aire pour les r??acteurs ?? neutrons rapides. Son la nature pyrophorique et de haute sensibilit?? ?? la corrosion au point d'auto-inflammation ou d??sagr??gation apr??s l'exposition ?? l'air exigent d'alliage avec d'autres composants. Ajout d'aluminium, de carbone ou de cuivre ne ont pas am??liorer les taux de d??sint??gration nettement, de zirconium et d'alliages de fer ont une meilleure r??sistance ?? la corrosion mais ils se d??sint??grer en plusieurs mois dans l'air ainsi. L'addition de titane et / ou zirconium augmente consid??rablement le point de fusion de l'alliage.
- Le plutonium-uranium-titane et le plutonium de l'uranium et de zirconium ont ??t?? ??tudi??s pour ??tre utilis??s comme combustibles nucl??aires. L'addition du troisi??me ??l??ment augmente la r??sistance ?? la corrosion, r??duit l'inflammabilit??, et am??liore la ductilit??, usinabilit??, la force et la dilatation thermique. Plutonium-uranium-molybd??ne a la meilleure r??sistance ?? la corrosion en formant un film protecteur d'oxydes, mais le titane et le zirconium sont pr??f??r??s pour raisons de physique.
- Thorium-uranium et de plutonium a ??t?? ??tudi??e comme un combustible nucl??aire pour les r??acteurs ?? neutrons rapides.
Occurrence
Des traces d'au moins trois isotopes du plutonium (plutonium 238, 239 et 244) peuvent ??tre trouv??s dans la nature. Petites traces de plutonium-239, quelques-uns parties par billion, et son produits de d??sint??gration sont pr??sents naturellement dans certains minerais concentr??s d'uranium, comme le naturelle r??acteur de fission nucl??aire en Oklo, Gabon . Le ratio de plutonium-239 ?? l'uranium au Gisement d'uranium de Cigar Lake Mine varie de 2,4 ?? 10 -12 ?? 44 ?? 10 -12. M??me de petites quantit??s de primordiale plutonium-244 se produisent naturellement en raison de sa relativement longue demi-vie d'environ 80 millions d'ann??es. Ces traces de Pu 239 proviennent de la fa??on suivante: En de rares occasions, 238 U subit la fission spontan??e, et dans le processus, le noyau ??met un ou deux neutrons libres avec un peu d'??nergie cin??tique. Lorsque l'un de ces neutrons frappe le noyau d'un autre atome de U 238, il est absorb?? par l'atome, qui devient 239 U. Avec une demi-vie relativement courte, U-239 se d??sint??gre en neptunium -239 (239 Np), puis 239 se d??sint??gre en Np 239 Pu.
Depuis l'isotope vie relativement longue du plutonium-240 se produit dans le cha??ne de d??sint??gration du plutonium-244, il devrait ??galement ??tre pr??sent, mais 10 000 fois plus rare encore. Enfin, excessivement petites quantit??s de plutonium-238, attribu??s ?? la incroyablement rare la double d??sint??gration b??ta de l'uranium-238, ont ??t?? trouv??s dans les ??chantillons d'uranium naturel.
Des traces infimes de plutonium sont habituellement trouv??s dans le corps humain en raison de la 550 atmosph??rique et sous l'eau essais nucl??aires qui ont ??t?? r??alis??es, et ?? un petit nombre de grands accidents nucl??aires. La plupart des essais nucl??aires dans l'atmosph??re et sous l'eau a ??t?? arr??t?? par la Trait?? limit??e Interdiction des Essais en 1963, qui a ??t?? sign?? et ratifi?? par le Etats-Unis , le Royaume-Uni , l' Union sovi??tique , et d'autres nations. Les essais d'armes nucl??aires dans l'atmosph??re continue depuis 1963 par les pays non-trait??s inclus ceux de la Chine ( bombe atomique essai au-dessus du D??sert de Gobi en 1964, test de bombe ?? hydrog??ne en 1967, et des tests de suivi sur) et France (tests que r??cemment que les ann??es 1980). Parce que ce est d??lib??r??ment fabriqu?? des armes nucl??aires et des r??acteurs nucl??aires, le plutonium 239 est l'isotope le plus abondant de plutonium de loin.
Histoire
D??couverte
Enrico Fermi et une ??quipe de scientifiques ?? la Universit?? de Rome ont indiqu?? qu'ils avaient d??couvert l'??l??ment 94 en 1934. Fermi appel?? l'??l??ment hesperium et a mentionn?? dans son discours du prix Nobel en 1938. L'??chantillon ??tait en fait un m??lange de baryum , le krypton , et d'autres ??l??ments, mais ce ne ??tait pas connu ?? l'??poque parce fission nucl??aire ne avait pas ??t?? encore d??couvert.
La perc??e avec du plutonium ??tait au Cavendish Laboratory, Cambridge par Egon Bretscher et Norman Feather. Ils ont r??alis?? que un r??acteur ?? neutrons lents aliment?? avec de l'uranium serait th??oriquement produire des quantit??s importantes de plutonium-239 en tant que sous-produit. Ce est parce que l'U-238 absorbe neutrons lents et forme un nouvel isotope U-239. Le noyau de la nouvelle isotope ??met rapidement un ??lectron par d??sint??gration b??ta produire un nouvel ??l??ment d'une masse de 239 et de num??ro atomique 93. Le noyau de cet ??l??ment puis ??met ??galement un ??lectron et devient un nouvel ??l??ment de masse 239, mais avec un nombre atomique 94 et une demi-vie beaucoup plus grande. Bretscher and Feather montr?? motifs th??oriquement possible cet ??l??ment 94 serait facilement ??fissiles?? par les deux neutrons lents et rapides, et avait l'avantage suppl??mentaire d'??tre chimiquement diff??rente de l'uranium, et pourrait facilement ??tre s??par?? d'elle.
Ce nouveau d??veloppement a ??t?? ??galement confirm??e dans le travail ind??pendant par Edwin M. McMillan et Philip Abelson au Berkeley Radiation Laboratory ??galement en 1940. Nicholas Kemmer de l'??quipe Cambridge a propos?? les noms neptunium pour le nouvel ??l??ment 93 et le plutonium pour 94 par analogie avec les plan??tes ext??rieures au-del?? de Neptune et Pluton Uranus (uranium ??tant l'??l??ment 92). Les Am??ricains fortuitement sugg??r?? les m??mes noms.

Plutonium (sp??cifiquement, le plutonium-238) a ??t?? produit et isol?? le 14 D??cembre 1940, et a identifi?? chimiquement le 23 F??vrier 1941, par le Dr Glenn T. Seaborg, Edwin M. McMillan, JW Kennedy, et AC Wahl par deuteron bombardement de l'uranium dans le 60 pouces (150 cm) cyclotron au Universit?? de Californie, Berkeley. Dans l'exp??rience 1940, le neptunium -238 a ??t?? cr???? directement par le bombardement, mais pourri par ??missions beta avec une demi-vie d'un peu plus de deux jours, ce qui indique la formation de l'??l??ment 94.
Un article relatant la d??couverte a ??t?? pr??par?? par l'??quipe et envoy?? ?? la revue Examen physique dans Mars 1941. Le document a ??t?? retir?? avant la publication apr??s la d??couverte qu'un isotope de l'??l??ment nouveau (plutonium-239) pourrait subir une fission nucl??aire d'une mani??re qui pourrait ??tre utile dans une bombe atomique . Publication a ??t?? retard??e jusqu'?? un an apr??s la fin de la Seconde Guerre mondiale en raison de probl??mes de s??curit??.
Edwin McMillan avait r??cemment nomm?? le premier ??l??ment transuranien apr??s que la plan??te Neptune et a sugg??r?? que l'??l??ment 94, ??tant l'??l??ment suivant dans la s??rie, ??tre nomm?? pour ce qui ??tait alors consid??r?? comme la plan??te suivante, Pluton . Seaborg l'origine consid??r?? comme le nom "plutium", mais plus tard, pensait que ??a ne sonnait pas aussi bon que "le plutonium." Il a choisi les lettres "PU" comme une plaisanterie, qui passaient sans pr??avis dans le tableau p??riodique. Autres noms consid??r??s par Seaborg et d'autres ??taient "ultimium" ou "extremium" en raison de la croyance erron??e qu'ils avaient trouv?? la derni??re possible ??l??ment sur le tableau p??riodique .
Les premi??res recherches
La chimie de base de plutonium a ??t?? trouv?? pour ressembler ?? l'uranium apr??s quelques mois d'??tude initiale. Les premi??res recherches a ??t?? poursuivie ?? le secret Laboratoire m??tallurgique de la Universit?? de Chicago. Le 18 Ao??t 1942, une quantit?? de trace de cet ??l??ment a ??t?? isol?? et mesur?? pour la premi??re fois. Environ 50 microgrammes de plutonium-239 combin?? ?? l'uranium et des produits de fission a ??t?? produit et seulement environ 1 microgramme a ??t?? isol??. Cette proc??dure a permis aux chimistes de d??terminer le poids atomique de l'??l??ment nouveau.
En Novembre 1943 une certaine plutonium trifluorure a ??t?? r??duite ?? cr??er le premier ??chantillon de plutonium m??tal: quelques microgrammes de billes m??talliques. Assez plutonium a ??t?? produit pour en faire le premier ??l??ment synth??tiquement pour ??tre visible ?? l'??il nu.
Les propri??t??s nucl??aires de plutonium-239 ont ??galement ??t?? ??tudi??s; les chercheurs ont trouv?? que, quand il est frapp?? par un neutron, il se brise (fissions) en lib??rant davantage de neutrons et de l'??nergie. Ces neutrons peuvent frapper d'autres atomes de plutonium-239 et ainsi de suite dans un exponentiellement vite r??action en cha??ne. Cela peut entra??ner une explosion suffisamment importante pour d??truire une ville si suffisamment de l'isotope est concentr??e pour former un masse critique.
La production au cours du Projet Manhattan
Pendant la Seconde Guerre mondiale, le gouvernement des ??tats-Unis a cr???? le Projet Manhattan, qui a ??t?? charg?? d'??laborer une bombe atomique. Les trois sites principaux de recherche et de production du projet ??taient l'installation de production de plutonium ?? ce qui est maintenant la Hanford Site, le installations d'enrichissement d'uranium ?? Oak Ridge, Tennessee, et de la recherche et la conception des armes laboratoire, maintenant connu comme Los Alamos National Laboratory.

Le premier r??acteur de production fait que le plutonium 239 est le X-10 Graphite r??acteur. Il est en ligne depuis 1943 et a ??t?? construit dans une usine de Oak Ridge qui devint plus tard le Oak Ridge National Laboratory.
Le 5 Avril 1944, Emilio Segr?? ?? Los Alamos a re??u le premier ??chantillon de plutonium produite par le r??acteur de Oak Ridge. Dans les dix jours, il a d??couvert que le plutonium du r??acteur de race avait une concentration plus ??lev??e de l'isotope du plutonium-240 que le plutonium de produit par cyclotron. Plutonium-240 a une haute taux de fission spontan??e, l'??l??vation du niveau de fond neutronique global de l'??chantillon de plutonium. L'original -type de pistolet plutonium, nom de code " Thin Man ", a d?? ??tre abandonn?? en raison-augmentation du nombre de neutrons spontan??s signifiait que pr??-explosion nucl??aire (une fizzle) serait probable.
Tout l'effort de conception de plutonium d'armes ?? Los Alamos fut bient??t remplac?? par le dispositif de l'implosion plus compliqu??e, nom de code " Fat Man. "Avec une arme d'implosion, un solide (ou, dans des conceptions plus tard, creuse) sph??re de plutonium est comprim?? ?? une haute densit?? avec des lentilles-a explosifs t??che techniquement plus difficile que de la conception de type pistolet simple, mais n??cessaire d'utiliser du plutonium ?? des fins militaires. ( L'uranium enrichi, en revanche, peut ??tre utilis?? avec les deux m??thodes.)
Construction de la Hanford R??acteur B, le premier r??acteur nucl??aire de taille industrielle pour les besoins de la production mat??rielle, a ??t?? achev?? en Mars 1945. B r??acteur produit la mati??re fissile pour les armes de plutonium utilis??s pendant la Seconde Guerre mondiale. B, D et F ??taient les r??acteurs initiaux construits ?? Hanford, et six r??acteurs au plutonium produisant suppl??mentaires ont ??t?? construits plus tard sur le site.
En 2004, un s??curit?? a ??t?? d??couvert lors de fouilles d'une tranch??e d'enfouissement ?? la Site nucl??aire de Hanford. L'int??rieur du coffre ??taient divers ??l??ments, y compris une grande bouteille en verre contenant une suspension blanch??tre qui a ensuite ??t?? identifi?? comme ??tant le plus ancien ??chantillon de plutonium de qualit?? militaire connu pour exister. l'analyse isotopique par Pacific Northwest National Laboratory a indiqu?? que le plutonium dans la bouteille a ??t?? fabriqu?? dans le X-10 r??acteur ?? Oak Ridge en 1944.
Bombes atomiques Trinity et Fat Man
Le premier essai de bombe atomique, nom de code ??Trinity?? et a explos?? le 16 Juillet 1945, pr??s de Alamogordo, Nouveau-Mexique, a utilis?? du plutonium comme mati??re fissile. La conception de l'implosion de ?? gadget ??, comme le dispositif Trinity ??tait le nom de code, utilis?? lentilles explosifs conventionnels pour compresser une sph??re de plutonium en une masse supercritique, qui a ??t?? simultan??ment douch??s avec des neutrons de la "Urchin", un initiateur en polonium et le b??ryllium ( source de neutrons: (Α, n) la r??action). Ensemble, ils ont assur?? une r??action en cha??ne d'emballement et d'explosion. L'arme globale pesait plus de 4 tonnes, bien qu'il utilise seulement 6,2 kg de plutonium dans son noyau.Environ 20% du plutonium utilisé dans l'arme subit Trinity fission, ce qui entraîne une explosion avec une énergie équivalente à environ 20 000tonnes de TNT.
Une conception identique a été utilisée dans le "Fat Man "bombe atomique larguée surNagasaki,le Japon, le 9 Août 1945, tuant 70.000 personnes et en blessant un autre 100.000. Le " Little Boy "bombe larguée surHiroshima trois jours plus tôt utilisél'uranium 235, le plutonium pas . Le Japon a capitulé le 15 Août au généralDouglas MacArthur. Seulement après l'annonce des premières bombes atomiques était l'existence de plutonium rendu public.
L'utilisation de la Guerre froide et les déchets
D'importants stocks de plutonium de qualité militaire ont été construits à la fois par l' Union soviétique et l' États-Unis pendant la guerre froide . Les réacteurs américains de Hanford et le site de Savannah River en Caroline du Sud ont produit 103 tonnes, et on estime que 170 tonnes de plutonium de qualité militaire a été produit en URSS. Chaque année, environ 20 tonnes de l'élément est encore produite en tant que sous-produit de la puissance nucléaire industrie. Autant que 1000 tonnes de plutonium peuvent être dans le stockage de plus de 200 tonnes de ce soit à l'intérieur ou extrait d'armes nucléaires. SIPRI estime le plutonium monde stocks en 2007 environ 500 tonnes, réparties à parts égales entre l'arme et les stocks civils.

Depuis la fin de la guerre froide, ces stocks sont devenus un centre de problèmes de prolifération nucléaire. Aux États-Unis, certains plutonium extrait du démantèlement des armes nucléaires est fondu pour former les journaux de verre de l'oxyde de plutonium qui pèsent deux tonnes. Le verre est faite de borosilicates mélangés avec le cadmium et le gadolinium . Ces journaux sont prévues pour être enfermé dans l'acier inoxydable et stocké autant que 4 km (2 mi) souterraine dans des trous de forage qui seront remblayées avec b??ton. à partir de 2008, la seule installation aux États-Unis qui a été prévu pour stocker le plutonium dans ce chemin était le Yucca Mountain, qui est d'environ 100 miles (160 km) au nord-est de Las Vegas, Nevada . L'opposition locale et de l'Etat à ce plan retardé les efforts pour stocker les déchets nucléaires à Yucca Mountain. En Mars 2010, le ministère de l'Énergie a retiré sa demande de licence pour le dépôt de Yucca Mountain "avec préjudice» et le financement éliminé pour le Bureau de la gestion des déchets radioactifs civile, qui avait géré le site de Yucca Mountain depuis 25 ans, l'annulation du programme.
Expérimentation médicale
Pendant et après la fin de la Seconde Guerre mondiale, les scientifiques travaillant sur ??????le projet Manhattan et d'autres projets de recherche d'armes nucléaires ont mené des études sur les effets du plutonium sur les animaux de laboratoire et des sujets humains. Les études animales ont constaté que quelques milligrammes de plutonium par kilogramme de tissu est une dose létale.
Dans le cas de sujets humains, cela impliquait l'injection de solutions contenant (en général) cinq microgrammes de plutonium dans des patients de l'hôpital pensé pour être soit en phase terminale, ou d'avoir une espérance de vie de moins de dix ans, soit en raison de l'âge ou de l'état de la maladie chronique. Cela a été réduit à un microgramme en Juillet 1945 après des études animales ont constaté que la façon dont le plutonium lui-même distribué dans les os était plus dangereux que le radium .
Dix-huit des sujets humains ont été injectés avec du plutonium sans consentement éclairé. Les tests ont été utilisés pour créer des outils de diagnostic pour déterminer l'absorption de plutonium dans le corps afin de développer des normes de sécurité pour travailler avec du plutonium.
L'épisode est maintenant considéré comme une violation grave de l'éthique médicale et du serment d'Hippocrate. Des commentateurs plus sympathiques ont noté que, si elle était certainement une brèche dans la confiance et l'éthique, "les effets des injections de plutonium ne sont pas aussi dommageable pour les sujets que les premiers reportages peints, ils ne se sont donc sans conséquence que de nombreux scientifiques, alors et maintenant , croire. "
Applications
Explosifs

L'isotope du plutonium-239 est un composant clé dans fissiles des armes nucléaires , en raison de sa facilité de la fission et de la disponibilité. Enveloppant de la bombe la fosse de plutonium dans un sabotage (une couche facultative de matière dense) diminue la quantité de plutonium nécessaire pour atteindre une masse critique en reflétant neutrons fuient de nouveau dans le noyau de plutonium. Cela réduit la quantité de plutonium nécessaire pour atteindre la criticité de 16 kg à 10 kg, ce qui est une sphère avec un diamètre d'environ 10 centimètres (4 in). Cette masse critique est d'environ un tiers de ce que l'uranium-235.
Le " Fat Man "bombes au plutonium de -Type produites au cours de laManhattan Project utilisés compression explosive du plutonium à obtenir des densités nettement plus élevées que la normale, combinées avec une source de neutrons central pour commencer la réaction et augmenter l'efficacité. Ainsi, seulement 6,2 kg de plutonium ont été nécessaires pour unexplosif rendement équivalent à 20 kilotonnes de TNT. (Voir aussi types d'armes nucléaires.) Hypothétiquement, aussi peu que 4 kg de plutonium et peut-être même moins pourrait être utilisé pour faire une seule bombe atomique en utilisant des dessins d'assemblage très sophistiqués.
Mixed oxyde fuel
Le combustible nucléaire usé à partir normales réacteurs à eau légère contient du plutonium, mais il est un mélange de plutonium-242, 240, 239 et 238. Le mélange est pas suffisamment enrichi pour des armes nucléaires efficaces, mais peut être utilisé une fois comme combustible MOX. Accidentelle capture des neutrons provoque la quantité de plutonium-242 et 240 de croître chaque fois que le plutonium est irradiée dans un réacteur à basse vitesse neutrons "thermiques", de sorte que, après le deuxième cycle, le plutonium ne peut être consommé par les réacteurs à neutrons rapides. Si les réacteurs à neutrons rapides ne sont pas disponibles (le cas normal), plutonium excédentaire est habituellement mis au rebut, et constitue la composante la plus longue durée des déchets nucléaires. Le désir de consommer ce plutonium et autres transuraniens carburants et de réduire la radiotoxicité des déchets est la raison habituelle ingénieurs nucléaires donnent de faire les réacteurs à neutrons rapides.
Le processus chimique le plus commun, PUREX ( P lutonium- UR anium EX traction) RETRAITE combustible nucléaire usé d'extraire du plutonium et de l'uranium qui peut être utilisé pour former un oxyde mixte " de combustible MOX "pour une réutilisation dans les réacteurs nucléaires. Plutonium de qualité peut être ajouté au mélange de carburant. Combustible MOX est utilisé dans les réacteurs à eau légère et se compose de 60 kg de plutonium par tonne de combustible; après quatre ans, les trois quarts du plutonium est brûlé (transformé en d'autres éléments). réacteurs surgénérateurs sont spécifiquement conçus pour créer du matériel fissile plus que ce qu'ils consomment.
Combustible MOX a été en usage depuis les années 1980 et est largement utilisé en Europe. En Septembre 2000, les Etats-Unis et la Fédération de Russie ont signé un accord de gestion de plutonium et de Disposition par laquelle chaque convenu de disposer de 34 tonnes de plutonium de qualité militaire. Le US Department of Energy prévoit de disposer de 34 tonnes de plutonium de qualité militaire aux États-Unis avant la fin de 2019 par la conversion du plutonium à un combustible MOX pour être utilisé dans les réacteurs nucléaires commerciaux.
Combustible MOX améliore combustion totale. Une tige de combustible est retraité après trois ans d'utilisation à éliminer les déchets, qui d'ici là représentent 3% du poids total des tiges. Toute uranium ou de plutonium isotopes produits au cours de ces trois années sont de gauche et la tige remonte en production. La présence d'un maximum de 1% de gallium par masse dans le grade d'arme alliage de plutonium a le potentiel d'interférer avec le fonctionnement à long terme d'un réacteur à eau légère.
Plutonium extrait du combustible usé du réacteur pose un moins important risque de prolifération, en raison de la contamination excessive non fissile du plutonium-240 et le plutonium-242. La séparation des isotopes est impossible. Un réacteur dédié fonctionnant sur ??????très faible taux de combustion (exposition donc minime du nouvellement formé Pu-239 à neutrons supplémentaires qui l'amène à être transformé en isotopes lourds de plutonium) est généralement nécessaire pour produire un matériau approprié pour une utilisation dans efficaces des armes nucléaires . Alors que le plutonium "de qualité militaire» est défini pour contenir au moins 92% de plutonium-239 (du plutonium), les Etats-Unis ont réussi à faire exploser un dispositif sous-20kt à partir de plutonium censé contenir seulement environ 85% de plutonium-239, dite «de qualité carburant» plutonium. Le plutonium "de qualité réacteur» produite par un cycle de combustion de LWR régulière contient généralement moins de 60% ??????de Pu-239, avec jusqu'à 30% parasite Pu-240 / Pu-242, et 10-15% fissile Pu-241. On ne sait pas si un dispositif utilisant le plutonium obtenu à partir de déchets nucléaire civil retraité peut être exploser, mais un tel dispositif pourrait hypothétiquement long feu et la propagation de matières radioactives sur une grande région urbaine. Le AIEA classe conservatrice plutonium de tous les vecteurs isotopiques matériau «utilisation directe», qui est, "matières nucléaires qui peuvent être utilisés pour la fabrication d'explosifs composants nucléaires sans transmutation ou enrichissement supplémentaire".
241Ama récemment été suggéré pour l'utilisation comme un agent dénaturant en plutonium des barres de combustible du réacteur pour limiter davantage son potentiel de prolifération.
Pr??cautions
Toxicit??
Isotopes et des composés de plutonium sont radioactifs et accumulent dans la moelle osseuse. la contamination par de l'oxyde de plutonium a résulté de catastrophes nucléaires et les accidents radioactifs, y compris les accidents nucléaires militaires où les armes nucléaires ont brûlées. Les études sur les effets de ces plus petits de presse, ainsi que de la très répandue maladie de l'empoisonnement de rayonnement et de la mort à la suite des bombardements atomiques d'Hiroshima et de Nagasaki, ont fourni des informations considérables sur les dangers, les symptômes et le pronostic de l'empoisonnement de rayonnement, ce qui dans le cas de la japonais Hibakusha / survivants était en grande partie sans rapport avec l'exposition directe du plutonium.
Au cours de la désintégration du plutonium, trois types de rayonnement sont libérés-alpha, bêta et gamma. Le rayonnement alpha peut voyager à une courte distance et ne peut pas voyager à travers la couche externe morte de la peau humaine. Le rayonnement bêta peut pénétrer la peau humaine, mais ne peut pas aller tout le chemin à travers le corps. Le rayonnement gamma peut aller tout le chemin à travers le corps. Alpha, bêta, et gamma sont toutes les formes de rayonnement ionisant. Soit une exposition aiguë ou à long terme porte un risque de résultats de santé graves, y compris la maladie des rayons, des dommages génétiques, le cancer et la mort. Le risque augmente avec la quantité d'exposition.
Même si le rayonnement alpha peut pas pénétrer la peau, ingestion ou inhalation de plutonium fait irradier les organes internes. Le squelette, où le plutonium est absorbée, et le foie, où il recueille et se concentre, sont à risque. Le plutonium est pas absorbé dans le corps de manière efficace lorsqu'il est ingéré; seulement 0,04% d'oxyde de plutonium est absorbé après l'ingestion. Le plutonium absorbée par le corps est excrétée très lentement, avec une demi-vie biologique de 200 ans. Le plutonium passe lentement à travers les membranes cellulaires et les limites intestinales, de sorte absorption par ingestion et l'incorporation dans la structure osseuse se déroule très lentement.
Le plutonium est plus dangereux lorsqu'il est inhalé que lorsqu'il est ingéré. Le risque de cancer du poumon augmente une fois que le rayonnement total équivalent de dose de plutonium inhalé dépasse 400 mSv. Le département américain de l'énergie estime que le risque de cancer de la durée de vie de l'inhalation de particules de plutonium 5000, chacun d'environ 3 microns de large, soit 1% par rapport à l'arrière-plan moyenne américaine. L'ingestion ou l'inhalation de grandes quantités peut provoquer aiguë empoisonnement par les radiations et de la mort; aucun être humain est connu pour être mort parce que d'inhaler ou d'ingérer le plutonium, et beaucoup de gens ont des quantités mesurables de plutonium dans leurs corps. Le danger d'inhalation est environ 23.000 fois supérieure à celle de l'uranium de qualité militaire, le danger d'ingestion d'environ 130 000 fois plus grande.
Le " particules théorie chaud »dans lequel une particule de poussière de plutonium rayonne une tache localisée du tissu pulmonaire a été testé et trouvé faux telles particules sont plus mobiles que le pensait initialement et la toxicité est pas mesurable augmenté en raison de la forme de particules.
Lorsqu'il est inhalé, le plutonium peut passer dans la circulation sanguine. Une fois dans le sang, se déplace de plutonium dans le corps et dans les os, le foie ou d'autres organes du corps. Le plutonium qui atteint généralement organes du corps reste dans le corps pendant des décennies et continue à exposer le tissu environnant au rayonnement et donc peut provoquer le cancer.
Une citation couramment cité par Ralph Nader, stipule qu'un livre de poussière de plutonium se répandre dans l'atmosphère serait suffisant pour tuer 8 milliards de personnes. Cependant, les calculs montrent qu'une livre de plutonium pourrait tuer plus de 2 millions de personnes par inhalation. Cela rend la toxicité du plutonium à peu près équivalent à celui de gaz nerf.
Plusieurs populations de personnes qui ont été exposés à la poussière de plutonium (par exemple, les personnes vivant sous le vent des sites d'essais du Nevada, les survivants de Nagasaki, les travailleurs des installations nucléaires, et les patients en phase terminale "" injectés avec Pu en 1945-46 pour étudier le métabolisme Pu) ont été attentivement suivie et analysée. Ces études ne montrent généralement pas de toxicité du plutonium particulièrement élevé ou les résultats de cancer induit plutonium, comme Albert Stevens qui a survécu dans la vieillesse après avoir été injecté avec du plutonium. "Il y avait environ 25 travailleurs de Los Alamos National Laboratory qui ont inhalé une quantité considérable de poussière de plutonium au cours des années 1940; selon la théorie chaud particules, chacun d'eux a une chance d'être mort d'un cancer du poumon en maintenant de 99,5%, mais il a pas eu un cancer du poumon unique parmi eux ".
Le plutonium a un goût métallique.
potentiel de criticité

les questions de toxicité côté, les soins doivent être prises pour éviter l'accumulation de quantités de plutonium qui approchent masse critique, en particulier parce que la masse critique de plutonium est seulement un tiers de celle de l'uranium-235. Une masse critique de plutonium émet des quantités mortelles de neutrons et de les rayons gamma. plutonium en solution est plus susceptible de former une masse critique que la forme solide en raison de la modération de l'hydrogène dans l'eau.
accidents de criticité se sont produits dans le passé, certains d'entre eux avec des conséquences létales. La manipulation imprudente des briques de carbure de tungstène autour d'une sphère de plutonium de 6,2 kg a entraîné une dose mortelle de rayonnement à Los Alamos le 21 Août 1945, lorsque le scientifique Harry K. Daghlian, Jr. a reçu une dose estimée à 5,1 Sievert (510 rems) et décédé 25 jours plus tard. Neuf mois plus tard, un autre scientifique de Los Alamos, Louis Slotin, est mort d'un accident similaire impliquant un réflecteur de béryllium et le même noyau de plutonium (le soi-disant " noyau démon ») qui avaient coûté la vie à Daghlian. Ces incidents ont été romancés dans le film 1989 Les Maîtres de l'ombre .
En Décembre 1958, lors d'un processus de purification du plutonium à Los Alamos, une masse critique a été formé dans une cuve de mélange, ce qui a entraîné la mort d'un opérateur chimique nomméCecil Kelley. Autre accidents nucléaires ont eu lieu dans l'Union soviétique,le Japon, leRoyaume- Unis, et de nombreux autres pays.
Inflammabilit??
Plutonium métallique est un risque d'incendie, surtout si le matériau est finement divisée. Dans un environnement humide, le plutonium forme d'hydrures sur sa surface, qui sont pyrophoriques et peuvent enflammer à l'air à température ambiante. Plutonium dilate jusqu'à 70% de volume en oxyde et peut donc casser son récipient. La radioactivité de la matière brûlante est un danger supplémentaire. sable de l'oxyde de magnésium est probablement le matériau le plus efficace pour éteindre un incendie de plutonium. Il refroidit le matériau de combustion, agissant comme un dissipateur de chaleur, et aussi des blocs de l'oxygène. Précautions particulières sont nécessaires pour stocker ou manipuler du plutonium sous une forme quelconque; généralement sec atmosphère de gaz inerte est nécessaire.
Transport
Air
Les règlements du gouvernement américain de transport aérien permettent le transport de plutonium par voie aérienne, sous réserve de restrictions sur d'autres matières dangereuses transportées sur le même vol, les exigences d'emballage, et l'arrimage dans la partie arrière de l'avion.
En 2012, les médias ont révélé que le plutonium a été volé sur la Norvège sur commerciales compagnies aériennes autour de passagers tous les deux ans, y compris une fois en 2011. Règlement permet à un avion de transport de 15 grammes de matière fissile. Ces transports de plutonium est sans problèmes, selon un conseiller principal ( de seniorrådgiver ) au Statens strålevern.
![\ Mathrm {^ {238} _ {\ 92} U \ + \ ^ _ {1} {0} n \ \ longrightarrow \ ^ {239} _ {\ 92} U \ \ xrightarrow [23,5 \ min] {\ beta ^ -} \ ^ {239} _ {\ 93} Np \ \ xrightarrow [2,3565 \ d] {\ beta ^ -} \ ^ {239} _ {\ 94}} Pu](../../images/2301/230147.png)
![\ Mathrm {^ {238} _ {\ 92} U \ + \ ^ _ {2} {1} D \ \ longrightarrow \ ^ {238} _ {\ 93} Np \ + \ 2 \ ^ {1} {_ 0} n \ quad; \ quad ^ {238} _ {\ 93} Np \ \ xrightarrow [2,117 \ d] {\ beta ^ -} \ ^ {238} _ {\ 94}} Pu](../../images/2301/230148.png)
