
Tungst??ne
Contexte des ??coles Wikip??dia
SOS Enfants produite ce site pour les ??coles ainsi que ce site de vid??o sur l'Afrique . Avec enfants SOS vous pouvez choisir de parrainer des enfants dans plus de cent pays
| Tungst??ne | ||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
74 W | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apparence | ||||||||||||||||||||||||||||||||||||||||||||||||||||
blanc gris??tre, brillant  | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propri??t??s g??n??rales | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nom, symbole, nombre | tungst??ne, W, 74 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Prononciation | / t ʌ ŋ s t ən / TUNG -stən; / w ʊ l fa r əm / Wuul -frəm | |||||||||||||||||||||||||||||||||||||||||||||||||||
| ??l??ment Cat??gorie | m??tal de transition | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Groupe, p??riode, bloc | 6, 6, r?? | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Poids atomique standard | 183,84 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuration ??lectronique | [ Xe ] 4f 14 5d quatre 6s 2 2, 8, 18, 32, 12, 2 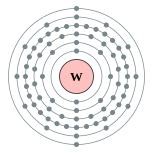 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Histoire | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| D??couverte | Torbern Bergman (1781) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Premier isolement | Juan Jos?? Elhuyar et Fausto Elhuyar (1783) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Propri??t??s physiques | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phase | solide | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Densit?? (?? proximit?? rt) | 19,25 g ?? cm -3 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Liquid densit?? au mp | 17,6 g ?? cm -3 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Point de fusion | 3695 K , 3422 ?? C, 6192 ?? F | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Point d'??bullition | 5828 K, 5555 ?? C, 10 031 ?? F | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Point critique | 13 892 K, MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| La chaleur de fusion | 35,3 kJ ?? mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Chaleur de vaporisation | 806,7 kJ ?? mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacit?? thermique molaire | 24,27 J ?? mol -1 ?? K -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| La pression de vapeur | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propri??t??s atomiques | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ??tats d'oxydation | 6, 5, 4, 3, 2, 1, 0, -1, -2 (L??g??rement acide oxyde) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| ??lectron??gativit?? | 2,36 (??chelle de Pauling) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| ??nergies d'ionisation | 1e: 770 kJ ?? mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 2??me: 1700 kJ ?? mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon atomique | 139 h | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon covalente | 162 ?? 19 heures | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscellan??es | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Crystal structure | cubique centr??  | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Ordre magn??tique | paramagn??tique | |||||||||||||||||||||||||||||||||||||||||||||||||||
| R??sistivit?? ??lectrique | (20 ?? C) 52,8 nΩ ?? m | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivit?? thermique | 173 W ?? m -1 ?? K -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Dilatation thermique | (25 ?? C) 4,5 pm ?? m -1 ?? K -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Le module d'Young | 411 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Module de cisaillement | 161 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Module Bulk | 310 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Coefficient de Poisson | 0,28 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Duret?? Mohs | 7,5 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Duret?? Vickers | 3430 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Duret?? Brinell | 2570 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Num??ro de registre CAS | 7440-33-7 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| La plupart des isotopes stables | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Article d??taill??: Isotopes de tungst??ne | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
Tungst??ne, aussi connu comme le wolfram, est un ??l??ment chimique avec le symbole chimique W et de num??ro atomique 74. Le mot de tungst??ne vient de la langue su??doise tung sten directement traduisible en pierre lourde, si le nom est Volfram en su??dois pour la distinguer de Scheelite, en su??dois tungst??ne alternativement nomm??.
A, rare disque m??tallique dans des conditions standard lorsque non combin??e, le tungst??ne se trouve naturellement sur Terre que dans les compos??s chimiques. Il a ??t?? identifi?? comme un ??l??ment nouveau en 1781, et le premier isol?? comme un m??tal en 1783. Il est important minerais comprennent wolframite et scheelite. Le ??l??ment libre est remarquable pour sa robustesse, en particulier le fait qu'il a le plus haut point de fusion de tous les non- m??taux alli??s et le deuxi??me plus ??lev?? de tous les ??l??ments apr??s le carbone . De plus remarquable est la densit?? ??lev??e de 19,3 fois celle de l'eau, comparable ?? celle de l'uranium et l'or , et beaucoup plus ??lev??es (environ 1,7 fois) que celle de plomb . Tungst??ne avec des quantit??s mineures d'impuret??s est souvent cassants et dur, ce qui rend difficile ?? travail. Toutefois, le tungst??ne tr??s pur, mais encore difficile, est plus ductile, et peut ??tre coup?? avec un disque en acier scie ?? m??taux.
De nombreux alliages de tungst??ne ont de nombreuses applications, notamment dans incandescence filaments d'ampoules, Tubes ?? rayons X (?? la fois comme le filament et la cible), des ??lectrodes de soudage TIG , et superalliages. La duret?? de tungst??ne et de haute densit?? donnent applications militaires ?? p??n??trer projectiles. Compos??s tungst??ne sont le plus souvent utilis??s industriellement comme catalyseurs .
Le tungst??ne est le seul m??tal de la troisi??me transition s??rie qui est connu pour se produire dans biomol??cules, o?? il est utilis?? dans quelques esp??ces de bact??ries et arch??es. Ce est l'??l??ment le plus lourd connu pour ??tre utilis?? par ne importe quel organisme vivant. Tungsten interf??re avec le molybd??ne et le cuivre m??tabolisme, et est peu toxique pour la vie animale.
Histoire
En 1781, Carl Wilhelm Scheele d??couvrit qu'un nouveau l'acide , acide tungstique, pourrait ??tre fabriqu?? ?? partir de scheelite (?? l'??poque nomm?? tungst??ne). Scheele et Torbern Bergman a sugg??r?? qu'il pourrait ??tre possible d'obtenir un nouveau m??tal en r??duisant cet acide. En 1783, Jos?? et Fausto Elhuyar trouv?? un acide fabriqu?? ?? partir de wolframite qui ??tait identique ?? l'acide tungstique. Plus tard cette ann??e, en Espagne, les fr??res ont r??ussi ?? isoler le tungst??ne par r??duction de cet acide avec charbon de bois, et ils sont cr??dit??s de la d??couverte de l'??l??ment.
Dans la Seconde Guerre mondiale , le tungst??ne a jou?? un r??le important dans les relations politiques de fond. Portugal, comme la principale source europ??enne de l'??l??ment, a ??t?? mis sous pression des deux c??t??s, en raison de ses gisements de minerai de wolframite ?? Panasqueira. La r??sistance de tungst??ne ?? des temp??ratures ??lev??es et de son renforcement des alliages ont fait une mati??re premi??re importante pour l'industrie de l'armement.
??tymologie
Le nom "tungst??ne" (?? partir de la Nordic tung sten, qui signifie ??lourde pierre??) est utilis?? en anglais, fran??ais, et bien d'autres langues que le nom de l'??l??ment. Tungsten ??tait l'ancien nom su??dois pour la scheelite min??rale. L'autre nom "Wolfram" (ou "Volfram"), utilis?? par exemple dans la plupart des langues europ??ennes (surtout germaniques et slaves), est d??riv??e de la min??rale wolframite, et ce est aussi l'origine de son symbole chimique, W. Le nom "wolframite?? est d??riv?? de l'allemand ??Rahm loup" ("la suie de loup?? ou ??cr??me loup??), le nom donn?? au tungst??ne par Johan Gottschalk Wallerius en 1747. Ceci, ?? son tour, d??rive de ??Lupi spuma", le nom Georg Agricola utilis?? pour l'??l??ment en 1546, ce qui se traduit en anglais par ??mousse de loup?? ou ??cr??me?? (l'??tymologie ne est pas tout ?? fait certain), et est une r??f??rence aux grandes quantit??s d' ??tain consomm??s par le min??ral lors de son extraction.
Caract??ristiques
Propri??t??s physiques
En forme brute de tungst??ne, ce est un gris acier dur m??tallique qui est souvent fragile et difficile ?? travail. Si fait tr??s pur, le tungst??ne conserve son duret?? (qui est sup??rieure ?? celle de nombreux aciers), et devient suffit qu'elle peut ??tre travaill?? facilement mall??able. Il est travaill?? par forgeage, dessin, ou extrusion. Objets tungst??ne sont aussi couramment form??s par frittage.
De tous les m??taux ?? l'??tat pur, le tungst??ne a le plus haut point de fusion (3422 ?? C , 6192 ?? F) le plus bas la pression de vapeur (?? des temp??ratures sup??rieures 1650 ?? C, 3000 ?? F) et le plus haut r??sistance ?? la traction. Le tungst??ne a le plus bas coefficient de dilatation thermique de ne importe quel m??tal pur. La faible dilatation thermique et un point de fusion ??lev?? et r??sistance ?? la traction du tungst??ne provenir forte des liaisons covalentes form??es entre les atomes de tungst??ne par les ??lectrons 5d. Alliage de petites quantit??s de tungst??ne acier augmente consid??rablement son t??nacit??.
Tungsten existe sous deux principales formes cristallines α et β:. Le premier a un corps-centr?? structure cubique et est la forme la plus stable. La structure de la phase β est appel??e A15 cube; il est m??tastable, mais peut coexister avec la phase α dans des conditions ambiantes en raison de la synth??se de non-??quilibre ou la stabilisation par des impuret??s. Contrairement ?? la phase α qui cristallise dans les grains isom??triques, la forme de β pr??sente une colonne habitude. La phase α a une trois fois plus faible et une r??sistivit?? ??lectrique beaucoup plus faible temp??rature de transition supraconductrice T c de la phase β: ca. 0,015 K vs 04/01 K; m??langer les deux phases permet d'obtenir des valeurs intermedicate T c. La valeur T C peut ??galement ??tre ??lev??e par alliage de tungst??ne avec un autre m??tal (par exemple 7,9 K pour W Tc ). De tels alliages de tungst??ne sont parfois utilis??s dans des circuits supraconducteurs ?? basse temp??rature.
Isotopes
Tungst??ne naturelle se compose de cinq isotopes dont la moiti??-vies sont si longues qu'elles peuvent ??tre consid??r??es comme stables . Th??oriquement, tous les cinq peut se d??sint??grer en isotopes de l'??l??ment 72 ( hafnium ) par ??mission alpha, mais seulement 180 W a ??t?? observ??e pour le faire avec une demi-vie de (1,8 ?? 0,2) x 10 ?? 18 ans; en moyenne, cela donne environ deux d??sint??grations alpha de 180 W dans un gramme de tungst??ne naturel par an. Les autres isotopes naturels ne ont pas ??t?? observ??s ?? la pourriture, contraignant leurs demi-vies d'??tre
- 182 W, T 1/2> 1,7 ?? 10 20 ann??es
- 183 W, T> 8 1/2 x 10 19 ann??es
- 184 W, T 1/2> 1,8 ?? 10 20 ann??es
- 186 W, T 1/2> 4,1 ?? 10 18 ann??es
Un autre 30 artificielle radio-isotopes de tungst??ne ont ??t?? caract??ris??s, les plus stables qui sont 181 W avec une demi-vie de 121,2 jours, 185 W avec une demi-vie de 75,1 jours, 188 W avec une demi-vie de 69,4 jours, 178 W avec un La demi-vie de 21,6 jours et 187 W avec une demi-vie de 23,72 h. Tout le reste isotopes radioactifs ont une demi-vie de moins de trois heures, et la plupart d'entre eux ont des demi-vies inf??rieures ?? 8 minutes. Le tungst??ne a ??galement 4 ??tats Meta, le plus stable ??tre 179m W (T ?? 6,4 minutes).
Propri??t??s chimiques
Tungst??ne ??l??mentaire r??siste attaque par l'oxyg??ne, les acides , et alcalis.
La plus courante formelle ??tat d'oxydation du tungst??ne est 6, mais il pr??sente tous les ??tats d'oxydation de -2 ?? 6. Tungst??ne combine g??n??ralement avec l'oxyg??ne pour former le jaune oxyde tungstique, WO 3, qui se dissout dans des solutions alcalines aqueuses pour former des ions tungstate, WO 2-
4.
Tungst??ne carbures (W 2 C et WC) sont produites par le chauffage de tungst??ne en poudre avec le carbone . W 2 C est r??sistant ?? l'attaque chimique, mais il r??agit fortement avec le chlore pour former hexachlorure de tungst??ne (CMT 6).
En solution aqueuse, donne le tungstate des h??t??ropolyacides et polyoxom??tallates anions dans des conditions neutres et acides. Comme tungstate est progressivement trait?? ?? l'acide, il donne le premier soluble, m??tastable "paratungstate A" anion , W
7 O 6-
24, qui au fil du temps se transforme en l'anion moins soluble "paratungstate B", H
2 W
12 O 10-
42. En outre acidification produit l'anion m??tatungstate tr??s soluble, H
2 W
12 O 6-
40, apr??s que l'??quilibre soit atteint. L'ion m??tatungstate existe comme un cluster sym??trique de douze tungst??ne oxyg??ne octa??dres connu sous le nom Anion Keggin. Beaucoup d'autres anions polyoxom??tallates existent comme des esp??ces m??tastables. L'inclusion d'un atome diff??rent, tel que le phosphore ?? la place des deux centrales hydrog??nes en m??tatungstate produit une grande vari??t?? d'acides, tels que les h??t??ropolyacides acide phosphotungstique H 3 PW 12 O 40.
Le trioxyde de tungst??ne peut former compos??s d'intercalation avec les m??taux alcalins. Elles sont connues comme bronzes; un exemple est tungst??ne sodium bronze.
Occurrence
Le tungst??ne est disponible dans les min??raux wolframite ( fer - mangan??se tungstate, (Fe, Mn) WO 4), scheelite ( calcium tungstate, (CaWO 4), ferberite (FeWO 4) et H??bn??rite (MnWO 4). La Chine a produit 51 000 tonnes de concentr?? de tungst??ne en 2009, qui ??tait de 83% de la production mondiale. En pr??lude ?? la Seconde Guerre mondiale la production de la Chine du tungst??ne jou?? un r??le que la Chine pourrait utiliser ce levier pour exiger une assistance mat??rielle du gouvernement am??ricain. La plupart du reste de la production provenaient de Russie (2500 t), le Canada (1964 t), la Bolivie (1023 t), en Autriche (900 t), le Portugal (900 t), la Tha??lande (600 t), le Br??sil (500 t), le P??rou (500 t) et le Rwanda (500 t). Le tungst??ne est ??galement consid??r?? comme un min??rale en raison des pratiques contraires ?? l'??thique mini??res observ??es en R??publique d??mocratique du Congo de conflit.
R??le biologique
Tungst??ne, au num??ro atomique 74, est l'??l??ment le plus lourd connu pour ??tre biologiquement fonctionnel, avec le prochain le plus lourd ??tant iode (Z = 53). Bien que non dans les eucaryotes , le tungst??ne est utilis??e par certaines bact??ries. Par exemple, enzymes appel??s oxydor??ductases utilisent tungst??ne est similaire ?? molybd??ne en l'utilisant dans une tungst??ne complexe avec pt??rine molybdopt??rine (molybdopt??rine, malgr?? son nom, ne contient pas de molybd??ne, mais peut complexe avec soit du molybd??ne ou du tungst??ne en cours d'utilisation par des organismes vivants). enzymes de tungst??ne utilisant r??duisent g??n??ralement acides carboxyliques en ald??hydes. Le tungst??ne oxydor??ductases peuvent ??galement catalyser les oxydations. La premi??re enzyme de tungst??ne n??cessitant d'??tre d??couvert n??cessite ??galement le s??l??nium, et dans ce cas la paire de tungst??ne-s??l??nium peut fonctionner de mani??re analogue ?? la liaison de molybd??ne-soufre de certains molybd??ne cofacteur n??cessitant enzymes. L'une des enzymes de la famille des oxydor??ductase qui emploient parfois tungst??ne (bact??rienne formiate d??shydrog??nase H) est connu d'utiliser une version de s??l??nium et de molybd??ne molybdopt??rine. Bien que la xanthine d??shydrog??nase contenant du tungst??ne ?? partir de bact??ries se est r??v??l??e contenir molydopterin tungst??ne et ??galement non li??e aux prot??ines du s??l??nium, un complexe de tungst??ne-molybdopt??rine s??l??nium n'a pas ??t?? d??finitivement d??crit.
Dans le sol, le tungst??ne m??tal se oxyde ?? l' anions tungstate. Il peut ??tre de mani??re s??lective ou non s??lective par certains import?? organismes procaryotes et peuvent suppl??er molybdate dans certains enzymes. Son effet sur l'action de ces enzymes est, dans certains cas et dans d'autres inhibiteurs positifs. La chimie du sol d??termine comment le tungst??ne polym??rise; sols alcalins provoquent tungstates monom??res; acides sols provoquent tungstates polym??res.
Le tungstate de sodium et le plomb ont ??t?? ??tudi??s pour leur effet sur les vers de terre. Le plomb se est r??v??l?? ??tre l??tale ?? des niveaux bas et le tungstate de sodium ??tait beaucoup moins toxique, mais le tungstate compl??tement inhib??e leur la capacit?? de reproduction.
Tungst??ne a ??t?? ??tudi?? comme un m??tabolisme de cuivre biologique antagoniste, dans un r??le similaire ?? l'action du molybd??ne. Il a ??t?? trouv?? que tetrathiotungstates peuvent ??tre utilis??s comme le cuivre biologique produits chimiques de ch??lation, similaires ?? la tetrathiomolybdates.
Production


Environ 61 300 tonnes de concentr??s de tungst??ne ont ??t?? produites dans l'ann??e 2009. Le tungst??ne est extrait de ses minerais en plusieurs ??tapes. Le minerai est finalement converti en tungst??ne (VI) oxyde (WO 3), qui est chauff?? avec de l'hydrog??ne ou du carbone pour produire du tungst??ne en poudre. Parce que de la haute temp??rature de fusion de tungst??ne, il ne est pas commercialement viable pour jeter de tungst??ne lingots. Au lieu de cela, le tungst??ne en poudre est m??lang?? avec de petites quantit??s de poudre de nickel ou d'autres m??taux, et fritter. Au cours du processus de frittage, le nickel diffuse dans le tungst??ne, produisant un alliage.
Le tungst??ne peut aussi ??tre extrait par r??duction ?? l'hydrog??ne de WF 6:
- WF 6 + 3 H 2 → W + 6 HF
ou d??composition pyrolytique:
- WF 6 → 3 W + F 2 ( Δ H = r +)
Tungsten ne est pas n??goci?? comme un contrat ?? terme et ne peut ??tre suivi sur les ??changes comme le Londres Bourse des m??taux. Les prix sont g??n??ralement indiqu??s pour concentr?? de tungst??ne ou de WO 3. Si converti ?? l'??quivalent de m??tal, ils ??taient environ 19 000 par tonne en 2009.
Applications


Environ la moiti?? du tungst??ne est consomm?? pour la production de mat??riaux durs - ?? savoir carbure de tungst??ne - avec l'utilisation majeure reste ??tant dans les alliages et aciers. Moins de 10% est utilis?? dans d'autres compos??s chimiques .
Les mat??riaux durs
Le tungst??ne est principalement utilis?? dans la production de mat??riaux durs ?? base de carbure de tungst??ne, une des plus difficiles carbures, avec un point de 2770 ?? C de fusion. WC est un moyen efficace conducteur ??lectrique, W 2 C, mais l'est moins. WC est utilis?? pour faire r??sistant ?? l'usure abrasifs et les couteaux et les couteaux pour perceuses, scies circulaires, fraisage et outils utilis??s par les m??taux, travail du bois, tourner miniers , p??troliers industries et des comptes et de la construction pour environ 60% de la consommation actuelle de tungst??ne.
Les bijoux industrie fait des cycles de carbure de tungst??ne fritt??, carbure de tungst??ne composite / m??tal, ainsi que le tungst??ne m??tallique. Parfois, les fabricants et les d??taillants se r??f??rent ?? du carbure de tungst??ne comme m??tal, mais ce est une c??ramique. En raison de la duret?? de carbure de tungst??ne, anneaux faits de ce mat??riau sont extr??mement r??sistant ?? l'abrasion, et tiendra une finition polie plus de bagues en tungst??ne m??tallique. Anneaux en carbure de tungst??ne sont fragiles, cependant, et peuvent se fissurer sous un coup sec.
Alliages
La duret?? et la densit?? du tungst??ne sont appliqu??es ?? obtenir heavy metal alliages. Un bon exemple est acier ?? grande vitesse, qui peut contenir jusqu'?? 18% de tungst??ne. Point de fusion ??lev?? de tungst??ne tungst??ne fait un bon mat??riau pour des applications telles que les tuy??res de fus??es, par exemple dans le UGM-27 Polaris Missile mer-sol. Superalliages contenant du tungst??ne, comme Hastelloy et Stellite, sont utilis??s dans aubes de turbine et des pi??ces r??sistant ?? l'usure et rev??tements.
Armements
Tungst??ne, g??n??ralement alli?? avec du nickel et du fer ou du cobalt pour former des alliages lourds, est utilis?? dans l'??nergie cin??tique de p??n??tration comme une alternative ?? l'uranium appauvri, dans des applications o?? de l'uranium la radioactivit?? est probl??matique, ou lorsque de l'uranium suppl??mentaire propri??t??s pyrophoriques ne sont pas n??cessaires (par exemple, dans ordinaires petites balles d'armes con??ues pour p??n??trer l'armure de corps). De m??me, les alliages de tungst??ne ont ??galement ??t?? utilis??s dans des coquilles de canon, grenades et missiles, de cr??er des ??clats d'obus supersonique. Le tungst??ne a ??galement ??t?? utilis?? dans Explosifs m??tal dense et inerte, qui l'utilisent comme poudre dense pour r??duire les dommages collat??raux, tout en augmentant la l??talit?? des explosifs dans un petit rayon.
applications chimiques
Tungsten (IV) de sulfure est une temp??rature ??lev??e et lubrifiant est un composant de catalyseurs pour hydrod??sulfuration. MoS2 est plus commun??ment utilis?? pour ces applications.
Tungst??ne les oxydes sont utilis??s dans gla??ures c??ramiques et calcium / magn??sium tungstates sont largement utilis??s dans ??clairage fluorescent. Cristal tungstates sont utilis??s comme d??tecteurs ?? scintillation en physique nucl??aire et m??decine nucl??aire. D'autres sels qui contiennent du tungst??ne sont utilis??s dans l'industrie chimique et industries de bronzage.
l'oxyde de tungst??ne (WO 3) est incorpor?? dans r??duction catalytique (SCR) des catalyseurs s??lectifs trouv??s dans les centrales au charbon. Ces catalyseurs convertissent oxydes d'azote ( NOx) en azote (N 2) et d'eau (H 2 O) avec de l'ammoniac (NH 3). L'oxyde de tungst??ne contribue ?? la r??sistance physique du catalyseur et prolonge la vie du catalyseur.
usages de niche
Les applications n??cessitant sa haute densit?? comprennent poids, contrepoids, quilles de ballast pour les yachts, la queue ballast pour les avions commerciaux, et comme ballast dans les voitures de course pour NASCAR et la Formule Un ; uranium appauvri est ??galement utilis?? ?? ces fins, en raison de haute densit?? similaire. 75 kg blocs de tungst??ne ont ??t?? utilis??s comme des ??dispositifs de masse de l'??quilibre de croisi??re" sur la partie du v??hicule d'entr??e de la sonde Mars Science Laboratory 2012. Ce est un mat??riau id??al pour l'utiliser comme un dolly pour rivetage, o?? la masse n??cessaire pour de bons r??sultats peut ??tre r??alis?? dans un bar compact. Les alliages ?? haute densit?? de tungst??ne avec du nickel, du cuivre ou du fer sont utilis??s dans de haute qualit?? fl??chettes (pour permettre un plus petit diam??tre et groupements ainsi strictes) ou pour leurres de p??che (perles de tungst??ne permettent la vol??e ?? couler rapidement). Certains types de cordes pour instruments de musique sont enroul??s des fils de tungst??ne.
le tungstate de sodium est utilis?? en Le r??actif de Folin-Ciocalteu, un m??lange de diff??rents produits chimiques utilis??s dans le "Dosage de Lowry" pour l'analyse de la teneur en prot??ines.
substitution de l'or
Sa densit??, analogue ?? celle de l'or, du tungst??ne permet d'??tre utilis?? en joaillerie comme une alternative ?? l'or ou le platine . Tungst??ne m??tallique est plus difficile que celle des alliages d'or (mais pas aussi dur que le carbure de tungst??ne), et est hypoallerg??nique, ce qui est utile pour anneaux qui r??sister aux rayures, en particulier dans des conceptions avec un bross??.
Parce que la densit?? est si semblable ?? l'or (tungst??ne est seulement 0,36% moins dense), le tungst??ne peut ??galement ??tre utilis?? dans de contrefa??on lingots d'or, comme en plaquant un bar de tungst??ne avec de l'or, qui a ??t?? observ??e depuis les ann??es 1980, ou de prendre une barre d'or existante, du forage de trous, et le remplacement de l'or enlev?? avec des tiges de tungst??ne. Les densit??s sont pas exactement les m??mes, et d'autres propri??t??s de l'or et de tungst??ne diff??rer, mais le tungst??ne plaqu?? or passeront des tests superficielles.
tungst??ne plaqu?? or est disponible dans le commerce de la Chine (la principale source de tungst??ne), ?? la fois dans les bijoux et des bars.
??lectronique
Parce qu'il conserve sa r??sistance ?? des temp??ratures ??lev??es et a une haute temp??rature de fusion , le tungst??ne ??l??mentaire est utilis?? dans de nombreuses applications ?? haute temp??rature, tels que ampoule, tube cathodique, et filaments des tubes ?? vide, des ??l??ments chauffants, et tuy??res de moteurs de fus??e. Son point de fusion ??lev?? de tungst??ne rend ??galement appropri?? pour l'a??rospatiale et ?? haute temp??rature utilise comme, les applications de chauffage et soudage ??lectrique, notamment dans le soudage ?? l'arc de gaz de tungst??ne processus (aussi appel?? gaz inerte de tungst??ne (TIG)).
En raison de ses propri??t??s conductrices et une inertie chimique relative, le tungst??ne est ??galement utilis?? dans ??lectrodes, et dans l'??metteur des conseils dans des instruments ?? faisceaux d'??lectrons qui utilisent canons ?? ??mission de champ, tels que microscopes ??lectroniques. En ??lectronique, le tungst??ne est utilis?? comme mat??riau d'interconnexion dans des circuits int??gr??s , entre le dioxyde de silicium un mat??riau di??lectrique et les transistors. Il est utilis?? dans les films m??talliques, qui remplacent le c??blage utilis?? dans l'??lectronique conventionnelle d'une couche de tungst??ne (ou de molybd??ne ) sur silicium .
La structure ??lectronique de tungst??ne en fait l'un des principales sources pour Objectifs de rayons X, et aussi pour prot??ger des radiations de haute ??nergie (par exemple dans le industrie radiopharmaceutique pour le blindage des ??chantillons radioactifs FDG). poudre de tungst??ne est utilis?? comme mat??riau de remplissage en plastique composites, qui sont utilis??s en tant que substitut non toxique pour le plomb dans balles, tir, et de rayonnement boucliers. Depuis dilatation thermique de cet ??l??ment est similaire ?? verre de borosilicate, il est utilis?? pour la fabrication de joints verre-m??tal.
Pr??cautions
Parce que le tungst??ne est rare et ses compos??s sont g??n??ralement inerte, les effets de tungst??ne sur l'environnement sont limit??es. Le m??diane dose l??tale DL 50 d??pend fortement de l'animal et la voie d'administration et varie entre 59 mg / kg (par voie intraveineuse, lapin) et 5000 mg / kg (poudre de tungst??ne m??tallique, intraperitoneale, rats).
demande de brevet
Le tungst??ne est unique parmi les ??l??ments qu'il a fait l'objet de poursuites judiciaires. En 1928, un tribunal am??ricain a rejet?? La tentative de General Electric pour breveter, renversant Le brevet US 1.082.933 accord?? en 1913 ?? William D. Coolidge.
