
Krypton
?? propos de ce ??coles s??lection Wikipedia
SOS Enfants a essay?? de rendre le contenu plus accessible Wikipedia par cette s??lection des ??coles. M??res SOS chaque regard apr??s une une famille d'enfants parrain??s .
| Krypton | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
36 Kr | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apparence | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
gaz incolore, pr??sentant une lueur blanch??tre dans un champ ??lectrique ??lev??  Raies spectrales du krypton | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propri??t??s g??n??rales | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nom, symbole, nombre | krypton, Kr, 36 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Prononciation | / k r ɪ p t ɒ n / Krip -ton | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ??l??ment Cat??gorie | gaz nobles | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Groupe, p??riode, bloc | 18 (gaz rares) , 4, p | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poids atomique standard | 83,798 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuration ??lectronique | [ Ar ] 3d 10 4s 2 4p 6 2, 8, 18, 8 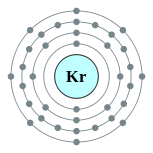 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Histoire | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| D??couverte | William Ramsay et Morris Travers (1898) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Premier isolement | William Ramsay et Morris Travers (1898) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propri??t??s physiques | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phase | gaz | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densit?? | (0 ?? C, 101,325 kPa) 3,749 g / L | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Liquid densit?? ?? BP | 2,413 g ?? cm -3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point de fusion | 115,79 K , -157,36 ?? C, -251,25 ?? F | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point d'??bullition | 119,93 K, -153,22 ?? C, -244,12 ?? F | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point triple | 115,775 K (-157 ?? C), 73,2 kPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point critique | 209,41 K, 5,50 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| La chaleur de fusion | 1,64 kJ ?? mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chaleur de vaporisation | 9,08 kJ ?? mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacit?? thermique molaire | 5 R / 2 = 20,786 J ?? mol -1 ?? K -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| La pression de vapeur | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propri??t??s atomiques | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ??tats d'oxydation | 2, 1, 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ??lectron??gativit?? | 3,00 (??chelle de Pauling) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ??nergies d'ionisation | 1er: 1350,8 kJ ?? mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2??me: 2350,4 kJ ?? mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3??me: 3565 kJ ?? mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon covalente | 116 ?? 16 heures | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon de Van der Waals | 202 h | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscellan??es | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Crystal structure | cubique ?? faces centr??es  | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ordre magn??tique | diamagn??tique | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivit?? thermique | 9,43 ?? 10 -3 W ?? m -1 ?? K -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vitesse du son | (Gaz, 23 ?? C) 220, (liquide) 1120 m ?? s -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Num??ro de registre CAS | 7439-90-9 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| La plupart des isotopes stables | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Article d??taill??: Isotopes du krypton | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Krypton (du grec : κρυπτός kryptos "le cach????) est un ??l??ment chimique avec le symbole Kr et de num??ro atomique 36. Ce est un membre du groupe 18 (gaz nobles) ??l??ments. Inodore, incolore et insipide, gaz noble , le krypton se produit dans ??tat de traces dans l' atmosph??re , est isol?? par distillation fractionn??e de l'air liqu??fi??, et est souvent utilis?? avec d'autres gaz rares lampes fluorescentes. Krypton est inerte ?? des fins plus pratiques.
Krypton, comme les autres gaz nobles , peut ??tre utilis?? dans l'??clairage et la photographie. Krypton la lumi??re a un grand nombre de lignes spectrales, et la sortie de la lumi??re ??lev??e de krypton dans les plasmas lui permet de jouer un r??le important dans de nombreux lasers de forte puissance gaz (krypton ions et lasers excim??res), qui pr??l??vent sur l'une des nombreuses raies spectrales ?? amplifier. Il existe ??galement un sp??cifique Laser ?? fluorure de krypton. La puissance ??lev??e et la facilit?? relative de fonctionnement de tubes ?? d??charge krypton caus??s (1960-1983) la dur??e officielle d'un m??tres ?? d??finir en termes de 605 nm (rouge-orange) raie spectrale de krypton-86.
Histoire

Krypton a ??t?? d??couvert en Grande-Bretagne en 1898 par Sir William Ramsay, un chimiste ??cossais, et Morris Travers, un chimiste anglais, dans les r??sidus de se ??vaporer laiss?? presque tous les composants de l'air liquide. Neon a ??t?? d??couvert par une proc??dure similaire par les m??mes travailleurs seulement quelques semaines plus tard. William Ramsay a re??u le 1904 Prix Nobel de chimie pour la d??couverte d'une s??rie de gaz rares , y compris le krypton.
En 1960, un accord international d??fini le compteur en termes de longueur d'onde de la lumi??re ??mise par le krypton-86 isotope (longueur d'onde de 605,78 nm). Cet accord a remplac?? le m??tre ??talon de longue date situ?? ?? Paris , qui ??tait une barre de m??tal fait d'une platine - iridium alliage (la barre a ??t?? estim?? ?? l'origine pour ??tre un dix-millioni??me d'un quadrant de la Terre circonf??rence polaire s '), et ??tait lui-m??me remplac?? par une d??finition bas??e sur la vitesse de la lumi??re - une constante physique fondamentale. Cependant, en 1927, le Conf??rence internationale sur les poids et mesures a red??fini le compteur en termes de rouge de cadmium raie spectrale (1 m = 1,553,164.13 longueurs d'onde). En Octobre 1983, le m??me bureau d??fini le m??tre comme la distance que la lumi??re voyage dans un vide pendant 1/299 792 458 s.
Caract??ristiques
Le krypton est caract??ris??e par plusieurs lignes d'??mission tranchants ( signatures spectrales) ??tre le plus fort de vert et jaune. Il est l'un des produits de l'uranium fission . solidifi??s krypton est blanc et cristallin avec un face-centr??e cubique la structure cristalline, qui est une propri??t?? commune de tous les gaz rares (?? l'exception de l'h??lium, avec une structure de cristal hexagonale compacte).
Isotopes
Naturellement krypton se produisant est faite de six stables isotopes. En outre, une trentaine d'isotopes instables et isom??res sont connus. 81 Kr, le produit de r??actions atmosph??riques, est produit avec les autres d'origine naturelle des isotopes du krypton. ??tre radioactive, il a une demi-vie de 230.000 ans. Krypton est tr??s volatil lorsqu'il est ?? proximit?? des eaux de surface, mais 81 Kr a ??t?? utilis?? pour la datation des vieux (50,000-800,000 ans) les eaux souterraines.
85 Kr est un gaz rare radioactif inerte avec une demi-vie de 10,76 ann??es. Elle est produite par la fission de l'uranium et du plutonium , comme dans la bombe nucl??aire essais et r??acteurs nucl??aires. 85 Kr est lib??r?? lors du retraitement des crayons combustibles de r??acteurs nucl??aires. Les concentrations au P??le Nord sont 30% plus ??lev?? qu'?? la P??le Sud en raison du m??lange convectif.
Chimie
Comme les autres gaz nobles, le krypton est chimiquement non r??actif. Cependant, apr??s la premi??re synth??se r??ussie de x??non dans les compos??s 1962, la synth??se de krypton difluorure (KrF 2) a ??t?? signal?? en 1963. Dans la m??me ann??e, KrF 4 a ??t?? rapport?? par Grosse, et al., mais a par la suite r??v??l?? ??tre une identification erron??e. Il ya aussi des informations non v??rifi??es d'un baryum sel d'un krypton oxoacide. Ar Kr + et Kr H + ions polyatomiques ont ??t?? ??tudi??s et il existe des preuves pour Kr Xe ou KrXe +.
Compos??s ?? krypton li??s ?? des atomes autres que le fluor ont ??galement ??t?? d??couvertes. La r??action de 2 avec B KrF (OTEF 5) 3 produit un compos?? instable, Kr (OTEF 5) 2, qui contient une liaison oxyg??ne-krypton. Une liaison krypton-azote se trouve dans le cation [HC≡N-Kr-F] +
, Produit par la r??action de 2 avec KrF [HC≡NH] +
[ASF -
6] inf??rieure ?? -50 ?? C. HKrCN et HKrC≡CH (krypton-hydrure cyanure et hydrokryptoacetylene) ont ??t?? signal??s ?? ??tre stable jusqu'?? 40 K .
Occurrence naturelle
La Terre a conserv?? tous les gaz rares qui ??taient pr??sents lors de sa formation ?? l'exception de l'h??lium . La concentration du krypton dans le atmosph??re est d'environ 1 ppm. Il peut ??tre extrait de l'air liquide par distillation fractionn??e. La quantit?? de krypton dans l'espace ne est pas certain, lorsque la quantit?? est d??riv??e de l'activit?? m??t??orique et que des vents solaires. Les premi??res mesures sugg??rent une surabondance de krypton dans l'espace.
Applications


Plusieurs lignes d'??mission de Krypton font les rejets de gaz krypton ionis?? apparaissent blanch??tres, qui ?? son tour rend ampoules ?? krypton-utile dans la photographie comme une source de lumi??re blanche brillante. Krypton est ainsi utilis??e dans certains types de flashs photographiques utilis??s ?? haute vitesse la photographie . Le gaz Krypton est ??galement combin?? avec d'autres gaz ?? faire des signes lumineux qui brillent avec une lumi??re verd??tre-jaune vif.
Krypton m??lange avec de l'argon en tant que gaz de remplissage des lampes fluorescentes d'??conomie d'??nergie. Cela r??duit leur consommation d'??nergie. Malheureusement, cela r??duit ??galement leur production de lumi??re et soul??ve leur co??t. Krypton co??te environ 100 fois plus que l'argon. Krypton (avec x??non) est ??galement utilis?? pour remplir les lampes ?? incandescence de r??duire l'??vaporation du filament et de permettre plus les temp??ratures de fonctionnement ?? utiliser pour le filament. A r??sultats brillantes de lumi??re qui contient plus de bleu que les lampes classiques.
Pertes blanches de Krypton est souvent utilis?? ?? bon escient dans des tubes ?? d??charge de gaz de couleur, qui sont ensuite simplement peint ou teint dans d'autres moyens pour permettre la couleur d??sir??e (par exemple, " n??on "panneaux publicitaires de type o?? les lettres apparaissent dans diff??rentes couleurs sont souvent enti??rement krypton-based). Krypton est ??galement capable de densit?? de puissance beaucoup plus de lumi??re que le n??on dans la r??gion de la ligne rouge spectrale, et pour cette raison, les lasers rouges pour haute puissance lumi??re laser spectacles sont souvent lasers krypton avec des miroirs qui s??lectionnent la ligne rouge du spectre pour l'amplification laser et des ??missions, plut??t que le plus familier vari??t?? h??lium-n??on, qui ne pourrait jamais pratiquement atteindre les multi-sorties watts de lumi??re laser rouge n??cessaires pour cette application.
Krypton a un r??le important dans la production et l'utilisation de la Laser ?? fluorure de krypton. Le laser a ??t?? important dans la communaut?? de recherche sur l'??nergie de fusion nucl??aire dans des exp??riences de confinement. Le laser a grande uniformit?? du faisceau, ?? court longueur d'onde, et la possibilit?? de modifier la taille du point de suivre un culot implosion.
Dans exp??rimentale en physique des particules , le krypton liquide est utilis?? pour construire des quasi-homog??ne ??lectromagn??tique calorim??tres. Un exemple notable est le calorim??tre de la Exp??rience NA48 au CERN contenant environ 27 tonnes de krypton liquide. Cet usage est rare, puisque le liquide moins cher argon est g??n??ralement utilis??. L'avantage de krypton sur l'argon est un petit Moli??re rayon de 4,7 cm, ce qui permet une excellente r??solution spatiale et faible degr?? de chevauchement. Les autres param??tres pertinents pour l'application de la calorim??trie sont: longueur de rayonnement de X 0 = 4,7 cm, densit?? de 2,4 g / cm 3.
Les assembl??es des ??clateurs scell??es contenues dans excitateurs d'allumage utilis??s dans certains moteurs ??g??s de jet contiennent une tr??s petite quantit?? de Krypton-85 pour obtenir des niveaux d'ionisation coh??rente et un fonctionnement uniforme.
Krypton-83 a des applications dans imagerie par r??sonance magn??tique (IRM) pour l'imagerie des voies respiratoires. En particulier, elle peut ??tre utilis??e pour distinguer entre des surfaces hydrophobes et hydrophiles contenant une voie a??rienne.
Bien que le x??non a un potentiel pour une utilisation dans la tomodensitom??trie (TDM) pour ??valuer la ventilation r??gionale, ses propri??t??s anesth??siques limitent sa fraction dans le gaz respiratoire ?? 35%. L'utilisation d'un m??lange respirable contenant 30% de x??non et de krypton 30% est comparable en efficacit?? ?? CT x??non ?? une fraction de 40%, tout en ??vitant les effets ind??sirables d'une fraction ??lev??e de x??non gazeux.
Pr??cautions
Le krypton est consid??r?? comme non toxique asphyxiant. Krypton a un puissance narcotique sept fois plus grande que l'air, respirer un gaz contenant 50% de krypton et 50% d'air causerait une narcose similaire ?? respirer l'air ?? quatre fois la pression atmosph??rique. Ce serait comparable ?? la plong??e ?? une profondeur de 30 m (100 pi) (voir narcose ?? l'azote) et pourraient potentiellement affecter ne importe qui respire. N??anmoins, ce m??lange ne contiendra que 10% d'oxyg??ne et hypoxie serait une plus grande pr??occupation.
