
Titanio
Sabías ...
SOS Children han producido una selección de artículos de la Wikipedia para escuelas desde 2005. SOS Children ha cuidado de niños en África durante cuarenta años. ¿Puedes ayudar a su trabajo en África ?
| Titanio | ||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
22 Ti | ||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia | ||||||||||||||||||||||||||||||||||||||||||||||
plateado metálico blanco grisáceo  | ||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades generales | ||||||||||||||||||||||||||||||||||||||||||||||
| Nombre, símbolo, número | de titanio, Ti, 22 | |||||||||||||||||||||||||||||||||||||||||||||
| Pronunciación | / t aɪ t eɪ n yo ə m / TY-TAY -nee-əm | |||||||||||||||||||||||||||||||||||||||||||||
| Categoría Elemento | metal de transición | |||||||||||||||||||||||||||||||||||||||||||||
| Grupo, período, bloque | 4, 4, d | |||||||||||||||||||||||||||||||||||||||||||||
| Peso atómico estándar | 47.867 (1) | |||||||||||||||||||||||||||||||||||||||||||||
| Configuración electrónica | [ Ar ] 3d 2 4s 2 2, 8, 10, 2 | |||||||||||||||||||||||||||||||||||||||||||||
| Historia | ||||||||||||||||||||||||||||||||||||||||||||||
| Descubrimiento | William Gregor (1791) | |||||||||||||||||||||||||||||||||||||||||||||
| Primer aislamiento | Jöns Jakob Berzelius (1825) | |||||||||||||||||||||||||||||||||||||||||||||
| Nombrado por | Martin Heinrich Klaproth (1795) | |||||||||||||||||||||||||||||||||||||||||||||
| Propiedades físicas | ||||||||||||||||||||||||||||||||||||||||||||||
| Fase | sólido | |||||||||||||||||||||||||||||||||||||||||||||
| Densidad (cerca rt) | 4,506 g · cm -3 | |||||||||||||||||||||||||||||||||||||||||||||
| Líquido densidad en mp | 4,11 g · cm -3 | |||||||||||||||||||||||||||||||||||||||||||||
| Punto de fusion | 1941 K , 1668 ° C, 3034 ° F | |||||||||||||||||||||||||||||||||||||||||||||
| Punto de ebullicion | 3560 K, 3287 ° C, 5949 ° F | |||||||||||||||||||||||||||||||||||||||||||||
| Calor de fusión | 14.15 kJ · mol -1 | |||||||||||||||||||||||||||||||||||||||||||||
| El calor de vaporización | 425 kJ · mol -1 | |||||||||||||||||||||||||||||||||||||||||||||
| Capacidad calorífica molar | 25.060 J · mol -1 · K -1 | |||||||||||||||||||||||||||||||||||||||||||||
| Presión del vapor | ||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades atómicas | ||||||||||||||||||||||||||||||||||||||||||||||
| Estados de oxidación | 4, 3, 2, 1 ( óxido anfótero) | |||||||||||||||||||||||||||||||||||||||||||||
| Electronegatividad | 1,54 (escala de Pauling) | |||||||||||||||||||||||||||||||||||||||||||||
| Energías de ionización ( más) | Primero: 658.8 kJ · mol -1 | |||||||||||||||||||||||||||||||||||||||||||||
| Segundo: 1309,8 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||
| Tercero: 2652,5 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||
| Radio atómico | 147 pm | |||||||||||||||||||||||||||||||||||||||||||||
| Radio covalente | 160 ± 20:00 | |||||||||||||||||||||||||||||||||||||||||||||
| Miscelánea | ||||||||||||||||||||||||||||||||||||||||||||||
| Estructura cristalina | hexagonal compacta | |||||||||||||||||||||||||||||||||||||||||||||
| Ordenamiento magnético | paramagnético | |||||||||||||||||||||||||||||||||||||||||||||
| La resistividad eléctrica | (20 ° C) 420 nΩ · m | |||||||||||||||||||||||||||||||||||||||||||||
| Conductividad térmica | 21.9 W · m -1 · K -1 | |||||||||||||||||||||||||||||||||||||||||||||
| Expansión térmica | (25 ° C) 8,6 micras · m -1 · K -1 | |||||||||||||||||||||||||||||||||||||||||||||
| Velocidad del sonido (varilla delgada) | ( rt) 5.090 m · s -1 | |||||||||||||||||||||||||||||||||||||||||||||
| El módulo de Young | 116 GPa | |||||||||||||||||||||||||||||||||||||||||||||
| Módulo de corte | 44 GPa | |||||||||||||||||||||||||||||||||||||||||||||
| Módulo de volumen | 110 GPa | |||||||||||||||||||||||||||||||||||||||||||||
| Relación de Poisson | 0.32 | |||||||||||||||||||||||||||||||||||||||||||||
| Dureza de Mohs | 6.0 | |||||||||||||||||||||||||||||||||||||||||||||
| Dureza Vickers | 970 MPa | |||||||||||||||||||||||||||||||||||||||||||||
| Dureza Brinell | 716 MPa | |||||||||||||||||||||||||||||||||||||||||||||
| Número de registro del CAS | 7440-32-6 | |||||||||||||||||||||||||||||||||||||||||||||
| La mayoría de los isótopos estables | ||||||||||||||||||||||||||||||||||||||||||||||
| Artículo principal: Los isótopos de titanio | ||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||
El titanio es un elemento químico con el símbolo Ti y número atómico 22. Tiene una baja densidad y es un brillante, fuerte corrosión resistentes (incluyendo agua de mar , agua regia y cloro ) metal de transición con un color plata.
El titanio fue descubierto en Cornwall, Gran Bretaña , por William Gregor en 1791 y nombrada por Martin Heinrich Klaproth para el Titanes de la mitología griega . El elemento se produce dentro de una serie de yacimientos minerales, principalmente rutilo y ilmenita, que están ampliamente distribuidos en la corteza de la Tierra y litosfera, y se encuentra en casi todas las cosas que viven, rocas, cuerpos de agua y suelos. El metal se extrae de sus principales minerales a través de la Proceso Kroll o la Proceso de Hunter. Su compuesto más común, dióxido de titanio, es un popular fotocatalizador y se utiliza en la fabricación de pigmentos blancos. Otros compuestos incluyen tetracloruro de titanio (TiCl 4), un componente de fumar pantallas y catalizadores ; y tricloruro de titanio (TiCl 3), que se utiliza como catalizador en la producción de polipropileno.
El titanio puede ser aleado con hierro , aluminio , vanadio , molibdeno , entre otros elementos, para producir aleaciones ligeras y fuertes para el sector aeroespacial ( motores a reacción , misiles, y nave espacial), militares, procesos industriales (productos químicos y petroquímicos, plantas de desalinización, pulpa y papel), automoción, agroalimentario, médico prótesis, ortopedia implantes, instrumentos y archivos dentales y endodoncia, implantes dentales, artículos deportivos, joyas, teléfonos móviles y otras aplicaciones.
Las dos propiedades más útiles de la forma de metal son resistencia a la corrosión y la relación más alta resistencia-peso de cualquier metal. En su condición sin alear, el titanio es tan fuerte como algunos aceros , pero 45% más ligero. Hay dos alotrópicas formas y cinco de origen natural isótopos de este elemento, 46 a través de Ti Ti 50, con 48 siendo el más Ti abundante (73.8%). Propiedades de titanio son química y físicamente similar a circonio , porque ambos tienen el mismo número de electrones de valencia y están en el mismo grupo en la tabla periódica .
Características
Propiedades físicas
Un metálico elemento , el titanio es reconocida por su alta relación resistencia-peso. Es un metal poco densidad que es bastante dúctil (especialmente en un oxígeno ambiente exento), brillante y metálico de color blanco en el color . El punto de fusión relativamente alta (más de 1650 ° C o 3000 ° F) lo hace útil como metal refractario. Es paramagnético y tiene bastante bajo eléctricos y conductividad térmica.
Comercial (99,2% de pureza) grados de titanio tienen una resistencia a la rotura por tracción de aproximadamente 63000 psi (434 MPa), igual a la de las aleaciones de acero, de baja ley común, pero son 45% más ligero. El titanio es un 60% más denso que el aluminio, pero más de dos veces tan fuerte como la aleación de aluminio 6061-T6 más comúnmente utilizado. Ciertas aleaciones de titanio (por ejemplo, Beta C) lograr la resistencia a la tracción de más de 200 000 psi (1400 MPa). Sin embargo, el titanio pierde fuerza cuando se calienta por encima de 430 ° C (806 ° F).
El titanio es bastante difícil (aunque no tanto como algunos tipos de acero con tratamiento térmico), no magnéticos y un mal conductor de calor y electricidad. El mecanizado requiere precauciones, como el material se ablanda y biliar si no se utilizan herramientas afiladas y métodos de refrigeración adecuados. Al igual que las hechas de acero, estructuras de titanio tienen un límite de fatiga que garantiza la longevidad en algunas aplicaciones. Las aleaciones de titanio tienen rigideces específicas inferiores que en muchos otros materiales estructurales tales como aleaciones de aluminio y fibra de carbono.
El metal es un dimorfismo alótropo cuya forma alfa hexagonal cambia en un cúbico (celosía) centrada en el cuerpo β forma a 882 ° C (1620 ° F). La calor específico de la forma alfa aumenta dramáticamente a medida que se calienta a esta temperatura de transición, pero luego cae y permanece bastante constante para la forma β independientemente de la temperatura. Similar a circonio y hafnio, existe una fase omega adicional, que es termodinámicamente estable a altas presiones, pero es metaestable a presiones ambiente. Esta fase es generalmente hexagonal (ideal) o trigonal (distorsionada) y se puede ver como debido a una acústica longitudinal suave fonón de la fase β causando colapso de (111) planos de átomos.
Propiedades químicas
Como aluminio y magnesio de metal, superficies de metal de titanio y superficies de aleaciones de oxidar inmediatamente cuando se exponen al aire. El titanio reacciona fácilmente con el oxígeno a 1200 ° C (2190 ° F) en el aire, y a 610 ° C (1130 ° F) con oxígeno puro, formando dióxido de titanio. Sin embargo, es lento para reaccionar con el agua y el aire, debido a que forma una recubrimiento de óxido pasiva y protectora que protege de la reacción adicional. Cuando por primera vez formas, esta capa protectora es sólo 1-2 nm de espesor pero sigue creciendo lentamente; llegar a un espesor de 25 nm en cuatro años.
Cuando se expone a nitrógeno metal de titanio limpia se cubre con una capa de nitruro de titanio. La delgada capas de dióxido de titanio y nitruro de titanio en las superficies son muy duro y inerte.
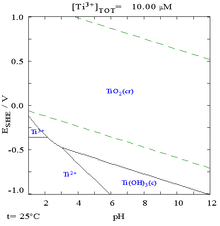
La propiedad química más conocido de titanio es su excelente resistencia a la corrosión; es casi tan resistente como el platino , capaz de resistir el ataque por diluida de ácido sulfúrico y ácido clorhídrico , así como de cloro gas, soluciones de cloruro, y la mayoría de los ácidos orgánicos. Sin embargo, es soluble en ácidos concentrados. La Diagrama de Pourbaix en la imagen muestra que el titanio es realmente termodinámicamente un metal muy reactivo.
El metal no se puede fundir al aire libre ya que se quema antes de que se alcance el punto de fusión. De fusión sólo es posible en una atmósfera inerte o en el vacío. A 550 ° C (1022 ° F), se combina con el cloro. También reacciona con los otros halógenos y absorbe hidrógeno.
El titanio es uno de los pocos elementos que arde en gas nitrógeno puro, reaccionar a 800 ° C (1470 ° F) para formar nitruro de titanio, lo que provoca la fragilización. El polvo de titanio puede formar una suspensión explosiva con el aire.
Porque el metal de titanio limpio es altamente reactivo y el titanio se une fuertemente al oxígeno, nitrógeno y muchos otros gases, filamentos de titanio se aplican en Bombas de sublimación de titanio. Bombas de sublimación de titanio son dispositivos económicos y fiables que se aplican como el último paso para crear extremadamente bajas presiones en sistemas de ultra-alto vacío.
Los experimentos han demostrado que el titanio natural se vuelve radiactivo después de que se bombardea con deuterones, emitiendo principalmente positrones y duro rayos gamma.
Compuestos

El 4 estado de oxidación domina la química de titanio, pero los compuestos en el 3 estado de oxidación son también comunes. Debido a este alto estado de oxidación, muchos compuestos de titanio tienen un alto grado de unión covalente.
Zafiros estrella y rubíes obtienen su asterismo de las impurezas de dióxido de titanio presente en ellos. Titanatos son compuestos hechos con dióxido de titanio. Titanato de bario tiene propiedades piezoeléctricas, lo que permite usarlo como un transductor en la interconversión de sonido y electricidad . Ésteres de titanio se forman por la reacción de alcoholes y tetracloruro de titanio y se utilizan para impermeabilizar telas .
Nitruro de titanio (TiN), que tiene una dureza equivalente a zafiro y carborundum (9,0 en la escala de Mohs ), se utiliza a menudo para herramientas de corte de capa, tales como brocas. También encuentra uso como un acabado decorativo de color oro, y como barrera de metal en de fabricación de semiconductores.
Tetracloruro de titanio (titanio (IV), cloruro de TiCl 4) es un líquido incoloro que se utiliza como un intermedio en la fabricación de dióxido de titanio para la pintura. Es ampliamente utilizado en la química orgánica como una Ácido de Lewis, por ejemplo en el Condensación aldólica Mukaiyama. El titanio también forma un cloruro inferior, de titanio (III) cloruro (TiCl 3), que se utiliza como una agente reductor.
Dicloruro de titanoceno es un catalizador importante para la formación de enlaces carbono-carbono. Isopropóxido de titanio se utiliza para Epoxidación de Sharpless. Otros compuestos incluyen bromuro de titanio (utilizados en la metalurgia, superaleaciones, y el cableado eléctrico de alta temperatura y recubrimientos) y carburo de titanio (que se encuentra en las herramientas de corte y recubrimientos de alta temperatura).
Aparición
| País | mil toneladas | % Del total |
|---|---|---|
| Australia | 1300 | 19.4 |
| Sudáfrica | 1160 | 17.3 |
| Canadá | 700 | 10.4 |
| India | 574 | 8.6 |
| Mozambique | 516 | 7.7 |
| China | 500 | 7.5 |
| Vietnam | 490 | 7.3 |
| Ucrania | 357 | 5.3 |
| Mundo | 6700 | 100 |
El titanio es siempre unido a otros elementos en la naturaleza. Es el noveno más abundante elemento en la Tierra corteza 's (0,63% en masa ) y el metal más abundante séptimo. Está presente en la mayoría de las rocas ígneas y en los sedimentos derivados de ellos (al igual que en los seres vivos y los cuerpos naturales de agua). De los 801 tipos de rocas ígneas analizados por el Servicio Geológico de Estados Unidos, 784 contenía titanio. Su proporción en suelos es de aproximadamente 0,5 a 1,5%.
Se distribuye ampliamente y se presenta principalmente en los minerales anatasa, brookita, ilmenita, perovskita, rutilo y titanita (sphene). De estos minerales, sólo rutilo y la ilmenita tienen importancia económica, pero incluso ellos son difíciles de encontrar en altas concentraciones. Acerca de 6,0 y 0,7 millones de toneladas de estos minerales han sido extraídos en 2011, respectivamente. Existen depósitos de ilmenita titanio incidencia significativa en el oeste de Australia , Canadá , China, , India , Mozambique , Nueva Zelanda , Noruega , Ucrania y Sudáfrica . Acerca de 186.000 toneladas de esponja de titanio metálico se produjeron en 2011, sobre todo en China (60.000 t), Japón (56.000 t), Rusia (40.000 t), Estados Unidos (32.000 t) y Kazajstán (20.700 t). Se estima que las reservas totales de titanio para superar los 600 millones de toneladas.
El titanio está contenido en meteoritos y se ha detectado en el sol y en De tipo M estrellas ; el tipo más cool de la estrella con una temperatura superficial de 3200 ° C (5790 ° F). Las rocas traídas de la Luna durante el Apolo 17 misión se compone de 12,1% TiO2. También se encuentra en carbón de ceniza, plantas , e incluso el humano cuerpo.
Isótopos
Naturalmente titanio se producen se compone de 5 estables isótopos : 46 Ti, 47 Ti, 48 Ti, 49 Ti, Ti y 50, con 48 Ti siendo la más abundante (73,8% abundancia natural). Once radioisótopos se han caracterizado, con ser más estable 44 Ti con una vida media de 63 años, 45 Ti con una vida media de 184,8 minutos, 51 Ti con una vida media de 5,76 minutos, y 52 Ti con una media vida de 1,7 minutos. Todos los restantes isótopos radiactivos tienen vidas medias que son menos de 33 segundos y la mayoría de ellos tienen vidas medias que son menos de medio segundo.
Los isótopos de titanio de gama peso atómico de 39,99 u (40 Ti) a 57.966 U (58 Ti). El primario modo de decaimiento antes del isótopo estable más abundante, 48 Ti, es captura de electrones y el modo primario después de que se emisión beta. El primario productos de desintegración antes de 48 Ti son elemento 21 ( escandio ) isótopos y los productos primarios después de son elemento 23 ( vanadio ) isótopos.
Historia

El titanio fue descubierto incluido en un mineral en Cornwall, Gran Bretaña , en 1791 por el clérigo y geólogo aficionado William Gregor, entonces vicario de Parroquia Creed. Reconoció la presencia de un nuevo elemento en la ilmenita cuando encontró arena negro por un arroyo en el cercano parroquia de Manaccan y notado la arena fue atraído por un imán . Análisis de la arena determinó la presencia de dos óxidos metálicos; óxido de hierro (que explica la atracción que el imán) y 45.25% de un óxido metálico de color blanco que no pudo identificar. Gregor, al darse cuenta de que el óxido no identificado contenía un metal que no coincidía con las propiedades de cualquier elemento conocido, informaron sus conclusiones a la Real Sociedad Geológica de Cornualles y en la revista científica alemana Annalen de Crell.
Por la misma época, Franz-Joseph Müller von Reichenstein producía una sustancia similar, pero no podía identificarlo. El óxido se redescubrió independientemente en 1795 por Químico prusiano Martin Heinrich Klaproth en rutilo de Hungría . Klaproth encontró que contenía un nuevo elemento y la llamó para el Titanes de la mitología griega . Después de escuchar sobre el descubrimiento anterior de Gregor, obtuvo una muestra de manaccanite y confirmó que contenía titanio.
Los procesos necesarios para extraer titanio de sus diversos minerales son laboriosos y costosos; no es posible reducir de la manera normal, por calentamiento en la presencia de carbono , debido a que produce carburo de titanio. Titanio metálico puro (99,9%) se preparó por primera vez en 1910 por Matthew A. Hunter en Rensselaer Polytechnic Institute por calentamiento de TiCl 4 con sodio a 700-800 ° C en el Proceso de Hunter. Titanio metálico no fue utilizado fuera del laboratorio hasta 1932 cuando William Justin Kroll demostró que podía ser producido por la reducción tetracloruro de titanio (TiCl 4) con calcio . Ocho años más tarde se perfeccionó este proceso mediante el uso de magnesio e incluso de sodio en lo que se conoció como la Proceso de Kroll. Aunque la investigación continúa en procesos más eficientes y más baratos (por ejemplo, FFC Cambridge), el proceso Kroll todavía se utiliza para la producción comercial.

Titanio de muy alta pureza se realizó en pequeñas cantidades cuando Anton Eduard van Arkel y Jan Hendrik de Boer descubrió el yoduro o barra de cristal, proceso en el año 1925, al reaccionar con el yodo y la descomposición de los vapores formados sobre un filamento caliente de metal puro.
En los años 1950 y 1960 la Unión Soviética fue pionero en el uso del titanio en aplicaciones militares y submarinos ( Alfa y Clase Mike Class) como parte de los programas relacionados con la Guerra Fría. A partir de la década de 1950, el titanio comenzó a ser utilizado ampliamente con fines de aviación militar, sobre todo en aviones de alto rendimiento, a partir de aviones como el F100 SABRE estupendo y Lockheed A-12.
En los EE.UU., el Departamento de Defensa dio cuenta de la importancia estratégica del metal y apoyó los esfuerzos iniciales de comercialización. Durante todo el período de la Guerra Fría , el titanio fue considerado un material estratégico por el gobierno de Estados Unidos, y un gran arsenal de esponja de titanio fue mantenida por la Defensa Centro Nacional de arsenales, que finalmente se agota en la década de 2000. Hoy en día, el mayor productor del mundo, basada en Rusia VSMPO-Avisma, se calcula que representa alrededor del 29% de la cuota de mercado mundial.
En 2006, la Agencia de Defensa de Estados Unidos otorgó $ 5,7 millones a un consorcio de dos empresas para desarrollar un nuevo proceso para fabricar titanio metálico en polvo. Bajo calor y presión, el polvo se puede utilizar para crear elementos fuertes, ligeros que van desde el blindaje a los componentes para las industrias aeroespacial, de transporte, y procesamiento químico.
Producción y fabricación

El procesamiento de metal de titanio se produce en 4 pasos principales: la reducción de mineral de titanio en "esponja", una forma porosa; de fusión de esponja, o una esponja además de una aleación madre para formar un lingote; fabricación primaria, donde un lingote se convierte en productos generales de molino como palanquilla, barra, placa, lámina, tira, y el tubo; y la fabricación secundaria de formas acabadas de productos de acero fundido.
Debido a que el metal reacciona con el oxígeno a altas temperaturas no pueden ser producidos por reducción de su dióxido de carbono. Por lo tanto, de metal de titanio se produce comercialmente por el Proceso Kroll, un complejo y costoso proceso por lotes. (El relativamente alto valor de mercado de titanio es principalmente debido a su procesamiento, que sacrifica otro metal caro, magnesio). En el proceso de Kroll, el óxido se convierte en primer lugar a cloruro través carbocloración, con lo que el cloro se pasa gas durante rutilo rojo vivo o ilmenita en presencia de carbono para hacer TiCl4. Este se condensa y se purificó por destilación fraccionada y luego reducida con 800 ° C fundida de magnesio en una atmósfera de argón atmósfera.
Un método más desarrollado recientemente, el Proceso Cambridge FFC, pueden llegar a sustituir el proceso de Kroll. Este método utiliza polvo de dióxido de titanio (que es una forma refinada de rutilo) como materia prima para hacer el producto final que es o bien un polvo o una esponja. Si se utilizan polvos de óxido mezclado, el producto es una aleación fabricada a un costo mucho más bajo que el proceso de fusión de múltiples etapas convencional. El proceso FFC Cambridge puede hacer que el titanio un material menos raro y caro para el industria aeroespacial y el mercado de bienes de lujo, y se podía ver en muchos productos fabricados actualmente utilizando aluminio y grados especializados de acero.
Titanio Común aleaciones se hacen por reducción. Por ejemplo, cuprotitanium (rutilo con cobre añadido se reduce), titanio ferrocarbon (ilmenita reducida con coque en un horno eléctrico), y manganotitanium (rutilo con óxidos de manganeso o de manganeso) se reducen.
- 2 FeTiO 3 + 7 Cl 2 + 6 C → 2 TiCl4 + 2 FeCl3 + 6 CO (900 ° C)
- TiCl4 + 2 Mg → 2 MgCl2 + Ti (1100 ° C)
Alrededor del 50 grados de titanio y aleaciones de titanio se designan y se utilizan en la actualidad, aunque sólo un par de docenas están fácilmente disponibles en el mercado. La ASTM Internacional reconoce 31 grados de metal de titanio y aleaciones, de los cuales los grados 1 a 4 están comercialmente puro (puro). Estos cuatro se distinguen por sus diversos grados de resistencia a la tracción, en función del oxígeno contenido, con grado 1 es el más dúctil (resistencia a la tracción más baja con un contenido de oxígeno de 0,18%), y el grado 4 (resistencia a la tracción más alta por lo menos con un contenido de oxígeno de 0,40%). Los grados restantes son aleaciones, cada uno diseñado para fines específicos, ya sea ductilidad, resistencia, dureza, resistividad eléctrica, resistencia a la fluencia, resistencia a la corrosión de los medios de comunicación específicos, o una combinación de los mismos.
La grados cubiertos por la norma ASTM y otras aleaciones también se producen para satisfacer Aeroespacial y especificaciones militares (SAE-AMS, MIL-T), normas ISO, y las especificaciones de cada país, así como las especificaciones de propiedad del usuario final para el sector aeroespacial, militar, médico, y aplicaciones industriales.
En términos de fabricación, toda la soldadura de titanio se debe realizar en una atmósfera inerte de argón o de helio con el fin de protegerlo de la contaminación con los gases atmosféricos tales como oxígeno, nitrógeno , o de hidrógeno . La contaminación causar una variedad de condiciones, tales como fragilización, lo que reducirá la integridad de las soldaduras de montaje y conducir a fallo de la junta. Producto plano comercialmente puro (hojas, láminas) se puede formar fácilmente, pero el proceso debe tener en cuenta el hecho de que el metal tiene una "memoria" y tiende a rebotar. Esto es especialmente cierto de ciertas aleaciones de alta resistencia. El titanio no puede ser soldadas sin primero pre chapado en un metal que es soldable. El metal se puede mecanizar con el mismo equipo y a través de los mismos procesos que acero inoxidable.
Aplicaciones

El titanio se utiliza en acero como elemento de aleación ( ferro-titanio) para reducir tamaño de grano y como desoxidante, y en de acero inoxidable para reducir el contenido de carbono. El titanio es a menudo aleado con aluminio (para refinar el tamaño de grano), vanadio , cobre (para endurecer), hierro , manganeso , molibdeno , y con otros metales. Las solicitudes de los productos de acero de titanio (hoja, placa, barra, alambre, piezas de forja, fundición) se pueden encontrar en el industrial, aeroespacial, de recreo, y los mercados emergentes. De titanio en polvo se utiliza en pirotecnia como fuente de partículas brillantes quema.
Pigmentos, aditivos y recubrimientos

Alrededor del 95% de mineral de titanio extraído de la Tierra está destinada para el refinamiento en dióxido de titanio (Ti O 2), una permanente intensamente blanco pigmento utilizado en pinturas, papel, pasta de dientes, y los plásticos . También se utiliza en cemento, en piedras preciosas, como un agente de opacidad óptica en papel, y un agente de fortalecimiento en las barras de pesca compuesto de grafito y palos de golf.
TiO2 en polvo es químicamente inerte, resiste la decoloración en la luz solar, y es muy opaca: esto permite a impartir un color blanco puro y brillante a los productos químicos de color marrón o gris que forman la mayoría de los plásticos de uso doméstico. En la naturaleza, este compuesto se encuentra en los minerales anatasa, brookite, y rutilo. Pintura hecha con dióxido de titanio hace bien en temperaturas extremas, y se pone de pie para entornos marinos. Dióxido de titanio puro tiene un muy alto índice de refracción y una dispersión óptica más alta que el diamante . Además de ser un pigmento muy importante, dióxido de titanio también se usa en filtros solares debido a su capacidad para proteger la piel por sí mismo. Recientemente, óxido de titanio se ha puesto en uso en purificadores de aire (como un recubrimiento de filtro), o en película utilizada para cubrir ventanas en los edificios de modo que cuando el óxido de titanio se expone a la luz UV (ya sea solar o artificial) y la humedad en el aire, se producen especies redox reactivos como los radicales hidroxilo para que puedan purificar el aire o mantener las superficies de la ventana limpia.
Aeroespacial y marina
Debido a su alto resistencia a la tracción a la relación de densidad, alta resistencia a la corrosión, resistencia a la fatiga, alta resistencia a la fisuración, y la capacidad para resistir temperaturas moderadamente altas sin rastrero, de titanio aleaciones se utilizan en aviones , blindaje, buques de guerra, nave espacial, y misiles. Para estas aplicaciones de titanio aleado con aluminio, vanadio, y otros elementos se utiliza para una variedad de componentes, incluyendo partes críticas de la estructura, las paredes de fuego, tren de aterrizaje, conductos de evacuación (helicópteros), y sistemas hidráulicos. De hecho, cerca de dos tercios de todo el metal de titanio producido se utiliza en los motores y los marcos de las aeronaves. El SR-71 "Blackbird" fue uno de los primeros aviones para hacer un amplio uso de titanio en su estructura, allanando el camino para su uso en el ejército moderno y de aviones comerciales. Se estima que 59 toneladas métricas (130.000 libras) se utilizan en el Boeing 777 , 45 en el Boeing 747 , 18 en el Boeing 737, 32 en el Airbus A340, 18 en el Airbus A330, y 12 en el Airbus A320. El Airbus A380 puede utilizar 77 toneladas métricas, incluyendo cerca de 11 toneladas en los motores. En las aplicaciones de motores, el titanio se usa para rotores, los álabes del compresor, componentes del sistema hidráulico, y barquillas. La aleación de titanio 6Al-4V representa casi el 50% de todas las aleaciones utilizadas en aplicaciones aeronáuticas.
Debido a su alta resistencia a la corrosión de agua de mar , el titanio se utiliza para fabricar ejes de la hélice y el aparejo y en el intercambiadores de calor de plantas de desalinización; en calentador de enfriadores para agua salada acuarios , hilo de pescar y líder, y para los cuchillos de los buceadores. El titanio se utiliza para la fabricación de las cajas y otros componentes de vigilancia oceánica-desplegado y dispositivos de control para uso científico y militar. La ex Unión Soviética desarrolló técnicas para la fabricación de submarinos en gran parte fuera de titanio.
Industrial

Tubos soldados de titanio y equipos de proceso (intercambiadores de calor, tanques, depósitos de proceso, válvulas) se utilizan en las industrias químicas y petroquímicas, principalmente para la resistencia a la corrosión. Aleaciones específicas se utilizan en el fondo del pozo y de níquel aplicaciones hidrometalurgia debido a su alta resistencia (por ejemplo: de titanio Beta C aleación), resistencia a la corrosión, o combinación de ambos. La industria de la pulpa y el papel utiliza titanio en equipos de proceso expuesto a medios corrosivos como el hipoclorito de sodio o cloro gas húmedo (en el bleachery). Otras aplicaciones incluyen: soldadura ultrasónica, soldadura por ola, y blancos de pulverización.
Tetracloruro de titanio (TiCl 4), un líquido incoloro, es importante como un intermedio en el proceso de hacer TiO2 y también se utiliza para producir el Catalizador de Ziegler-Natta, y se utiliza para iridize vidrio y porque humos fuertemente en el aire húmedo también se utiliza para hacer pantallas de humo.
Consumidor y arquitectónico
Titanio metal se utiliza en aplicaciones de automoción, en particular en el automóvil o motocicleta de carreras, donde la reducción de peso es crítica mientras se mantiene una alta resistencia y rigidez. El metal es generalmente demasiado caro para que sea comercializable para el mercado de consumo en general, excepto los productos de gama alta, especialmente para el mercado de las carreras / rendimiento. Último modelo Corvettes han estado disponibles con los tubos de escape de titanio.
El titanio se utiliza en muchos productos deportivos: raquetas de tenis, clubes de golf, árboles de palo de lacrosse; grillo parrillas, hockey, lacrosse, y casco de fútbol americano; y bicicletas marcos y componentes. Aunque no es un material convencional para la producción de bicicletas, bicicletas de titanio han sido utilizados por los equipos de carrera y ciclistas de aventura. Las aleaciones de titanio también se utilizan en gafas marcos. Esto se traduce en un marco duradera bastante caro, pero altamente resistente y de larga que es ligero de peso y no causa alergias en la piel. Muchos mochileros utilizan equipos de titanio, incluyendo utensilios de cocina, utensilios de cocina, linternas y estacas de la tienda. Aunque un poco más caro que las alternativas tradicionales de acero o de aluminio, estos productos de titanio pueden ser significativamente más ligero sin comprometer la resistencia. El titanio también es favorecido para el uso de herradores, ya que es más ligero y más duradero que el acero cuando se conforma en herraduras.
Titanio en ocasiones se ha utilizado en aplicaciones arquitectónicas: el monumento de 40 m (131 pies) de Yuri Gagarin , el primer hombre en viajar al espacio, en Moscú , está hecho de titanio de color atractivo del metal y la asociación con los cohetes. La Museo Guggenheim de Bilbao y el Cerritos Milenio Biblioteca fueron los primeros edificios en Europa y América del Norte, respectivamente, que se forran en paneles de titanio. Otros usos de la construcción de revestimiento de titanio incluyen el Edificio Frederic C. Hamilton en Denver , Colorado y los 107 m (350 pies) Monumento a los Conquistadores del Espacio en Moscú .
Debido a su superior resistencia y peso ligero en comparación con otros metales usados tradicionalmente en las armas de fuego (acero, acero inoxidable, y aluminio), y los avances en las técnicas de trabajo de los metales, el uso de titanio se ha extendido en la fabricación de armas de fuego. Usos primarios incluyen marcos de pistola y cilindros de revólver. Por estas mismas razones, también se utiliza en el cuerpo de los ordenadores portátiles (por ejemplo, en de Apple línea PowerBook 's).
Algunas categorías de lujo de herramientas hechas para ser ligero y resistente a la corrosión, tales como palas y linternas, están hechos de titanio o aleaciones de titanio también.
Joyas
Debido a su durabilidad, el titanio se ha vuelto más popular para la diseñadora de joyas (en particular, anillos de titanio). Su inercia hace que sea una buena opción para las personas con alergias o los que va a usar la joyería en ambientes tales como piscinas. El titanio es también aleado con oro para producir una aleación que puede ser comercializado como Oro de 24 quilates, ya que el 1% de la aleación Ti es insuficiente para requerir una marca menor. La aleación resultante es más o menos la dureza de oro de 14 quilates y por lo tanto es más durable que un elemento de oro de 24 quilates puro sería.
Durabilidad de titanio, peso ligero, abolladuras y resistencia a la corrosión hace que sea útil en la producción de relojes casos. Algunos artistas trabajan con titanio para producir obras de arte como esculturas, objetos de decoración y muebles.
La inercia y la capacidad de ser de color atractivo hace de titanio un metal popular para su uso en perforaciones en el cuerpo. El titanio puede ser anodizado para producir diversos colores, que varía el espesor de la capa de óxido de la superficie y las causas franjas de interferencia.
Médico
Porque es biocompatible (no tóxico y no es rechazada por el cuerpo), el titanio se usa en una gama de aplicaciones médicas, incluyendo instrumentos y los implantes quirúrgicos, tales como bolas de cadera y receptáculos ( reemplazo de la articulación) que puede permanecer en el lugar durante un máximo de 20 años. El titanio es a menudo aleado con aproximadamente el 4% de aluminio o 6% de Al y 4% de vanadio.
El titanio tiene la propiedad inherente a osteointegración, lo que permite su uso en implantes dentales que pueden permanecer en el lugar durante más de 30 años. Esta propiedad también es útil para aplicaciones de implantes ortopédicos. Estos se benefician de menor módulo de titanio de elasticidad ( Módulo de Young) para aproximarse más a la del hueso que los productos estén destinados a la reparación. Como resultado, las cargas esqueléticos están más uniformemente compartido entre el hueso y el implante, dando lugar a una menor incidencia de la degradación de hueso debido a la protección de esfuerzos y fracturas óseas periprotésicas que se producen en los límites de los implantes ortopédicos. Sin embargo, la rigidez aleaciones de titanio 'todavía es más de dos veces la del hueso de modo hueso adyacente soporta una carga muy reducido y puede deteriorarse.
Puesto que el titanio es no ferromagnético, los pacientes con implantes de titanio se pueden examinar de manera segura con imágenes por resonancia magnética (conveniente para los implantes a largo plazo). Preparación de titanio para la implantación en el cuerpo consiste en someter a una alta temperatura del plasma de arco que elimina los átomos de la superficie, la exposición de titanio puro que se oxida al instante.
El titanio también se utiliza para el instrumentos quirúrgicos utilizados en cirugía guiada por imagen, así como sillas de ruedas, muletas y otros productos donde la alta resistencia y bajo peso son deseables.
Almacenamiento de residuos nucleares
Debido a su resistencia a la corrosión extrema, contenedores de titanio se han estudiado para el almacenamiento a largo plazo de los residuos nucleares (contenedores que duren más de 100.000 años son posibles bajo condiciones de fabricación adecuadas para reducir los defectos en el proceso). Una de titanio "protector de goteo" también podría ser colocado sobre otros tipos de recipientes para contener además los residuos.
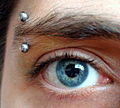
Una perforación del cuerpo de titanio.

Características cordones de soldadura en una mano de titanio cuadro de la bicicleta.

La Museo Guggenheim Bilbao se enfundó en paneles de titanio.

La anillo de titanio.

A titanio spork útil para mochileros. Cerca de 16 gramos, más ligero que un utensilio de acero, pero más fuertes que un plástico implementar.
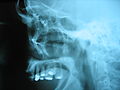
Una fractura de la órbita del ojo fue reparado mediante la estabilización de los huesos fracturados con pequeñas placas de titanio y tornillos.
Precauciones

El titanio es no tóxico incluso en grandes dosis y no juega ningún papel natural en el interior del cuerpo humano. Una cantidad estimada de 0,8 miligramos de titanio es ingerido por seres humanos cada día, pero la mayor parte pasa a través sin ser absorbida. Lo hace, sin embargo, tienen una tendencia a bio-acumularse en los tejidos que contienen sílice . Un estudio indica una posible conexión entre el titanio y El síndrome de las uñas amarillas. Un mecanismo desconocido en plantas puede utilizar titanio para estimular la producción de hidratos de carbono y estimular el crecimiento. Esto puede explicar por qué la mayoría de las plantas contienen aproximadamente 1 parte por millón (ppm) de titanio, plantas de alimentos tienen de aproximadamente 2 ppm, y la cola de caballo y ortiga contiene hasta 80 ppm.
Como un polvo o en forma de virutas de metal, metal de titanio plantea un peligro significativo de fuego y, cuando se calienta en aire , un peligro de explosión. El agua y el dióxido de carbono basados en métodos para extinguir los incendios no son eficaces en la quema de titanio; Clase D agentes de extinción de incendios de polvo seco se deben utilizar en su lugar.
Cuando se utiliza en la producción o manipulación de cloro , se debe tener cuidado de usar titanio sólo en lugares en los que no esté expuesto a secar gas cloro que puede resultar en un incendio de titanio / cloro. Existe un peligro de incendio, incluso cuando se utiliza titanio en cloro húmedo debido a la posible secado inesperada provocada por condiciones climáticas extremas.
El titanio puede incendiarse cuando una superficie fresca, no oxidado entra en contacto con oxígeno líquido. Tales superficies pueden aparecer cuando la superficie oxidada es golpeado con un objeto duro, o cuando una tensión mecánica provoca la aparición de una grieta. Esto plantea la posible limitación para su uso en sistemas de oxígeno líquido, tales como las encontradas en la industria aeroespacial.
