
Punto de fusion
Antecedentes
Esta selecci??n wikipedia ha sido elegido por los voluntarios que ayudan Infantil SOS de Wikipedia para esta Selecci??n Wikipedia para las escuelas. Ver http://www.soschildren.org/sponsor-a-child para averiguar sobre el apadrinamiento de ni??os.
El punto de fusi??n de un s??lido cristalino es el rango de temperatura a la que cambia estado de s??lido a l??quido . Aunque la frase sugerir??a una temperatura espec??fica y se utiliza com??nmente e incorrectamente, como tal, en la mayor??a de libros de texto y la literatura, la mayor??a de los compuestos cristalinos en realidad se funden en un rango de unos pocos grados o menos. En el punto de fusi??n existe la fase s??lida y l??quida en equilibrio. Cuando se considera como la temperatura del cambio inverso de l??quido a s??lido, que se conoce como el punto de congelaci??n. Debido a la capacidad de algunas sustancias a supercool, el punto de congelaci??n no se considera que es una propiedad caracter??stica de una sustancia.
Fundamentos

Para la mayor??a de las sustancias, fusi??n y puntos de congelaci??n son esencialmente iguales. Por ejemplo, el punto de fusi??n y el punto de congelaci??n del elemento mercurio es 234,32 kelvin (-38,83 ?? C o -37.89 ?? F). Sin embargo, ciertas sustancias poseen temperaturas de transici??n s??lido-l??quido diferentes. Por ejemplo, agar se funde a 85 ?? C (185 ?? F) y se solidifica a partir de 31 ?? C a 40 ?? C (89,6 ?? F a 104 ?? F); este proceso es conocido como hist??resis.
Ciertos materiales, tales como vidrio , pueden endurecer sin cristalizar; estos son llamados s??lidos amorfos. Los materiales amorfos, as?? como algunos pol??meros no tienen un verdadero punto de fusi??n ya que no hay cambio de fase abrupta a cualquier temperatura espec??fica. En su lugar, hay un cambio gradual en su propiedades viscoel??sticas m??s de una gama de temperaturas. Tales materiales se caracterizan por una temperatura de transici??n v??trea que puede ser m??s o menos definido como el punto "rodilla" de la densidad de la materia frente gr??fico de temperatura.
El punto de fusi??n del agua a 1 atm??sfera de presi??n est?? muy cerca de 0 ?? C (32 ?? F, 273,15 K), esto tambi??n se conoce como el punto de hielo. En la presencia de nucleaci??n sustancias el punto de congelaci??n del agua es el mismo que el punto de fusi??n, pero en ausencia de agua puede nucleadores supercool a -42 ?? C (-43.6 ?? F, 231 K) antes de la congelaci??n.
A diferencia del punto de ebullici??n , el punto de fusi??n es relativamente insensible a presi??n debido a la transici??n s??lido / l??quido representa s??lo un peque??o cambio en el volumen. Los puntos de fusi??n se utilizan a menudo para caracterizar compuestos org??nicos y para determinar la pureza. El punto de fusi??n de una sustancia pura es siempre superior y tiene un rango menor que el punto de una sustancia impura de fusi??n. Cuanto m??s impureza est?? presente, el punto de fusi??n m??s bajo y el m??s amplio rango. Finalmente, se alcanzar?? un punto de fusi??n m??nimo. La proporci??n de mezcla que resulta en el punto de fusi??n m??s bajo posible se conoce como el punto eut??ctico.
El elemento qu??mico con el punto de fusi??n m??s alto es de tungsteno , a 3695 K (3422 ?? C, 6192 ?? F) por lo que es excelente para su uso como filamentos de bombillas. El frecuentemente citado de carbono no se funde a la presi??n ambiente, pero sublima a aproximadamente 4000 K; una fase l??quida s??lo existe presiones por encima de 10 MPa y estimada 4300-4700 K. Tantalio carburo de hafnio (HfC Ta 4 5) es una compuesto refractario con un punto de fusi??n muy alto de 4488 K (4215 ?? C, 7619 ?? F). En el otro extremo de la escala, el helio no se congela en absoluto a presi??n normal, incluso a temperaturas infinitesimalmente cerca de cero absoluto ; presiones de m??s de 20 veces la presi??n atmosf??rica normal son necesarios.
Mediciones de punto de fusi??n
Muchos Existen t??cnicas de laboratorio para la determinaci??n de puntos de fusi??n. Un banco de Kofler es una tira de metal con un (intervalo de temperatura ambiente a 300 ?? C) gradiente de temperatura. Cualquier sustancia puede ser colocado en una secci??n de la tira revelando su comportamiento t??rmico a la temperatura en ese punto. Calorimetr??a de barrido diferencial proporciona informaci??n sobre el punto de fusi??n junto con su La entalp??a de fusi??n.
Un aparato de punto de fusi??n b??sica para el an??lisis de los s??lidos cristalinos consiste en una ba??o de aceite con una ventana transparente (m??s dise??o b??sico: una Tubo de Thiele) y una lupa simple. Los varios granos de un s??lido se colocan en un tubo de vidrio delgada y parcialmente sumergidos en el ba??o de aceite. El ba??o de aceite se calienta (y se agit??) y con la ayuda de la lupa de fusi??n (y fuente de luz externa) de los cristales individuales a una cierta temperatura puede ser observado. En los dispositivos actuales se automatiza esta detecci??n ??ptica.
Termodin??mica

No s??lo se requiere calor para elevar la temperatura del s??lido al punto de fusi??n, pero la propia fusi??n requiere calor llamado calor de fusi??n.
Desde un punto de vista de la termodin??mica, en el punto de fusi??n por el cambio en la energ??a libre de Gibbs (  ) Del material es cero, debido a que la entalp??a (
) Del material es cero, debido a que la entalp??a ( 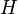 ) Y la entrop??a (
) Y la entrop??a ( 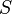 ) Del material est??n aumentando (
) Del material est??n aumentando (  ). Melting fen??meno que ocurre cuando la energ??a libre de Gibbs del l??quido se hace menor que el s??lido para ese material. En diversas presiones esto ocurre a una temperatura espec??fica. Tambi??n puede demostrarse que:
). Melting fen??meno que ocurre cuando la energ??a libre de Gibbs del l??quido se hace menor que el s??lido para ese material. En diversas presiones esto ocurre a una temperatura espec??fica. Tambi??n puede demostrarse que:

El " 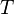 ","
"," 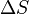 ", Y"
", Y"  "En lo anterior son, respectivamente, la temperatura en el punto de fusi??n, el cambio de entrop??a de fusi??n, y el cambio de entalp??a de fusi??n.
"En lo anterior son, respectivamente, la temperatura en el punto de fusi??n, el cambio de entrop??a de fusi??n, y el cambio de entalp??a de fusi??n.
Regla de Carnelley
En qu??mica org??nica Regla de Carnelley establecido en 1882 por Thomas Carnelley, establece que el alto simetr??a molecular est?? asociada con alto punto de fusi??n. Carnelley basa su gobierno en el examen de 15.000 compuestos qu??micos. Por ejemplo, para tres is??meros estructurales con f??rmula molecular C 5 H 12 el punto de fusi??n aumenta en la serie isopentano -160 ?? C (113 K) n-pentano -129,8 ?? C (143 K) y neopentano -18 ?? C (255 K). Asimismo, en xilenos y tambi??n Diclorobencenos el punto de fusi??n aumenta en el orden meta, orto y luego p??rr. La piridina tiene una simetr??a m??s baja que el benceno , por tanto, su punto de fusi??n m??s bajo, pero el punto de fusi??n aumenta de nuevo con diazina y triazinas. Muchos compuestos de jaula como adamantano y cubane con alta simetr??a tienen puntos de fusi??n muy altas.
Un alto punto de fusi??n fruto de un elevado calor de fusi??n o un bajo entrop??a de fusi??n o una combinaci??n. En mol??culas altamente sim??tricas la fase cristalina est?? densamente poblada por muchas interacciones intermoleculares eficientes que ocasionen un cambio de entalp??a de fusi??n m??s alto en.

