
Energ??a libre de Gibbs
Acerca de este escuelas selecci??n Wikipedia
SOS Children produjo este sitio web para las escuelas, as?? como este sitio web video sobre ??frica . SOS Children ha cuidado de ni??os en ??frica durante cuarenta a??os. ??Puedes ayudar a su trabajo en ??frica ?
| La mec??nica estad??stica |
|---|
 |
|
Estad??sticas de part??culas
|
Conjuntos
|
|
Modelos
|
Potenciales
|
En termodin??mica , la energ??a libre de Gibbs ( IUPAC nombre recomendado: energ??a de Gibbs o funci??n de Gibbs) es un potencial termodin??mico que mide el "??til" o proceso de iniciar un trabajo que se puede obtener a partir de un isot??rmica, isob??rica sistema termodin??mico. T??cnicamente, la energ??a libre de Gibbs es la m??xima cantidad de trabajo no-expansi??n que se puede extraer de un sistema cerrado o este m??ximo s??lo puede alcanzarse de forma totalmente proceso reversible. Cuando un sistema pasa de un estado inicial bien definido a un estado final bien definido, el Gibbs energ??a libre? G es igual al trabajo intercambiado por el sistema con su entorno, menos el trabajo de las fuerzas de presi??n, durante una transformaci??n reversible del sistema del mismo estado inicial al mismo estado final.
Energ??a de Gibbs es tambi??n el potencial qu??mico que se minimiza cuando un sistema alcanza el equilibrio a la presi??n y temperatura constantes. Como tal, es un criterio de espontaneidad conveniente para procesos con presi??n y temperatura constante.
La energ??a libre de Gibbs, originalmente llamada energ??a disponible, se desarroll?? en la d??cada de 1870 por el f??sico matem??tico estadounidense Willard Gibbs . En 1873, en una nota al pie, Gibbs define lo que ??l llam?? la "energ??a disponible" de un cuerpo como tal:
| " | La mayor cantidad de trabajo mec??nico que se puede obtener a partir de una determinada cantidad de una determinada sustancia en un estado inicial dado, sin aumentar su total de volumen o permitir que el calor pase o de ??rganos externos, excepto los que al cierre de los procesos son dejado en su condici??n inicial. | " |
El estado inicial del cuerpo, de acuerdo con Gibbs, se supone que es tal que "el cuerpo puede hacerse pasar de ella a los estados de energ??a disipada por procesos reversibles ". En su 1876 obra maestra En el equilibrio de sustancias heterog??neas, un an??lisis gr??fico de sistemas qu??micos de varias fases, que dedica sus pensamientos sobre la energ??a libre de qu??micos en su totalidad.
Definiciones

La energ??a libre de Gibbs se define como:
que es el mismo que:
donde:
- U es la energ??a interna ( Unidad SI: Joule)
- p es presi??n (unidad SI: pascal)
- V es el volumen (Unidad SI: m 3)
- T es la temperatura (unidad SI: kelvin )
- S es la entrop??a (unidad SI: joule por kelvin)
- H es la entalp??a (unidad SI: julios)
La expresi??n para el cambio reversible infinitesimal en la energ??a libre de Gibbs, para una sistema abierto, sometido a la operaci??n de fuerzas externas X i, que causan los par??metros externos del sistema a i a cambio por una cantidad i da, viene dada por:
 donde:
donde:
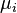 es el potencial qu??mico del -??simo i componente qu??mico. (Unidad SI: julios por part??culas o julios por mol)
es el potencial qu??mico del -??simo i componente qu??mico. (Unidad SI: julios por part??culas o julios por mol) 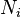 es el n??mero de part??culas (o n??mero de moles) que componen componente qu??mico el i-??simo.
es el n??mero de part??culas (o n??mero de moles) que componen componente qu??mico el i-??simo.
Esta es una forma de Gibbs ecuaci??n fundamental. En la expresi??n infinitesimal, el plazo, que incluye las cuentas potenciales qu??micos de los cambios en la energ??a libre de Gibbs resultantes de una afluencia o outflux de part??culas. En otras palabras, que tiene para una sistema abierto. Para sistema cerrado, este t??rmino se puede eliminar.
Cualquier n??mero de t??rminos adicionales se puede a??adir, dependiendo del sistema particular que est?? siendo considerado. Aparte de trabajo mec??nico , un sistema puede adem??s realizar numerosos otros tipos de trabajo. Por ejemplo, en la expresi??n infinitesimal, la energ??a de trabajo contr??ctil asociada con un sistema termodin??mico que es una fibra contr??ctil que acorta por una cantidad - dl bajo una fuerza f dar??a lugar a que se a??ade una fdl plazo. Si una cantidad de carga - de es adquirida por un sistema en una Ψ potencial el??ctrico, el trabajo el??ctrico asociado con esto es -Ψ de, que se incluye en la expresi??n infinitesimal. Otros t??rminos de trabajo se a??aden por los requisitos del sistema.
Cada cantidad en las ecuaciones anteriores se puede dividir por la cantidad de sustancia, medido en lunares, para formar molar energ??a libre de Gibbs. La energ??a libre de Gibbs es una de las funciones termodin??micas m??s importantes para la caracterizaci??n de un sistema. Es un factor en los resultados determinantes tales como la voltaje de una celda electroqu??mica, y el constante de equilibrio para una reacci??n reversible. En isot??rmica, los sistemas de isob??ricas, energ??a libre de Gibbs puede ser pensado como una cantidad "din??mica", en que es una medida representativa de los efectos de las fuerzas que compiten ent??lpicos y de conducci??n entr??pico que participan en un proceso termodin??mico.
La dependencia de la temperatura de la energ??a de Gibbs para un gas ideal est?? dada por la Gibbs-Helmholtz ecuaci??n y su dependencia de la presi??n viene dada por:
si el volumen es conocido en lugar de la presi??n entonces se convierte en:
o m??s convenientemente como su potencial qu??mico:
En los sistemas no ideales, fugacidad entra en juego.
Derivaci??n
La energ??a libre de Gibbs diferencial total en t??rminos de su variables naturales pueden derivarse a trav??s de Legendre transforma de la energ??a interna. Para un sistema de someterse a un proceso internamente reversible que se le permite intercambiar materia, calor y trabajo con su entorno, el diferencial de la energ??a interna se da desde la primera ley de la termodin??mica como
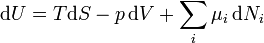 .
.
Porque 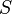 ,
, 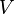 Y
Y  son las variables extensivas, Funci??n homog??nea teorema de Euler permite una f??cil integraci??n de
son las variables extensivas, Funci??n homog??nea teorema de Euler permite una f??cil integraci??n de 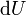 :
:
 .
.
La definici??n de 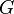 desde arriba es
desde arriba es
 .
.
Tomando la diferencial total, tenemos
 .
.
Sustituci??n 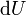 con el resultado de da la primera ley
con el resultado de da la primera ley

 .
.
Las variables naturales de 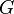 son entonces
son entonces 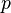 ,
, 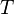 Y
Y  . Debido a que algunas de las variables naturales son intensivos,
. Debido a que algunas de las variables naturales son intensivos, 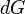 no pueden estar integradas utilizando integrales de Euler como es el caso con la energ??a interna. Sin embargo, simplemente sustituyendo el resultado de
no pueden estar integradas utilizando integrales de Euler como es el caso con la energ??a interna. Sin embargo, simplemente sustituyendo el resultado de 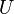 en la definici??n de
en la definici??n de 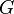 da una expresi??n est??ndar para G:
da una expresi??n est??ndar para G:

 .
.
Visi??n de conjunto
De una manera simple, con respecto a las STP sistemas reaccionar, un general regla de oro es:
| " | Cada sistema trata de alcanzar un m??nimo de energ??a libre. | " |
Por lo tanto, fuera de esta tendencia natural en general, una medida cuantitativa en cuanto a c??mo cerca o lejos una reacci??n potencial es de este m??nimo es cuando la energ??tica calculados del proceso indican que el cambio en la energ??a libre de Gibbs? G es negativo. Esencialmente, esto significa que tal reacci??n se ver?? favorecida y liberar energ??a. La energ??a liberada es igual a la cantidad m??xima de trabajo que puede ser realizado como resultado de la reacci??n qu??mica. A la inversa, si las condiciones indican un Delta G positiva, entonces la energ??a - en la forma de trabajo - tendr??a que ser a??adido al sistema de reacci??n para hacer la reacci??n ir.
Historia
La cantidad llamada "energ??a libre" es esencialmente un reemplazo m??s avanzada y precisa para el t??rmino anticuado " afinidad ", que fue utilizado por los qu??micos en a??os anteriores para describir la" fuerza "que caus?? reacciones qu??micas . La afinidad plazo, tal como se utiliza en relaci??n qu??mica, se remonta al menos a la hora de Alberto Magno en 1250.
De los 1998 libros de texto modernos Termodin??mica por el premio Nobel y profesor de ingenier??a qu??mica Ilya Prigogine encontramos:?? "A medida que el movimiento se explica por el concepto newtoniano de fuerza, los qu??micos quer??an un concepto similar de 'motor' para el cambio qu??mico ??Por qu?? ocurren las reacciones qu??micas, y por qu?? hacer que se detengan en ciertos puntos Qu??micos llamado el ' fuerza 'que caus?? afinidad reacciones qu??micas, pero carec??a de una definici??n clara ".
Durante todo el siglo 18, la opini??n dominante en cuanto al calor y la luz era la formulada por Isaac Newton , llamada la "hip??tesis de Newton", que afirmaron que la luz y el calor son formas de la materia atra??dos o repelidos por otras formas de la materia, con fuerzas an??logas a la gravitaci??n o la afinidad qu??mica.
En el siglo 19, el qu??mico franc??s Marcelino Berthelot y el qu??mico dan??s Julius Thomsen hab??a intentado cuantificar afinidad utilizando calores de reacci??n. En 1875, despu??s de la cuantificaci??n de los calores de reacci??n para un gran n??mero de compuestos, Berthelot propuso la " principio de trabajo m??ximo "en el que todos los cambios qu??micos que ocurren sin la intervenci??n de la energ??a exterior tienden hacia la producci??n de cuerpos o de un sistema de cuerpos que liberan calor .
Adem??s de esto, en 1780 Antoine Lavoisier y Pierre-Simon Laplace sentaron las bases de termoqu??mica mostrando que el calor dada a cabo en una reacci??n es igual al calor absorbido en la reacci??n inversa. Tambi??n investigaron la calor espec??fico y calor latente de un n??mero de sustancias, y cantidades de calor propuestos en la combusti??n. Del mismo modo, en 1840 el qu??mico suizo Germain Hess formul?? el principio de que la evoluci??n de calor en una reacci??n es la misma si el proceso se realiza en un solo paso o en un n??mero de etapas. Esto se conoce como La ley de Hess. Con el advenimiento de la teor??a mec??nica del calor en el siglo 19, la ley de Hess lleg?? a ser visto como una consecuencia de la ley de conservacion de energia.
Sobre la base de estas y otras ideas, Berthelot y Thomsen, as?? como otros, considerado el calor emitido en la formaci??n de un compuesto como una medida de la afinidad, o el trabajo realizado por las fuerzas qu??micas. Este punto de vista, sin embargo, no era del todo correcto. En 1847, el f??sico Ingl??s James Joule demostr?? que pod??a elevar la temperatura del agua girando una rueda de paletas en ella, mostrando de esta manera que el calor y trabajo mec??nico fueron equivalentes o proporcionales entre s??, es decir, aproximadamente,  . Esta declaraci??n vino a ser conocido como el equivalente mec??nico del calor y era una forma precursora de la primera ley de la termodin??mica .
. Esta declaraci??n vino a ser conocido como el equivalente mec??nico del calor y era una forma precursora de la primera ley de la termodin??mica .
En 1865 el f??sico alem??n Rudolf Clausius hab??a demostrado que este principio de equivalencia necesaria enmienda. Es decir, uno puede utilizar el calor derivado de una reacci??n de combusti??n en un horno de carb??n para hervir el agua, y utilizar este calor para evaporar el vapor, y luego usar la energ??a de alta presi??n mejorada del vapor vaporizado para empujar un pist??n. As??, podr??amos razonar ingenuamente que uno puede convertir completamente el calor de combusti??n inicial de la reacci??n qu??mica en el trabajo de empujar el pist??n. Clausius mostr??, sin embargo, que tenemos que tener en cuenta la labor que las mol??culas del cuerpo de trabajo, es decir, las mol??culas de agua en el cilindro, hacer el uno del otro a medida que pasan o transformar de un paso o estado de la ciclo del motor a la siguiente, por ejemplo, a partir de (P1, V1) a (P2, V2). Clausius originalmente llam?? a esto el "contenido transformaci??n" del cuerpo, y m??s tarde cambi?? el nombre a la entrop??a . Por lo tanto, el calor usado para transformar el cuerpo de trabajo de las mol??culas de un estado al siguiente no se puede utilizar para hacer el trabajo externo, por ejemplo, para empujar el pist??n. Clausius defini?? este calor transformaci??n como dQ = TdS.
En 1873, Willard Gibbs public?? un m??todo de representaci??n geom??trica de las propiedades termodin??micas de las sustancias por medio de superficies en la que introdujo el esquema preliminar de los principios de su nueva ecuaci??n capaces de predecir o estimar las tendencias de varios procesos naturales que sobrevendr?? cuando los cuerpos o sistemas se ponen en contacto. Mediante el estudio de las interacciones de sustancias homog??neas en contacto, es decir, ??rganos, siendo en la composici??n de parte s??lida, parte l??quida y parte vapor, y mediante el uso de un tridimensional volumen - entrop??a - gr??fico interior de la energ??a, Gibbs fue capaz de determinar tres estados de equilibrio, es decir, "necesariamente estable", "neutral", y "inestable", y si o no los cambios se producir??n. En 1876, Gibbs construido en este marco mediante la introducci??n del concepto de potencial qu??mico de manera que tome en cuenta las reacciones qu??micas y los estados de los ??rganos que son qu??micamente diferentes entre s??. En sus propias palabras, para resumir sus resultados en 1873, Gibbs dice:
En esta descripci??n, tal como se utiliza por Gibbs, ε se refiere a la energ??a interna del cuerpo, η se refiere a la entrop??a del cuerpo, y ν es el volumen del cuerpo.
Por lo tanto, en 1882, despu??s de la introducci??n de estos argumentos por Clausius y Gibbs, el cient??fico alem??n Hermann von Helmholtz declar??, en oposici??n a Berthelot y Thomas 'hip??tesis de que la afinidad qu??mica es una medida del calor de reacci??n de la reacci??n qu??mica como basado en el principio de m??xima de trabajo, que la afinidad no es el calor emitido en la formaci??n de un compuesto sino que es la mayor cantidad de trabajo que se puede obtener cuando la reacci??n se lleva a cabo de una manera reversible, por ejemplo, el trabajo el??ctrico en una c??lula reversible. El trabajo m??xima es as?? considerada como la disminuci??n de los libres, o disponibles, la energ??a del sistema (energ??a libre de Gibbs G a T = constante, P = constante o energ??a libre de Helmholtz F a T = constante, V = constante), mientras que el calor emitido a cabo por lo general es una medida de la disminuci??n de la energ??a total del sistema ( Energ??a interna). Por lo tanto, G o F es la cantidad de energ??a "libre" para el trabajo en las condiciones dadas.
Hasta este punto, la vista general hab??a sido tal que: "todas las reacciones qu??micas conducen al sistema a un estado de equilibrio en el que las afinidades de las reacciones desaparecen". Durante los pr??ximos 60 a??os, la afinidad t??rmino lleg?? a ser reemplazado por la libre expresi??n de la energ??a. Seg??n el historiador qu??mica Henry Leicester, el influyente libro de texto de 1923 Termodin??mica y la energ??a libre de las reacciones qu??micas por Gilbert N. Lewis y Merle Randall llev?? a la sustituci??n del t??rmino "afinidad" por el t??rmino "energ??a libre" en gran parte del mundo de habla Ingl??s.
??Qu?? significa el t??rmino "libre"?
En los siglos 18 y 19, la teor??a del calor, es decir, que el calor es una forma de energ??a que tiene relaci??n con movimiento vibratorio, empezaba a suplantar tanto la teor??a cal??rica, es decir, que el calor es un fluido, y el cuatro teor??a elemento en el que el calor era el m??s ligero de los cuatro elementos. Muchos libros de texto y art??culos de ense??anza durante estos siglos presentan estas teor??as al lado del otro. Del mismo modo, durante estos a??os, el calor empezaba a distinguirse en diferentes categor??as de clasificaci??n, como "calor libre", "producci??n combinada de calor", "calor radiante", calor especifico, capacidad calor??fica, "calor absoluto", "cal??rico latente", "libre" o "perceptible" cal??rica (calorique sensible), entre otros.
En 1780, por ejemplo, Laplace y Lavoisier declararon: "En general, se puede cambiar la primera hip??tesis en el segundo, cambiando las palabras" sin calor combinada de calor, y el calor liberado "en" . vis viva, p??rdida de fuerza viva, y aumento de la fuerza viva '"De esta manera, la masa total de calor??as en un cuerpo, llamado calor absoluta, fue considerada como una mezcla de dos componentes; el cal??rico libre o perceptible podr??a afectar un term??metro mientras que el otro componente, el cal??rico latente, no pod??a. El uso de las palabras "calor latente" implicaba una similitud con el calor latente en el sentido m??s habitual; se consideraba ligado qu??micamente a las mol??culas del cuerpo. En el adiab??tico compresi??n de un gas el calor absoluta se mantuvo constante por el aumento observado de la temperatura, lo que indica que algunos cal??rico latente se hab??a convertido en "libre" o perceptible.
Durante el siglo 19, el concepto de calor??as perceptible o libre comenz?? a ser conocido como "el calor libre" o el calor liberado. En 1824, por ejemplo, el f??sico franc??s Sadi Carnot, en sus famosas "Reflexiones sobre la potencia motriz del fuego", habla de cantidades de calor 'absorbidos o puestos en libertad' en diferentes transformaciones. En 1882, el f??sico y fisi??logo alem??n Hermann von Helmholtz acu???? la frase 'energ??a libre' para la expresi??n E - TS, en la que el cambio de F (o G) determina la cantidad de energ??a "libre" para el trabajo en las condiciones dadas.
As??, en el uso tradicional, el t??rmino "libre" se adjunt?? a energ??a libre de Gibbs, es decir, para sistemas a presi??n y temperatura constante, o para energ??a libre de Helmholtz, es decir, para sistemas en volumen y temperatura constante, para significar "disponible en la forma de trabajo ??til ". Con referencia a la energ??a libre de Gibbs, a??adimos la calificaci??n que es la energ??a libre para el trabajo no volumen.
Un creciente n??mero de libros y art??culos de revistas no incluyen el archivo adjunto "libre", en referencia a G como simplemente energ??a de Gibbs (y lo mismo para el La energ??a de Helmholtz). Este es el resultado de un 1,988 Reuni??n de la IUPAC para establecer terminolog??as unificadas para la comunidad cient??fica internacional, en la que supuestamente fue desterrado el adjetivo "libre". Esta norma, sin embargo, a??n no se ha adoptado universalmente, y muchos art??culos y libros publicados todav??a incluyen el descriptivo "libre".
La energ??a libre de las reacciones
Para derivar la ecuaci??n de la energ??a libre de Gibbs para un aislado sistema, sea S tot ser la entrop??a total del sistema aislado, es decir, un sistema que no puede intercambiar calor o masa con su entorno. De acuerdo con la segunda ley de la termodin??mica :
y si  entonces el proceso es reversible. La transferencia de calor
entonces el proceso es reversible. La transferencia de calor  desaparece para un sistema adiab??tico. Cualquier proceso adiab??tico que tambi??n es reversible se llama isentr??pico
desaparece para un sistema adiab??tico. Cualquier proceso adiab??tico que tambi??n es reversible se llama isentr??pico  proceso.
proceso.
Ahora considere sistemas diab??ticos, teniendo entrop??a S interna int. Dicho sistema est?? conectado t??rmicamente con su entorno, que tienen entrop??a S ext. La forma de la entrop??a de la segunda ley no se aplica directamente al sistema diab??tico, s??lo se aplica al sistema cerrado formado por el sistema y su entorno. Por lo tanto un proceso es posible si
 .
.
Vamos a tratar de expresar el lado izquierdo de esta ecuaci??n enteramente en t??rminos de las funciones del Estado? S ext se define como.:
Temperatura T es la misma para dos sistemas en equilibrio t??rmico. Por el ley cero de la termodin??mica, si un sistema est?? en equilibrio t??rmico con un segundo y un tercer sistema, estos dos ??ltimos est??n en equilibrio tambi??n. Tambi??n,  es el calor transferido al sistema, por lo
es el calor transferido al sistema, por lo  es el calor transferido a los alrededores, y -ΔQ / T es la entrop??a ganado por los alrededores. Ahora tenemos:
es el calor transferido a los alrededores, y -ΔQ / T es la entrop??a ganado por los alrededores. Ahora tenemos:
Multiplique ambos lados por T:
ΔQ es el calor transferido al sistema; si el proceso se supone que es ahora isob??rica, entonces ΔQ p =? H:
? H es el cambio de entalp??a de la reacci??n (para una reacci??n qu??mica a presi??n constante y temperatura). Entonces
para un posible proceso. Deje que el cambio Δ G en energ??a libre de Gibbs se define como
 (Eq.1)
(Eq.1)
Observe que no se define en t??rminos de las funciones estatales externos, como Δ S ext o Δ S tot. Luego la segunda ley se convierte, que tambi??n nos habla de la espontaneidad de la reacci??n:
 reacci??n favorecida (espont??nea)
reacci??n favorecida (espont??nea) 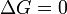 Ni el delantero ni la reacci??n inversa prevalece ( Equilibrium )
Ni el delantero ni la reacci??n inversa prevalece ( Equilibrium )  reacci??n desfavorecida (no espont??nea)
reacci??n desfavorecida (no espont??nea)
Energ??a libre de Gibbs G en s?? se define como
 (Ecuaci??n 2)
(Ecuaci??n 2)
Pero Tenga en cuenta que para obtener la ecuaci??n (2) de la ecuaci??n (1) debemos suponer que T es constante. Por lo tanto, energ??a libre de Gibbs es m??s ??til para los procesos termoqu??micos a temperatura y presi??n constantes: tanto isot??rmico y isob??rica. Tales procesos no se mueven en un P - T diagrama, tales como cambio de fase de una sustancia pura, que tiene lugar a la presi??n de saturaci??n y la temperatura. Las reacciones qu??micas, sin embargo, no sufren cambios en potencial qu??mico, que es una funci??n de estado. Por lo tanto, los procesos termodin??micos no se limitan a las dos dimensiones P - diagrama V. Hay una tercera dimensi??n para n, la cantidad de gas. Naturalmente para el estudio de los productos qu??micos explosivos, los procesos no son necesariamente isot??rmica y isob??rica. Para estos estudios, Se utiliza la energ??a libre de Helmholtz.
Si un sistema cerrado (Δ Q = 0) es a presi??n constante (Δ Δ Q = H), entonces
Por lo tanto la energ??a libre de Gibbs de un sistema cerrado es:
y si  a continuaci??n, esto implica que
a continuaci??n, esto implica que  , De vuelta al punto de partida la derivaci??n de Δ G.
, De vuelta al punto de partida la derivaci??n de Δ G.
Identidades ??tiles
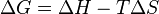 para temperatura constante
para temperatura constante 


y reordenando da
que relaciona el potencial el??ctrico de una reacci??n con el coeficiente de equilibrio para esta reacci??n.
donde
Δ G = cambio en la energ??a libre de Gibbs, Δ H = cambio de entalp??a , T = absoluto de temperatura , Δ S = cambio en la entrop??a , R = constante de los gases, ln = logaritmo natural , K = constante de equilibrio, Q = cociente de reacci??n, n = n??mero de electrones por producto en moles, F = Constante de Faraday ( culombios por mol), y Δ E = potencial el??ctrico de la reacci??n. Por otra parte, tambi??n tenemos:
que relaciona la constante de equilibrio con la energ??a libre de Gibbs.
Cambio est??ndar de formaci??n
La energ??a libre de Gibbs est??ndar de formaci??n de un compuesto es el cambio de energ??a libre de Gibbs que acompa??a la formaci??n de 1 mol de dicha sustancia a partir de sus elementos componentes, en su estados est??ndar (la forma m??s estable del elemento a 25 grados Celsius y 100 kilopascales). Su s??mbolo es Δ G f S.
Todos los elementos en sus estados est??ndar ( ox??geno gas, grafito, etc.) tienen 0 est??ndar Gibbs cambio de energ??a libre de formaci??n, ya que no hay cambio en cuesti??n.
- Δ G = Δ G ˚ + RT ln Q
En el equilibrio, Δ G = 0 y Q = K por lo que la ecuaci??n se convierte en Δ G ˚ = - RT ln K
Tabla de sustancias seleccionadas
| Sustancia | Estado | Δ G ˚ ( cal / mol) |
|---|---|---|
| NH 3 | g | -3.976 |
| H 2 O | lq | -56.69 |
| H 2 O | g | -54.64 |
| CO 2 | g | -94.26 |
| Colorado | g | -32.81 |
| CH 4 | g | -12.14 |
| C 2 H 6 | g | -7.86 |
| C 3 H 8 | g | -5.614 |
| C 8 H 18 | g | 4.14 |
| C 10 H 22 | g | 8.23 |



















