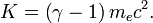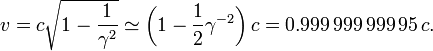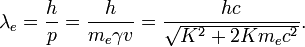Electrón
Antecedentes de las escuelas de Wikipedia
Esta selección wikipedia ha sido elegido por los voluntarios que ayudan Infantil SOS de Wikipedia para esta Selección Wikipedia para las escuelas. Con Infantil SOS se puede elegir a apadrinar a los niños en más de cien países
 Estimaciones teóricas de la densidad electrónica para los primeros orbitales de electrones de hidrógeno átomo se muestran como secciones transversales con densidad de probabilidad con código de color | |
| Composición | Partícula elemental |
|---|---|
| Estadística | Fermión |
| Generación | Primero |
| Interacciones | La gravedad , electromagnética , Débil |
| Símbolo | e -, β - |
| Antipartícula | Positrón |
| Teorizado | G. Johnstone Stoney (1874) |
| Descubierto | JJ Thomson (1897) |
| Masa | 9,109 382 15 (45) × 10 -31 kg 5,485 799 09 (27) × 10 -4 u 1 / 1822.888 4843 (11) u |
| Carga eléctrica | -1.602 176 487 (40) × 10 -19 C |
| Vuelta | ½ |
El electrón es una fundamental partícula subatómica que lleva un negativo carga eléctrica . Es un spin ½ leptón que participa en las interacciones electromagnéticas , y su masa es de aproximadamente 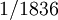 de la del protón . Junto con los núcleos atómicos , que consisten en protones y neutrones , los electrones forman los átomos. Su interacción con núcleos adyacentes es la principal causa de los enlaces químicos .
de la del protón . Junto con los núcleos atómicos , que consisten en protones y neutrones , los electrones forman los átomos. Su interacción con núcleos adyacentes es la principal causa de los enlaces químicos .
Historia
El nombre de electrones viene de la palabra griega para ámbar , ήλεκτρον. Este material juega un papel esencial en el descubrimiento de los fenómenos eléctricos. Los antiguos griegos sabían, por ejemplo, que frotar un trozo de ámbar con pieles dejó una carga eléctrica en su superficie, que podría crear una chispa cuando se pone cerca de un objeto conectado a tierra. Para saber más sobre la historia del término de electricidad, consulte Historia de la electricidad.
El electrón como unidad de carga en electroquímica se postuló por G. Johnstone Stoney en 1874, que también acuñó el término electrónico en 1894.
En este trabajo se realizó una estimación de la cantidad real de esta unidad fundamental más notable de la electricidad, por lo que he puesto aventurado sugerir el nombre de electrones.- Stoney, George Johnstone (octubre de 1894). "De los" electrones ", o Atom de Electricidad". Philosophical Revista 38 (5): 418-420. http://dbhs.wvusd.k12.ca.us/webdocs/Chem-History/Stoney-1894.html.
Durante finales de 1890 una serie de físicos postuló que la electricidad podría ser concebida como hechas de unidades discretas, que fueron dadas una variedad de nombres, pero la realidad de estas unidades no se había confirmado de una manera convincente.
El descubrimiento de que el electrón era una partícula subatómica se hizo en 1897 por JJ Thomson en el Laboratorio Cavendish en la Universidad de Cambridge , mientras estudiaba tubos de rayos catódicos. Un tubo de rayos catódicos es un cilindro de vidrio sellado en la que dos electrodos están separados por un vacío. Cuando se aplica un voltaje a través de los electrodos, los rayos catódicos se generan, haciendo que el tubo brille. A través de la experimentación, Thomson descubrió que la carga negativa no podía ser separada de los rayos (por la aplicación de magnetismo), y que los rayos puede ser desviado por un campo eléctrico. Llegó a la conclusión de que estos rayos, en lugar de ser olas, se compone de partículas con carga negativa que llamó "corpúsculos". Midió su relación masa-carga y nos pareció que es más de mil veces más pequeño que el de un ion de hidrógeno, lo que sugiere que eran o muy altamente cargadas o muy pequeña en masa. Experimentos posteriores de otros científicos confirmaron la última conclusión. Su relación de masa a carga también fue independiente de la elección del material del cátodo y el gas originalmente en el tubo de vacío. Esto llevó a la conclusión de Thomson que eran universales entre todos los materiales.
La carga del electrón se midió cuidadosamente por RA Millikan en su experimento de 1909 la gota de aceite.
La ley periódica establece que las propiedades químicas de los elementos en gran parte se repiten periódicamente y es la base de la tabla periódica de elementos. La ley en sí fue explicada inicialmente por el masa atómica del elemento. Sin embargo, ya que había anomalías en la tabla periódica, se hicieron esfuerzos para encontrar una mejor explicación para ello. En 1913, Henry Moseley introdujo el concepto de número atómico y explicó la ley periódica en cuanto al número de protones cada elemento tiene. En el mismo año, Niels Bohr mostró que los electrones son la base real de la tabla. En 1916, Gilbert Newton Lewis explicó la unión química de elementos por interacciones electrónicas.
Clasificación
El electrón está en la clase de partículas subatómicas llamadas leptones, que se cree que son partículas fundamentales.
Como con todas las partículas, los electrones pueden actuar también como ondas. Esto se llama la dualidad onda-partícula , también conocido por el término complementariedad acuñado por Niels Bohr , y se puede demostrar utilizando el experimento de la doble rendija.
La antipartícula de un electrón es el positrones, que tiene carga positiva en lugar de negativa. El descubridor del positrón, Carl D. Anderson, propuso llamar electrones negatrones estándar, y el uso de electrones como un término genérico para describir tanto las variantes de carga positiva y negativa. Este uso se encuentra ocasionalmente en la actualidad.
Propiedades y comportamiento
Los electrones tienen una carga eléctrica de -1,6021765 × 10 -19 Coulomb, una masa de 9,11 × 10 -31 kg en base a mediciones de carga / masa y un relativista masa en reposo de alrededor de 0.511 MeV / c ². La masa del electrón es aproximadamente 1/1836 de la masa del protón . El símbolo de electrones común es e -. Electron significa vida es 4.6x10> 26 años (ver Desintegración de partículas).
De acuerdo con la mecánica cuántica , los electrones pueden ser representados por funciones de onda, de las cuales un calculan probabilística densidad de electrones puede ser determinada. La orbital de cada electrón en un átomo puede ser descrita por una función de onda. Basado en el Principio de incertidumbre de Heisenberg, el exacto momento y la posición del electrón real no se puede determinar de forma simultánea. Esta es una limitación que, en este caso, simplemente afirma que la mayor exactitud sabemos la posición de una partícula, menos precisión que podemos conocer su impulso, y viceversa.
El electrón tiene espín ½ y es una fermión (sigue Fermi-Dirac estadísticas). Además de su momento angular intrínseco, un electrón tiene una intrínseca momento magnético a lo largo de su eje de rotación.
Los electrones en un átomo están obligados a ese átomo, mientras que los electrones se mueven libremente en el vacío, el espacio o determinados medios de comunicación son los electrones libres que pueden ser enfocados en una rayo de electrones. Cuando los electrones libres se mueven, hay una flujo neto de carga, y este flujo se denomina corriente eléctrica. La velocidad de deriva de los electrones en los alambres de metal está en el orden de milímetros por segundo. Sin embargo, la velocidad a la que una corriente en un punto en un cable provoca una corriente en otras partes del alambre, la velocidad de propagación, es típicamente 75% de la velocidad de la luz.
En algunos superconductores , pares de electrones se mueven como Pares de Cooper en la que su movimiento está acoplado a la materia cercana a través de vibraciones de la red llamados fonones. La distancia de separación entre los pares de Cooper es de aproximadamente 100 nm. (Rohlf, JW)
Un cuerpo tiene una carga eléctrica cuando dicho organismo tiene más o menos electrones que son necesarios para equilibrar la carga positiva de los núcleos. Cuando hay un exceso de electrones, se dice que el objeto a ser cargado negativamente. Cuando hay menos electrones que protones , se dice que el objeto a ser cargado positivamente. Cuando el número de electrones y el número de protones son iguales, sus cargas se anulan entre sí y el objeto se dice que es eléctricamente neutro. La cuerpo macroscópico puede desarrollar una carga eléctrica a través de frotamiento, por el fenómeno de triboelectricidad.
Cuando los electrones y positrones chocan, aniquilarse entre sí y producir pares de alta energía de fotones y otras partículas. Por otra parte, los fotones de alta energía pueden transformar en un electrón y un positrón por un proceso llamado la producción de pares, pero sólo en la presencia de una partícula cargada cerca, tal como un núcleo.
El electrón se describe actualmente como una partícula fundamental o elemental. No tiene ninguna conocida subestructura. Por lo tanto, por conveniencia, generalmente se define o se supone que es un punto-como matemática carga puntual, sin extensión espacial. Sin embargo, cuando una partícula de prueba se ve obligado a acercarse a un electrón, medimos los cambios en sus propiedades ( carga y masa ). Este efecto es común a todas las partículas elementales. La teoría actual sugiere que este efecto es debido a la influencia de fluctuaciones de vacío en su espacio local, de modo que las propiedades medidas a partir de una distancia significativa se considera que la suma de las propiedades desnudos y los efectos del vacío (véase la renormalización ).
La radio clásico del electrón es 2.8179 x 10 -15 m. Este es el radio que se infiere de la carga eléctrica del electrón, mediante el uso de la teoría clásica de electrodinámica solo, haciendo caso omiso de la mecánica cuántica . Clásico electrodinámica ( Maxwell 's electrodinámica) es el concepto más antiguo que se utiliza ampliamente para las aplicaciones prácticas de la electricidad, ingeniería eléctrica, física de semiconductores y electromagnetismo. La electrodinámica cuántica, por el contrario, es útil para aplicaciones que implican la física de partículas moderna y algunos aspectos de la óptica, láser y la física cuántica.
Basado en la teoría actual, la velocidad de un electrón puede acercarse, pero nunca llegar a, c (la velocidad de la luz en el vacío). Esta limitación se atribuye a la teoría de Einstein de la relatividad especial , que define la velocidad de la luz como una constante dentro de todos sistemas inerciales. Sin embargo, cuando relativista electrones se inyectan en una medio dieléctrico tal como agua, donde la velocidad local de la luz es significativamente menor que c, los electrones (temporalmente) viajar más rápido que la luz en el medio. A medida que interactúan con el medio, que generan una luz azulada débil llamada Radiación de Cherenkov.
Los efectos de la relatividad especial se basan en una cantidad conocida como γ o la Factor de Lorentz. γ es una función de v, la velocidad de coordenadas de la partícula. Se define como:
La energía cinética necesaria para acelerar un electrón es:
Por ejemplo, el Stanford acelerador lineal puede acelerar un electrón a aproximadamente 51 GeV . Esto da una gamma de 100 000, ya que la masa de un electrón es 0,51 MeV / c ² (el impulso relativista de este electrón es 100.000 veces el impulso clásica de un electrón a la misma velocidad). Resolviendo la ecuación anterior para la velocidad del electrón (y usando una aproximación para gran γ) da:
La de Broglie longitud de onda de una partícula es λ = h / p, donde h es P constante de Planck es el impulso. A bajas (por ejemplo, de fotoelectrones) energías esto determina el tamaño de los átomos, y a altas (por ejemplo, microscopio electrónico) energías esto hace que el Bragg ángulos para difracción de electrones (co-descubierto por JJ Thomson hijo 's GP Thomson) muy por debajo de un grado. Desde el momento es la masa por adecuada velocidad w = γv, tenemos
Para el 51 GeV de electrones anteriormente, adecuada velocidad es de aproximadamente? C, haciendo que la longitud de onda de los electrones lo suficientemente pequeños para explorar estructuras bien por debajo del tamaño de un núcleo atómico.
Visualización
Las primeras imágenes de vídeo de un electrón fueron capturados por un equipo de la Universidad de Lund en Suecia en febrero de 2008. Para capturar este evento, los científicos utilizaron destellos de luz extremadamente cortos. Para producir esta luz, la tecnología recientemente desarrollada para la generación de pulsos cortos de intensa luz láser, denominados pulsos de attosegundos, permitió al equipo de la Facultad de la Universidad de Ingeniería para capturar el movimiento del electrón por primera vez.
"Se tarda unos 150 attosegundos para un electrón para rodear el núcleo de un átomo. Un attosegundos está relacionado con un segundo como segunda se relaciona con la edad del universo", explicó Johan Mauritsson, profesor asistente en la física atómica en la Facultad de Ingeniería de la Universidad de Lund.
Video está disponible aquí:
En la práctica
En el universo
Los científicos creen que el número de electrones existentes en el conocido universo es de al menos 10 79. Este número asciende a una densidad media de alrededor de un electrón por metro cúbico de espacio. Los astrónomos han estimado que el 90% de la masa de los átomos en el universo es hidrógeno , que está hecho de un electrón y un protón.
En la industria
Los haces de electrones se utilizan en la soldadura , litografía, microscopios electrónicos de barrido y microscopios electrónicos de transmisión. LEED y RHEED son técnicas superficie de formación de imágenes que utilizan electrones.
Los electrones también están en el corazón de tubos de rayos catódicos, que se utilizan ampliamente como dispositivos de visualización de instrumentos de laboratorio, monitores de ordenador y aparatos de televisión. En un tubo fotomultiplicador, un fotón golpea el fotocátodo, iniciando una avalancha de electrones que produce una corriente detectable.
En el laboratorio
La relación única de alta carga a masa de electrones significa que interactúan fuertemente con los átomos, y son fáciles de acelerar y centrar con campos eléctricos y magnéticos. De ahí que algunos de hoy transmisión de aberración corregida microscopios electrónicos utilizan electrones 300keV con velocidades superiores a la velocidad de la luz en el agua, longitudes de onda inferiores 2 picómetros, transversales de coherencia anchos de más de un nanómetro y longitudinales-coherencia anchos 100 veces en las que, a la imagen de dispersión atómica-núcleos individual ( HAADF) así como la interferencia contraste de sólido-espécimen de salida de la superficie DeBroglie fase ( HRTEM) con lateral puntuales resoluciones abajo para 60 picómetros. Se necesitan aumentos que se aproximan 100 millones para hacer que el detalle de la imagen resultante cómodamente visible para el ojo desnudo.
Los efectos cuánticos de los electrones también se utilizan en el Microscopio de efecto túnel, para estudiar las características de las superficies sólidas con lateral resolución a escala atómica (alrededor de 200 picómetros) y-resoluciones verticales mucho mejores que eso. Además de la fuerte dependencia de túnel cuántico en la separación punta-muestra, la sensibilidad vertical se deriva de la precisión de control electrónico de la separación es posible con un escáner piezoeléctrico.
En la medicina
En terapia de radiación, haces de electrones se utilizan para el tratamiento de tumores superficiales.
En teoría
En el modelo de Dirac, un electrón se define como un punto matemático, una partícula "desnudo" puntual, acusado rodeado de un mar de pares de interacción de virtuales partículas y antipartículas. Estos proporcionan una corrección de poco más de 0.1% sobre el valor predicho de la década de los electrones relación giromagnética de exactamente 2 (según lo predicho por el modelo de una sola partícula de Dirac). El acuerdo con extraordinaria precisión de esta predicción con el valor determinado experimentalmente es visto como uno de los grandes logros de la física moderna.
En el Modelo Estándar de la física de partículas , el electrón es la primera generación cargada leptones. Se forma una débil doblete isospin con la neutrino electrónico; estas dos partículas interactúan entre sí tanto a través de la corriente cargada y neutral interacción débil. El electrón es muy similar a los dos más partículas masivas de generaciones superiores, el muón y el leptón tau, que son idénticos a cargo, centrifugado, y interacción pero difieren en masa.
La antimateria contraparte del electrón es la positrones. El positrón tiene la misma cantidad de carga eléctrica que el electrón, excepto que la carga es positiva. Tiene la misma masa y espín que el electrón. Cuando un electrón y un positrón se encuentran, se puede aniquilarse entre sí, dando lugar a dos fotones de rayos gamma emitidos en aproximadamente 180 ° entre sí. Si el electrón y el positrón tenían impulso insignificante, cada rayo gamma tendrá una energía de 0.511 MeV. Ver también Electrón-positrón aniquilación.
Los electrones son un elemento clave en el electromagnetismo , una teoría que es preciso para sistemas macroscópicos, como para la modelización clásica de los sistemas microscópicos.
| |||||