Paladio
Antecedentes de las escuelas de Wikipedia
Organizar una selección Wikipedia para las escuelas en el mundo en desarrollo sin acceso a Internet era una iniciativa de SOS Children. Haga clic aquí para obtener información sobre el apadrinamiento de niños.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Informacion General | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nombre , símbolo, número | paladio, Pd, 46 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Categoría Elemento | metales de transición | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo, Período, Bloque | 10, 5, d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia | metálico blanco plateado  | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Peso atómico estándar | 106.42 (1) g · mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuración electrónica | [ Kr ] 4d 10 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Los electrones por cáscara | 2, 8, 18, 18, 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades físicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fase | sólido | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidad (cerca rt) | 12.023 g · cm -3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Líquido densidad en mp | 10,38 g · cm -3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de fusion | 1828.05 K (1554.9 ° C, 2830.82 ° F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de ebullicion | 3236 K (2963 ° C, 5365 ° F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor de fusión | 16.74 kJ · mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
El calor de vaporización 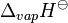 | 362 kJ · mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor específico | (25 ° C) 25.98 J · mol -1 · K -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades atómicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estructura cristalina | cara cúbica centrada | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estados de oxidación | 2, 4 (Levemente óxido básico) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegatividad | 2,20 (escala de Pauling) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energías de ionización | Primero: 804,4 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Segundo: 1870 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tercero: 3177 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio atómico | 140 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio atómico (calc.) | 169 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio covalente | 131 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals radio | 163 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscelánea | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ordenamiento magnético | sin datos | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| La resistividad eléctrica | (20 ° C) 105.4 n Ω · m | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductividad térmica | (300 K) 71.8 W · m -1 · K -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Expansión térmica | (25 ° C) 11,8 m · m -1 · K -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocidad del sonido (varilla delgada) | (20 ° C) 3070 m / s | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| El módulo de Young | 121 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Módulo de corte | 44 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Módulo de volumen | 180 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Relación de Poisson | 0.39 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureza de Mohs | 4.75 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureza Vickers | 461 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureza Brinell | 37,3 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Número de registro del CAS | 7440-05-3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| La mayoría de los isótopos estables | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Referencias | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Palladium (pronunciado \ pe-'La-de-em \) es una rara y brillante metal plateado-blanco que fue descubierto en 1803 por William Hyde Wollaston, quien lo nombró paladio después del asteroide Pallas, que a su vez, fue nombrado por la diosa griega de la sabiduría. El símbolo para el paladio es Pd, y su número atómico es 46. Palladium, junto con platino , rodio , rutenio , iridio y osmio formar un grupo de elementos referido como el metales del grupo del platino (PGM). PGMs comparten propiedades químicas similares, pero el paladio es único en que tiene el punto de fusión más bajo y es el menos denso de estos metales preciosos. Increíblemente, cuando el paladio se encuentra a temperatura ambiente y presión atmosférica, que puede absorber hasta 900 veces su propio volumen de hidrógeno , que hacen que el paladio un medio de almacenamiento eficiente y seguro para el hidrógeno y de hidrógeno isótopos. Palladium también se deslustre resistente al calor, eléctricamente estable y resistente a la erosión química, así como intenso.
Las propiedades únicas de paladio y otros MGP hacen necesario su uso generalizado como uno de cada cuatro de los productos fabricados hoy tampoco contienen PGM o habían MGP jugar un papel clave durante el proceso de fabricación. Más de la mitad de la oferta de paladio y su metal hermana platino entra en convertidores catalíticos, que convierten hasta un 90% de los gases nocivos de los escapes de automóviles ( hidrocarburos, monóxido de carbono y óxido de nitrógeno) en sustancias menos nocivas ( nitrógeno , dióxido de carbono y vapor de agua). Cualidades de metales preciosos de Palladium y el aspecto generan un consumo significativo en el lujo de la joyería mercado. El paladio se encuentra en muchos productos electrónicos, incluyendo computadoras , teléfonos móviles , condensadores cerámicos multicapa, chapado componente, contactos eléctricos de baja tensión, y / OLED / LCD SED televisores . Palladium también se utiliza en odontología, medicina , purificación de hidrógeno, aplicaciones químicas, tratamiento de las aguas subterráneas, y que está jugando un papel clave en la tecnología utilizada para las células de combustible, que se combinan el hidrógeno y el oxígeno para producir electricidad, calor y agua, prácticamente sin contaminación .
Depósitos de mineral de paladio y otros MGP son raros, y los más extensos yacimientos se han encontrado en el cinturón de la norite Complejo Bushveld ígnea en el Transvaal en Sudáfrica , el Complejo Stillwater en Montana, EE.UU. , el Sudbury Distrito de Ontario Canadá y la Complejo Norilsk en Rusia . Además de la minería , el paladio también se recupera a través de reciclaje ; la mayor parte de los cuales proviene de los convertidores catalíticos desguazados. Las numerosas aplicaciones y fuentes de suministros limitados de resultado paladio en paladio dibujo considerable intereses de inversión.
Historia
Palladium era descubierto por William Hyde Wollaston en 1803 . Este elemento fue nombrado por Wollaston en 1804 después de que el asteroide Pallas, descubierto dos años antes.
Wollaston encontró paladio en mineral de platino crudo de América del Sur disolviendo el mineral en aqua regia, neutralizando la solución con hidróxido de sodio , y la precipitación de platino como cloroplatinato amonio con de cloruro de amonio. Agregó cianuro mercúrico para formar el compuesto cianuro de paladio, que se calentó para extraer metal de paladio.
Cloruro de paladio fue en un tiempo prescrito como tuberculosis tratamiento a razón de 0,065 g por día (aproximadamente un miligramo por kilogramo de peso corporal). Este tratamiento tenía muchos negativo los efectos secundarios, y más tarde fue sustituido por medicamentos más eficaces.
La afinidad de Palladium de hidrógeno lo llevó a desempeñar un papel esencial en la Fleischmann-Pons experimento en 1989, también conocido como fusión fría.
En el período previo a 2000 , la oferta rusa de paladio al mercado mundial se retrasó en varias ocasiones e interrumpió porque la cuota de exportación no fue concedida el tiempo, debido a razones políticas. La consiguiente compras de pánico de mercado condujo el precio del paladio a un máximo histórico de 1,100 dólares por onza, alcanzado en enero de 2001. Durante el período de tiempo, Ford Motor Company , con el temor de vehículo auto interrupción de la producción debido a una posible escasez de paladio, almacenando grandes cantidades del metal, adquiridos cerca del alto precio. Como los precios posteriormente cayeron a principios de 2001 , Ford perdió casi 1 mil millones dólar dólares estadounidenses .
La demanda mundial de paladio aumentó de 100 toneladas en 1990 a cerca de 300 toneladas en 2000. La producción mundial de las minas fue de 222 toneladas métricas en 2006, según datos del USGS. La mayoría de paladio se utiliza para convertidores catalíticos en la industria del automóvil.
Aparición

En 2005, Rusia fue el principal productor de paladio con al menos el 50% de la cuota mundial, seguido por Sudáfrica, EE.UU. y Canadá, informa el British Geological Survey.
El paladio se encuentra como metal libre y alea con platino y oro con metales del grupo del platino en depósitos de placer de la Montes Urales, Australia , Etiopía , Sur y América del Norte . Es producido comercialmente de níquel - cobre depósitos encontrados en Sudáfrica , Ontario, y Siberia; el enorme volumen de mineral procesado hace esta extracción rentable a pesar de la baja proporción de paladio en estos minerales. Mayor productor individual de paladio del mundo es MMC Norilsk Nickel produce a partir de la Depósitos de níquel Norilsk-Talnakh. La Merensky Arrecife de las Bushveld ígnea Complejo de Sudáfrica contiene paladio significativa, además de otros elementos del grupo del platino. La Stillwater complejo ígneo de Montana también contiene paladio explotable.
Palladium también se produce en la fisión nuclear y reactores puede ser extraído de combustible nuclear gastado, ver Síntesis de metales nobles, aunque la cantidad producida es insignificante.
El paladio se encuentra en los minerales raros coopérite y polarité.
Características

El paladio es un metal blanco plateado suave que se asemeja a platino . Es el menos denso y tiene el más bajo punto de fusión de la metales del grupo del platino. Es suave y dúctil cuando recocido y aumenta considerablemente su resistencia y dureza cuando es trabajado en frío. Palladium es atacado químicamente por sulfúrico , nítrico , y ácido clorhídrico en el que se disuelve lentamente. Este metal también no reacciona con el oxígeno a temperaturas normales (y por lo tanto no se empaña en el aire ). Palladium calentó a 800 ° C producirá una capa de paladio (II) óxido (DOP). Es levemente empaña en húmedo atmósfera que contiene azufre.
Este metal tiene la capacidad infrecuente absorber hasta 900 veces su propio volumen de hidrógeno a temperatura ambiente. Se cree que esto posiblemente formas hidruro de paladio (PDH 2), pero aún no está claro si se trata de un verdadero compuesto químico .
Cuando el paladio ha absorbido grandes cantidades de hidrógeno, se expandirá ligeramente en tamaño.
Comunes estados de oxidación de paladio son 0, + 1, 2 y 4. Aunque originalmente se pensó 3 como uno de los estados de oxidación fundamentales de paladio, no hay evidencia para el paladio que ocurre en el estado de oxidación +3; esto ha sido investigado a través Difracción de rayos X para un número de compuestos, lo que indica una dímero de paladio (II) y paladio (IV) en su lugar. Recientemente, se sintetizaron los compuestos con un estado de oxidación +6.
Isótopos
Paladio natural se compone de seis isótopos . El más estable radioisótopos son 107 Pd con una vida media de 6,5 millones de años, 103 Pd con una vida media de 17 días, y 100 Pd con una vida media de 3,63 días. Dieciocho otros radioisótopos se han caracterizado con pesos atómicos que van desde 92.936 u (93 Pd) a 119.924 u (120 Pd). La mayoría de estos tienen vidas medias que son menos de media hora, excepto 101 Pd (vida media: 8,47 horas), 109 Pd (vida media: 13.7 horas), y 112 Pd (vida media: 21 horas) .
El primario modo de decaimiento antes del isótopo estable más abundante, 106 Pd, es captura de electrones y el modo primario después de que se desintegración beta. El primario producto de la desintegración antes 106 Pd es rodio y el producto primario después es plata .
Radiogénica 107 Ag es un producto de desintegración del 107 Pd y fue descubierto por primera vez en la Santa Clara, California meteorito de 1978 . Los descubridores sugieren que la fusión y diferenciación de los pequeños planetas con núcleo de hierro pueden haber producido 10 millones años después de un evento nucleosíntesis. 107 Pd frente a Ag correlaciones observadas en los cuerpos, que claramente han sido fundidos desde la acreción del sistema solar , debe reflejar la presencia de nucleidos de corta vida en el sistema solar primitivo.
Aplicaciones
El paladio se utiliza en odontología, reloj de decisiones, en las tiras de prueba de azúcar en la sangre, en los aviones bujías y en la producción de instrumentos quirúrgicos y contactos eléctricos. Palladium también se utiliza para hacer profesional flautas transversales.
Electrónica
La mayor aplicación de paladio en la electrónica está haciendo la condensador cerámico multicapa. Paladio (paladio y plata aleaciones) se utilizan como electrodos en cerámica multicapa condensadores. Palladium (a veces aleado con níquel ) se utiliza en recubrimientos del conector en la electrónica de consumo.
También se utiliza en el enchapado de componentes electrónicos y en materiales de soldadura. El sector de la electrónica consume 1,07 millones de onzas troy de paladio en 2006, según un Informe de Johnson Matthey.
Tecnología
El hidrógeno se difunde fácilmente a través de paladio calentado; por lo tanto, proporciona un medio de purificar el gas. Por lo tanto, reactores de membrana con membranas de Pd se utilizan para la producción de hidrógeno .
Es como parte de la electrodo de paladio hidrógeno en estudios electroquímicos. Palladium (II) cloruro puede absorber grandes cantidades de monóxido de carbono gas, y se utiliza en Detectores de monóxido de carbono.
Catálisis
Cuando se está finamente dividido, tal como en paladio sobre carbono, paladio constituye un buen catalizador y se utiliza para acelerar la hidrogenación y reacciones de deshidrogenación, así como en craqueo de petróleo. Una gran cantidad de enlace carbono-carbono en reacciones de formación de la química orgánica (como el Diablos y Suzuki acoplamiento) son facilitadas por la catálisis con compuestos de paladio. El mayor uso de paladio hoy está en convertidores catalíticos.
Pd es también un metal versátil para catálisis homogénea. Se utiliza en combinación con una amplia variedad de ligandos para transformaciones químicas altamente selectivos.
El almacenamiento de hidrógeno
Hidruro de paladio es paladio metálico que contiene una cantidad sustancial de hidrógeno dentro de su red cristalina. En la temperatura ambiente y la atmósfera presión, paladio puede absorber hasta 935 veces su propio volumen de hidrógeno en un proceso reversible. Esta propiedad ha sido investigado porque el almacenamiento de hidrógeno es de tal interés y una mejor comprensión de lo que sucede a nivel molecular podría dar pistas a diseñar mejor las hidruros de metal. Un almacén de base de paladio, sin embargo, sería prohibitivamente caro debido al coste del metal.
Joyas

Palladium sí mismo de vez en cuando se ha utilizado como un metal precioso en joyería , como reemplazo para el platino o oro blanco. Esto es debido a sus propiedades naturalmente blancos que le dan hay necesidad de una rodio chapado. Es ligeramente más blanca, mucho más ligero y un 12% más. Al igual que el oro, el paladio puede ser golpeado en una forma de hoja delgada tan delgada como 100 nm (1 / 250.000 en). Al igual que el platino, se desarrollará una nebulosa pátina con el tiempo. A diferencia de platino, sin embargo, el paladio se decoloran en temperaturas de soldadura, se vuelven frágiles con calefacción y enfriamiento repetido, y reaccionan con los ácidos fuertes.
También se puede utilizar como un sustituto para el níquel al hacer oro blanco. El paladio es uno de los tres metales más utilizados que pueden ser aleado con el oro para producir oro blanco. ( níquel y plata también pueden usarse.) Palladium-oro es una aleación mucho más caro que el níquel-oro, pero es hipoalergénico y mantiene su color blanco mejor.
Cuando el platino se declaró un recurso estratégico del gobierno durante la Segunda Guerra Mundial , se hicieron muchas bandas de joyería de paladio. Recientemente, en septiembre de 2001, el paladio era más caro que el platino y rara vez se utiliza en la joyería también se debe al obstáculo técnico de casting. Sin embargo el problema de fundición se ha resuelto, y su uso en la joyería ha aumentado debido a un gran aumento en el precio del platino y una caída en el precio del paladio.
Antes de 2004, el principal uso de paladio en la joyería era como una aleación en la fabricación de joyas de oro blanco, pero, a partir de principios de 2004, cuando el oro y los precios del platino comenzaron a subir abruptamente, joyeros chinos comenzaron la fabricación de volúmenes significativos de la joyería de paladio. Johnson Matthey estima que, en 2004, con la introducción de la joyería de paladio en China, la demanda de paladio para la fabricación de joyas era de 920.000 onzas, o aproximadamente el 14% de la demanda total de paladio para el año 2004, un incremento de casi 700.000 oz de 2003. Este crecimiento continuó durante el año 2005, estimando la demanda de joyas de todo el mundo para el paladio de 1,4 millones de onzas, o casi el 21% de la oferta neta de paladio, de nuevo con la mayor parte de la demanda se centró en China.
Fotografía
Con el platinotipia fotógrafos proceso de impresión hacen de bellas artes impresiones en blanco y negro, utilizando sales de platino o paladio. A menudo se utiliza con el platino, el paladio ofrece una alternativa a la plata.
Arte
Hoja Palladium es una de varias alternativas a la hoja de plata usado en la iluminación de manuscritos. El uso de la hoja de plata es problemático debido a su predisposición a empañar. Hoja de aluminio es una alternativa muy barato, sin embargo aluminio es mucho más difícil de trabajar que el oro o la plata y los resultados en menos de resultados óptimos cuando se emplean técnicas tradicionales leafing de metal, y así la hoja de paladio se considera el mejor sustituto a pesar de su coste considerable. Hoja de platino se puede usar para el mismo efecto que la hoja de paladio con propiedades de trabajo similares, pero no es tan fácilmente disponible comercialmente en forma de hoja.