
Ac??tyl??ne
Contexte des ??coles Wikip??dia
Arrangeant une s??lection Wikipedia pour les ??coles dans le monde en d??veloppement sans internet a ??t?? une initiative de SOS Enfants. Parrainer un enfant de faire une r??elle diff??rence.
| Ac??tyl??ne | |
|---|---|
| | |
 | |
??thyne | |
| Identificateurs | |
| Num??ro CAS | 74-86-2 |
| images de Jmol-3D | Image 1 |
SMILES
| |
| Propri??t??s | |
| Formule mol??culaire | C 2 H 2 |
| Masse molaire | 26,0373 g / mol |
| Densit?? | 1,09670 kg / m?? de gaz ?? |
| Point de fusion | -84 ?? C (189 K, subl) |
| Acidit?? (p K a) | 25 |
| Sauf indication contraire, les donn??es sont donn??es pour le mat??riel dans leur ??tat standard (?? 25 ?? C, 100 kPa) | |
| R??f??rences d'Infobox | |
Ac??tyl??ne ( syst??matique nom: ??thyne), C 2 H 2, est un hydrocarbure appartenant au groupe de alcynes. Elle est consid??r??e comme la plus simple des alcynes comme il se compose de deux hydrog??ne atomes et deux carbones atomes. L'ac??tyl??ne est un insatur?? compos?? organique parce que ses deux atomes de carbone sont triplement li??.
Le triple liaison carbone-carbone laisse les atomes de carbone avec deux orbitales sp hybrides pour la liaison sigma, en pla??ant les quatre atomes dans la m??me ligne droite, avec des angles de liaison de CCH de 180 ??.
Ac??tyl??ne a ??t?? d??couvert en 1836 par Edmund Davy qui l'a identifi?? comme un ??nouveau carbure d'hydrog??ne." Elle a ??t?? red??couverte en 1860 par le chimiste fran??ais Marcellin Berthelot, qui a invent?? le nom "d'ac??tyl??ne." Le laur??at du prix Nobel Gustaf Dal??n a ??t?? aveugl?? par une explosion ac??tyl??ne.
Pr??paration
Les principales mati??res premi??res pour la fabrication d'ac??tyl??ne sont le carbonate de calcium ( calcaire) et le charbon . Le carbonate de calcium est d'abord converti en oxyde de calcium et du charbon en coke, puis les deux sont mis ?? r??agir les uns avec les autres pour former le carbure de calcium et l'oxyde de carbone :
- CaO + 3C → CO + CaC 2
Calcium carbure (ou ac??tylure de calcium) et de l'eau sont ensuite mis ?? r??agir par une quelconque de plusieurs m??thodes pour produire de l'ac??tyl??ne et l'hydroxyde de calcium. Cette r??action a ??t?? d??couvert par Friedrich W??hler en 1862.
- CaC 2 + 2H 2 O → Ca (OH) 2 + C 2 H 2
La synth??se de carbure de calcium n??cessite une temp??rature extr??mement ??lev??e, ~ 2000 degr??s Celsius, de sorte que la r??action est effectu??e dans un Four ?? arc ??lectrique. Cette r??action ??tait une partie importante de la r??volution fin des ann??es 1800 dans la chimie permis par le massif projet d'??nergie hydro??lectrique ?? Niagara Falls .
L'ac??tyl??ne peut aussi ??tre fabriqu??e par le partiel combustion du m??thane ?? l'oxyg??ne , ou par le fissuration de des hydrocarbures.
Berthelot a pu pr??parer de l'ac??tyl??ne ?? partir de l'alcool m??thylique , l'alcool ??thylique , l'??thyl??ne ou l'??ther , quand il passait quelconque de ceux-ci sous forme de gaz ou de vapeur ?? travers un tube chauff?? au rouge. Berthelot a ??galement constat?? l'ac??tyl??ne a ??t?? form?? en suscitant l'??lectricit?? ?? travers m??lang?? cyanog??ne et hydrog??ne gaz. Il a ??galement ??t?? en mesure de former l'ac??tyl??ne directement en combinant l'hydrog??ne pur avec du carbone ?? l'aide d'une d??charge ??lectrique arc de carbone.
R??actions
- Au-dessus de 400 ?? C (673 K) la pyrolyse de l'ac??tyl??ne va commencer, ce qui est relativement faible pour un hydrocarbure. Les principaux produits sont les dim??re vinylac??tyl??ne (C 4 H 4) et le benz??ne . A des temp??ratures sup??rieures ?? 900 ?? C (1173 K), le produit principal sera suie.
- Utilisation de l'ac??tyl??ne, Berthelot fut le premier ?? montrer qu'une compos?? aliphatique pourrait former un Compos?? aromatique quand il chauffe l'ac??tyl??ne dans un tube de verre pour produire du benz??ne avec de tolu??ne . Berthelot oxyd?? ac??tyl??ne pour donner de l'acide ac??tique et l'acide oxalique. Il a trouv?? ac??tyl??ne peut ??tre r??duit pour former de l'??thyl??ne et de l'??thane .
- La polym??risation de l'ac??tyl??ne avec Les catalyseurs de Ziegler-Natta produit films polyac??tyl??ne. Polyac??tyl??ne, une cha??ne de mol??cules de carbone avec une alternance de liaisons simples et doubles, fut le premier semi-conducteur organique ?? d??couvrir; r??action avec l'iode produit un mat??riau extr??mement conducteur.
- Dans la r??action Kucherov (invent?? en 1881 par le chimiste russe Mikhail Kucherov) est l'ac??tyl??ne hydrat?? de l'ac??tald??hyde avec un mercure sel tel que de mercure (II) bromure. Avant l'av??nement du proc??d?? Wacker cette r??action a ??t?? r??alis??e ?? l'??chelle industrielle.
Reppe chimie
Walter Reppe d??couvert que l'ac??tyl??ne peut r??agir ?? des pressions ??lev??es avec m??taux lourds catalyseurs pour donner des produits chimiques ?? fort potentiel industriel:
- Ac??tyl??ne r??agir avec des alcools , du cyanure d'hydrog??ne , le chlorure d'hydrog??ne, ou des acides carboxyliques pour donner des compos??s vinyliques:
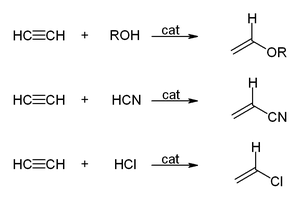
- Avec ald??hydes pour donner diols ??thynyle.
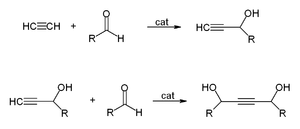
Ce est utilis?? industriellement pour produire 1,4-butynediol ?? partir de formald??hyde et de l'ac??tyl??ne:
- HCCH + CH 2 O → 2 CH (OH) 2 OH CCCH
- Avec du monoxyde de carbone pour donner l'acide acrylique, les esters acryliques ou qui peut ??tre utilis?? pour produire verre acrylique.
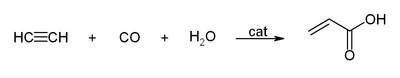
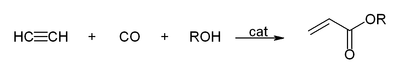
- Cyclicization pour donner du benz??ne et cyclooctat??tra??ne:
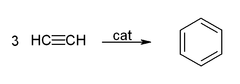

Utilisations
Environ 80 pour cent de l'ac??tyl??ne dans le produit annuellement aux Etats-Unis est utilis?? dans la synth??se chimique. Les 20 pour cent restants sont utilis??s principalement pour oxyac??tyl??nique soudage au gaz et coupe en raison de la temp??rature ??lev??e de la flamme; combustion de l'ac??tyl??ne avec de l'oxyg??ne produit une flamme de plus de 3300 ?? C (6000 ?? F), lib??rant 11,8 kJ / g. Oxyac??tyl??nique est le gaz combustion de carburant commune la plus chaude. Cyanog??ne, un gaz plus exotiques, produit une flamme de plus de 4525 ?? C (8180 ?? F) quand il br??le dans l'oxyg??ne.
L'ac??tyl??ne est ??galement utilis?? dans le ac??tyl??ne (??carbure??) lampe, une fois utilis?? par les mineurs (?? ne pas confondre avec le Davy lampe), sur les anciennes voitures , et encore parfois utilis?? par sp??l??ologues. Dans ce contexte, l'ac??tyl??ne est g??n??r?? par ??gouttement de l'eau de la chambre sup??rieure de la lampe sur le carbure de calcium (CaC 2 de) des granul??s dans le culot de la lampe.
Autrefois quelques villes d'ac??tyl??ne utilis??s pour l'??clairage, y compris Tata en Hongrie o?? il a ??t?? install?? sur 24 Juillet 1897 , et North Petherton, l'Angleterre en 1898.
Dans les temps modernes l'ac??tyl??ne est parfois utilis?? pour carburation (ce est-?? durcissement) de l'acier lorsque l'objet est trop volumineux pour tenir dans un four.
L'ac??tyl??ne a ??t?? propos??e comme une charge d'alimentation pour le carbone fabrication mol??culaire en utilisant la nanotechnologie. Comme il ne se produit pas naturellement, en utilisant l'ac??tyl??ne pourrait limiter out-of-commande auto-r??plication.
L'ac??tyl??ne est utilis?? pour volatiliser en carbone datation au radiocarbone. Le mat??riau carbon?? dans l'??chantillon arch??ologique a r??agi dans un petit four de recherche sp??cialis?? avec le lithium m??tal pour former carbure de lithium (??galement connu sous le nom ac??tylure de lithium). Le carbure peut alors ??tre mis ?? r??agir avec de l'eau, comme d'habitude, pour former du gaz d'ac??tyl??ne ?? ??tre introduit dans le spectrom??tre de masse pour trier le rapport isotopique du carbone 14 au carbone 12.
Le Futur
L'utilisation de l'ac??tyl??ne devrait se poursuivre une augmentation progressive de l'avenir que de nouvelles applications sont d??velopp??es. Une nouvelle application est la conversion d'ac??tyl??ne en ethylene pour la fabrication d'une vari??t?? de mati??res plastiques de poly??thyl??ne. Dans le pass??, une petite quantit?? d'ac??tyl??ne avait ??t?? g??n??r?? et gaspill?? dans le cadre du processus de craquage ?? la vapeur utilis?? pour fabriquer de l'??thyl??ne. Un nouveau catalyseur d??velopp?? par Phillips Petroleum permet plus de cet ac??tyl??ne ?? convertir en ??thyl??ne pour augmenter les rendements ?? un co??t global r??duit.
S??curit?? et la manipulation
Compression
En raison de la triple liaison carbone-carbone, du gaz ac??tyl??ne est fondamentalement instable, et la volont?? d??composer dans un exothermique r??action si comprim?? dans une mesure importante. Ac??tyl??ne peut exploser avec une extr??me violence si la pression du gaz d??passe environ 100 kPa (≈14.5 psi) comme un gaz ou sous forme liquide ou solide, il est transport?? et stock?? dissous dans l'ac??tone ou le dim??thylformamide (DMF), contenue dans un cylindre m??tallique avec un remplissage poreux ( Agamassan), ce qui le rend s??r ?? transporter et ?? utiliser.
Il ya des r??glements stricts sur l'exp??dition des dangereux les bouteilles de gaz ?? travers le monde. L'utilisation de l'ac??tyl??ne dissous diminue rapidement, en raison de sans flamme favorables soudage processus.
Les effets toxiques
L'inhalation de l'ac??tyl??ne peut causer des ??tourdissements, des maux de t??te et des naus??es. Il peut ??galement contenir des impuret??s toxiques: le Sp??cification Commodity Compressed Gas Association pour l'ac??tyl??ne a ??tabli un syst??me de classement pour identifier et quantifier phosphine, arsine, et teneur en sulfure d'hydrog??ne dans les qualit??s commerciales de l'ac??tyl??ne afin de limiter l'exposition ?? ces impuret??s. Le soufre, le phosphore et l'arsenic sont reports de la synth??se ingr??dient coke, une forme impure de carbone et diff??rents, les impuret??s organiques pourrait se attendre du craquage thermique d'hydrocarbures la source.
Alors que les impuret??s dans l'ac??tyl??ne peuvent ??tre toxiques et m??me mortels, l'ac??tyl??ne pur est d'une tr??s faible toxicit?? (sans compter les effets ??stup??fiant??). Jusqu'?? 80% pour cent (v / v) d'ac??tyl??ne a ??t?? administr?? ?? des patients en chirurgie comme anesth??sie g??n??rale. Le nom commercial pour l'ac??tyl??ne ??tait "narcylene." Il a ??t?? utilis?? une bonne quantit?? exp??rimentalement en Allemagne en 1920 leurs pauvres de, peut-??tre sur plusieurs milliers de patients. M??dicalement, l'ac??tyl??ne a ??t?? consid??r??e comme presque aussi s??r que le protoxyde d'azote et avec une puissance l??g??rement plus ??lev??e, ce qui permet l'utilisation de pourcentages ??lev??s d'oxyg??ne dans le m??lange; il est environ 50% plus puissant. Cependant, l'utilisation de m??langes d'ac??tyl??ne et d'oxyg??ne a ??t?? abandonn?? apr??s plusieurs explosions de gaz ?? l'int??rieur des poumons du patient. L'??nergie de ces explosions serait devrait d??passer l'un des anesth??siques par inhalation inflammables en raison de l'instabilit?? de la triple liaison (cyclopropane serait presque aussi mauvais). Il a ??t?? sugg??r?? qu'une telle explosion du thorax interne ne pouvait pas se produire avec des m??langes air (sans oxyg??ne purifi??).
Ac??tyl??ne a ??t?? rarement abus?? d'une mani??re semblable ?? l'abus de l'oxyde nitreux ?? travers les temps modernes, selon la litt??rature. Ces abus peuvent entra??ner la mort de l'agresseur en raison de la toxicit?? des impuret??s mentionn??es ci-dessus phosphine, arsine, et sulfure d'hydrog??ne. Comme le gaz est charg?? (absorb??e) dans des r??servoirs impr??gn??s avec de l'ac??tone sur une matrice solide, un peu d'ac??tone sort avec le gaz, contribuant davantage ?? les empoisonnements. Le pilote de ce comportement abusif est mieux comprise ?? la vue des propri??t??s anesth??siques de l'ac??tyl??ne et les comportements addictifs.
Impuret??s dans l'ac??tyl??ne sont facilement d??tectables par l'odorat. Ac??tyl??ne pur est un gaz incolore et inodore. La caract??ristique de l'ail l'odeur de l'ac??tyl??ne de qualit?? technique est attribuable ?? la contamination par des impuret??s. Les impuret??s qui peuvent ??tre pr??sents comprennent: sulfure de divinyle, l'ammoniac , l'oxyg??ne , l'azote , phosphine, arsine, m??thane , dioxyde de carbone , monoxyde de carbone , sulfure d'hydrog??ne, ac??tyl??ne vinylique, divinyl ac??tyl??ne, diac??tyl??ne, propadi??ne, hexadi??ne, butadi??nyle ac??tyl??ne, et ac??tyl??ne de m??thyle.
Risque d'incendie
Les m??langes avec de l'air contenant entre 3% et 82% d'ac??tyl??ne sont explosifs au feu. La temp??rature minimale d'inflammation est de 335 ?? C. La majorit?? de l'??nergie chimique de l'ac??tyl??ne est ce qui ne est pas contenue dans la triple liaison carbone-carbone; qui est, il est sup??rieur ?? celui des trois liaisons carbone-carbone r??partis, mais celui-ci est refus?? en raison des espaces entre son carbone mate et tous les autres carbones m??me blind??s en charge.
Incompatibilit??s
Autres significations
Parfois, les "ac??tyl??nes" pluriel peuvent se r??f??rer ?? la classe de compos??s chimiques organiques appel??es alcynes qui contiennent le groupe -C = C-.
Occurrence naturelle
L'ac??tyl??ne est un produit chimique mod??r??ment commune dans l'univers, souvent associ??e ?? des atmosph??res des g??antes gazeuses . Une curieuse d??couverte de l'ac??tyl??ne est sur Encelade, une lune de Saturne . Ac??tyl??ne naturel est cens?? former, ?? partir soit de catalyseur de d??composition d'hydrocarbures ?? cha??nes longues ou ?? des temp??ratures ≥ 1770 kelvin . ??tant donn?? que ces temp??ratures sont tr??s peu probable sur un si petit corps lointain, cette d??couverte est potentiellement ??vocateurs de r??actions catalytiques dans la lune, ce qui en fait un site prometteur pour rechercher la chimie pr??biotique.
