Liquide
Saviez-vous ...
SOS Enfants, un organisme de bienfaisance de l'??ducation , a organis?? cette s??lection. M??res SOS chaque regard apr??s une une famille d'enfants parrain??s .

| M??canique des milieux continus |
|---|
 |
Lois
|
M??canique des solides
|
|
Rh??ologie
|
Le liquide est l'un des les quatre ??tats fondamentaux de la mati??re (les autres ??tant solide , gaz et plasma ), et est le seul Etat avec un volume d??fini, mais pas de forme fixe. Un liquide est constitu?? de minuscules particules de vibration de la mati??re, tels que les atomes et mol??cules, maintenues ensemble par des liaisons intramol??culaires. L'eau est, de loin, le liquide le plus courant de la plan??te. Comme un gaz, un liquide est capable de se ??couler et prendre la forme d'un r??cipient. Certains liquides r??sister ?? la compression, tandis que d'autres peuvent ??tre compress??s. Contrairement ?? un gaz, un liquide ne se disperse pas ?? remplir chaque espace d'un conteneur, et maintient une densit?? relativement constante. Une propri??t?? caract??ristique de l'??tat liquide est la tension de surface , conduisant ?? les ph??nom??nes de mouillage.
La densit?? d'un liquide est habituellement voisine de celle d'un solide, et beaucoup plus ??lev?? que dans un gaz. Par cons??quent, liquide et solide sont ?? la fois appel?? la mati??re condens??e . D'autre part, comme des liquides et des gaz part l'aptitude ?? l'??coulement, ils sont tous deux appel??s fluides. Bien que l'eau liquide est abondant sur Terre, cet ??tat de la mati??re est en fait la moins courante dans l'univers connu, car les liquides n??cessitent une gamme relativement ??troite temp??rature / pression d'exister. Question la plus connue dans l'univers est sous forme gazeuse (avec des traces de mati??re solide d??tectable) que les nuages interstellaires ou sous forme de plasma ?? l'int??rieur des ??toiles.
Introduction

Le liquide est l'une des trois primaires ??tats de la mati??re, avec les autres ??tant solide et le gaz . Un liquide est un fluide. Contrairement ?? un solide, les mol??cules dans un liquide ont une bien plus grande libert?? de mouvement. Les forces qui lient les mol??cules dans un ensemble ne sont que temporaires solide dans un liquide, permettant ?? un liquide de se ??couler alors que subsiste un solide rigide.
Un liquide, comme un gaz, affiche les propri??t??s d'un fluide. Un liquide peut se ??couler, prendre la forme d'un r??cipient, et, se il est plac?? dans un r??cipient herm??tique, distribuera pression appliqu??e uniform??ment sur toutes les surfaces dans le r??cipient. Contrairement ?? un gaz, un liquide peut pas toujours se m??langer facilement avec un autre liquide, ne sera pas toujours remplir chaque espace dans le conteneur, formant sa propre surface, et ne sera pas compresser significativement, sauf sous des pressions extr??mement ??lev??es. Ces propri??t??s en font un liquide appropri?? pour des applications telles que hydraulique.
Particules liquides sont tenus fermement, mais pas de fa??on rigide. Ils sont capables de se d??placer librement autour de l'autre, ce qui entra??ne un certain degr?? de mobilit?? des particules. Comme les temp??rature augmente, l'augmentation des vibrations des mol??cules provoque distances entre les mol??cules d'augmenter. Lorsqu'un liquide atteint son point d'??bullition , les forces de coh??sion qui lient les mol??cules se brisent en ??troite collaboration, et les changements de liquide ?? l'??tat gazeux (sauf surchauffe se produit). Si la temp??rature est diminu??e, les distances entre les mol??cules deviennent plus petites. Lorsque le liquide atteint son point de cong??lation les mol??cules habituellement enfermer dans un ordre tr??s sp??cifique, appel??e cristallisation, et les liens entre eux deviendra plus rigide, en changeant le liquide dans son ??tat solide (?? moins que surfusion se produit).
Exemples
Seuls deux ??l??ments sont liquides ?? conditions normales de temp??rature et de pression: le mercure et le brome . Quatre autres ??l??ments ont des points de fusion l??g??rement sup??rieur ?? temp??rature ambiante: francium , le c??sium , le gallium et le rubidium . Les alliages m??talliques qui sont liquides ?? temp??rature ambiante comprennent NaK, d'un alliage de m??tal de sodium-potassium, Galinstan, un liquide d'alliage fusible et certaines amalgames (alliages impliquant mercure).
Les substances pures qui sont liquides dans les conditions normales comprennent l'eau , l'??thanol et d'autres solvants organiques. L'eau liquide est d'une importance vitale dans la chimie et de la biologie; il est consid??r?? comme une n??cessit?? pour l'existence de la vie .
Liquides quotidiens importants comprennent aqueuses solutions comme m??nage l'eau de Javel, autre des m??langes de diff??rentes substances telles que huile min??rale et essence, ??mulsions comme vinaigrette ou mayonnaise, suspensions comme le sang , et collo??des comme peinture et le lait .
Beaucoup de gaz peuvent ??tre liqu??fi??s par refroidissement, la production de liquides tels que l'oxyg??ne liquide, l'azote liquide, un atome d'hydrog??ne liquide et h??lium liquide. Pas tous les gaz peuvent ??tre liqu??fi??s sous pression atmosph??rique, par exemple du dioxyde de carbone ne peut ??tre liqu??fi?? ?? des pressions sup??rieures ?? 5,1 atm.
Certains mat??riaux ne peuvent pas ??tre class??es dans les trois ??tats de la mati??re classiques; ils poss??dent des propri??t??s solides et liquides-comme-like. Les exemples incluent des cristaux liquides utilis??s dans les ??crans LCD, et des membranes biologiques.
Applications
Les liquides ont une vari??t?? d'utilisations, comme les lubrifiants, les solvants et les liquides de refroidissement. Dans les syst??mes hydrauliques, le liquide est utilis?? pour transmettre la puissance.
En tribologie, liquides sont ??tudi??s pour leurs propri??t??s lubrifiants. Des lubrifiants tels que l'huile sont choisis pour caract??ristiques de viscosit?? et d'??coulement qui sont appropri??s tout au long de la Temp??rature de fonctionnement du composant. Les huiles sont souvent utilis??s dans les moteurs, bo??tes de vitesses, la m??tallurgie, et des syst??mes hydrauliques pour leurs bonnes propri??t??s de lubrification.
De nombreux liquides sont utilis??s en tant que solvants , ?? dissoudre d'autres liquides ou solides. Des solutions sont trouv??es dans une grande vari??t?? d'applications, y compris peintures, mastics, et les adh??sifs. Naphte et l'ac??tone sont fr??quemment utilis??s dans l'industrie pour nettoyer l'huile, la graisse et le goudron de pi??ces et de machinerie. Les fluides corporels sont des solutions ?? base d'eau.
Les tensioactifs sont g??n??ralement trouv??s dans des savons et d??tergents. Des solvants tels que l'alcool sont souvent utilis??s comme antimicrobiens. On les trouve dans cosm??tiques, encres et liquide lasers ?? colorant. Ils sont utilis??s dans l'industrie alimentaire, dans des proc??d??s tels que l'extraction de huile v??g??tale.
Liquides ont tendance ?? avoir une meilleure la conductivit?? thermique de gaz, et la capacit?? d'??coulement permet un liquide appropri?? pour ??liminer l'exc??s de chaleur ?? partir de composants m??caniques. La chaleur peut ??tre ??vacu??e par la canalisation du liquide ?? travers un Echangeur de chaleur, tel qu'un un radiateur ou de la chaleur peut ??tre ??vacu??e avec le liquide pendant ??vaporation. L'eau ou r??frig??rants de glycol sont utilis??s pour garder moteurs de la surchauffe. Les liquides de refroidissement utilis??s dans les r??acteurs nucl??aires comprennent l'eau ou de liquides, tels que des m??taux sodium ou de bismuth . Films de propergol liquide sont utilis??s pour refroidir les chambres de pouss??e de roquettes. En usinage, l'eau et les huiles sont utilis??es pour ??liminer l'exc??s de chaleur g??n??r??e, ce qui peut rapidement ruiner la fois la pi??ce et l'outillage. Pendant sueur, la sueur ??vacue la chaleur du corps humain par ??vaporation. Dans le Chauffage, ventilation et climatisation industrie (CVC), les liquides tels que l'eau sont utilis??s pour transf??rer la chaleur d'un endroit ?? un autre.
Liquid est le composant principal du syst??mes hydrauliques, qui tirent avantage de La loi de Pascal ?? fournir ??nergie hydraulique. Les dispositifs tels que les pompes et roues hydrauliques ont ??t?? utilis??s pour modifier le mouvement du liquide dans le travail m??canique depuis les temps anciens. Les huiles sont forc??s ?? travers pompes hydrauliques, qui transmettent cette force des v??rins hydrauliques. Syst??me hydraulique peut ??tre trouv??e dans de nombreuses applications, telles que freins automobile et transmissions, ??quipement lourd, et les syst??mes de contr??le de l'avion. Divers presses hydrauliques sont largement utilis??s dans la r??paration et la fabrication, de levage, de pression, de serrage et de formage.
Les liquides sont parfois utilis??s dans les appareils de mesure. Un thermom??tre utilise souvent le la dilatation thermique de liquides, tels que le mercure , associ??e ?? leur capacit?? ?? se ??couler pour indiquer la temp??rature. Un manom??tre utilise le poids du liquide ?? indiquer pression d'air.
Propri??t??s m??caniques
Volume
Quantit??s de liquides sont g??n??ralement mesur??s en unit??s de volume de . Ceux-ci comprennent le Unit?? SI m??tre cube (m 3) et de ses divisions, en particulier le d??cim??tre cube, plus commun??ment appel?? le litre (1 dm 3 = 1 L = 0,001 m 3), et le centim??tre cube, ??galement appel?? millilitre (1 cm 3 = 1 mL = 0,001 L = 10 -6 m 3).
Le volumique d'une quantit?? de liquide est fix??e par sa temp??rature et pression. Liquides ??tendre g??n??ralement lorsqu'il est chauff?? et contrat lorsque refroidi. L'eau entre 0 ?? C et 4 ?? C est une exception notable. Liquides ont peu compressibilit??: l'eau, par exemple, n??cessite une pression de l'ordre de 200 bar pour augmenter sa densit?? par 1/1000. Dans l'??tude de la dynamique des fluides, liquides sont souvent trait??es comme incompressible, en particulier lorsque l'on ??tudie ??coulement incompressible.
Pression et flottabilit??
Dans un champ gravitationnel, liquides exercent la pression sur les c??t??s d'un r??cipient, ainsi que sur ne importe quoi dans le liquide lui-m??me. Cette pression est transmise dans tous les sens et augmente avec la profondeur. Si un liquide est au repos dans un champ gravitationnel uniforme, la pression, p, ?? ne importe quelle profondeur, z, est donn??e par
o??:
 est la densit?? du liquide (suppos??e constante)
est la densit?? du liquide (suppos??e constante) 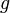 est l' acc??l??ration de la pesanteur .
est l' acc??l??ration de la pesanteur .
A noter que cette formule suppose que la pression au niveau de la surface libre est ??gale ?? z??ro et que la tension superficielle effets peut ??tre n??glig??e.
Les objets sont immerg??s dans un liquide soumis au ph??nom??ne de flottabilit??. (Flottabilit?? est ??galement observ?? dans d'autres fluides, mais il est particuli??rement forte dans les liquides en raison de leur haute densit??.)
Surfaces

?? moins que le volume d'un liquide correspond exactement au volume de son r??cipient, une ou plusieurs surfaces sont observ??es. La surface d'un liquide se comporte comme une membrane ??lastique, dans lequel la tension de surface affiche, permettant la formation de les gouttes et bulles. Les ondes de surface, action capillaire, mouillant, et ondulations sont d'autres cons??quences de la tension de surface .
Flux
des mesures de viscosit?? de la r??sistance d'un liquide qui est soit d??form?? par une contrainte de cisaillement ou une contrainte en extension.
Lorsqu'un liquide est surfondue vers la de transition vitreuse, la viscosit?? augmente de fa??on spectaculaire! Le liquide devient alors un milieu visco??lastique qui montre ?? la fois la l'??lasticit?? d'un solide et la fluidit?? d'un liquide, en fonction de l'??chelle de temps de l'observation ou de la fr??quence de perturbation.
Propagation du son
Dans un fluide de la seule non nulle la rigidit?? ?? la d??formation volum??trique est (ne est pas un fluide ?? maintenir des forces de cisaillement). D'o?? la vitesse du son dans un fluide est donn??e par 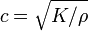 o?? K est le module de compressibilit?? du fluide, et la densit?? ρ. Pour donner une valeur typique, en eau douce c = 1,497 m / s ?? 25 ?? C.
o?? K est le module de compressibilit?? du fluide, et la densit?? ρ. Pour donner une valeur typique, en eau douce c = 1,497 m / s ?? 25 ?? C.
Thermodynamique
Phase transitions

A une temp??rature inf??rieure au point d'??bullition , toute question sous forme liquide se ??vapore jusqu'?? ce que la condensation de gaz ci-dessus atteindre un ??quilibre. ?? ce stade, le gaz se condense ?? la m??me vitesse que le liquide se ??vapore. Ainsi, un liquide ne peut exister de fa??on permanente si le liquide ??vapor?? est ??limin??e en continu. Un liquide ?? son point d'??bullition se ??vapore plus rapidement que le gaz peut se condenser ?? la pression actuelle. Un liquide ?? ou au-dessus de son point d'??bullition est normalement bouillir, bien surchauffe peut emp??cher cela dans certaines circonstances.
A une temp??rature inf??rieure au point de cong??lation d'un liquide aura tendance ?? cristalliser, le passage ?? sa forme solide. Contrairement ?? la transition vers le gaz, il n'y a pas d'??quilibre ?? cette transition sous pression constante, de sorte que si surfusion se produit, le liquide sera finalement compl??tement cristalliser. Notez que ce ne est vrai que sous la pression constante, de sorte que par exemple l'eau et de la glace dans un r??cipient ferm?? forte pourrait parvenir ?? un ??quilibre o?? les deux phases coexistent. Pour le passage en face du solide au liquide, voir fusion.
Solutions
Les liquides peuvent afficher immiscibilit??. Le m??lange le plus familier de deux liquides non miscibles dans la vie quotidienne est le d'huile v??g??tale et de l'eau dans Vinaigrette italienne. Un ensemble familier de liquides miscibles ?? l'eau et l'alcool. Les composants liquides dans un m??lange peuvent souvent ??tre s??par??s l'un de l'autre par distillation fractionn??e.
Propri??t??s microscopiques
Statique facteur de structure

Dans un liquide, les atomes ne forment pas un r??seau cristallin, pas plus qu'ils ne montrent toute autre forme de ordre ?? longue port??e. Ceci est d??montr?? par l'absence de Pics de Bragg dans X-ray et diffraction de neutrons. Dans des conditions normales, le motif de diffraction pr??sente une sym??trie circulaire, l'expression de la isotropie du liquide. En direction radiale, l'intensit?? de diffraction oscille doucement. Ceci est g??n??ralement d??crit par la statique facteur de structure S (q), avec un nombre d'onde q = (4π / λ) sin donn??e par la longueur d'onde λ de la sonde (photon ou un neutron) et le Bragg angle θ. Les oscillations de S (q) expriment l'ordre pr??s du liquide, ce est ?? dire les corr??lations entre un atome et quelques coquilles de pr??s, seconde, ... voisins les plus proches.
Une description plus intuitive de ces corr??lations est donn??e par la fonction de distribution radiale g (r), qui est essentiellement le Transform??e de Fourier S (q). Il repr??sente une moyenne spatiale d'un instantan?? temporelle corr??lations de paires dans le liquide.

Dispersion sonore et relaxation structurale
L'expression ci-dessus pour la vitesse du son 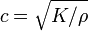 contient la vrac module K. Si K est ind??pendant de la fr??quence, puis le liquide se comporte comme un moyenne lin??aire, de sorte que le son se propage sans dissipation et sans couplage de modes. En r??alit??, tout liquide montre une certaine dispersion: avec une fr??quence croissante, K traverse de la basse fr??quence, limite de type liquide
contient la vrac module K. Si K est ind??pendant de la fr??quence, puis le liquide se comporte comme un moyenne lin??aire, de sorte que le son se propage sans dissipation et sans couplage de modes. En r??alit??, tout liquide montre une certaine dispersion: avec une fr??quence croissante, K traverse de la basse fr??quence, limite de type liquide 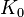 ?? la haute fr??quence, limite solide comme
?? la haute fr??quence, limite solide comme 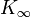 . Dans les liquides normales, la plupart de ces croix sur a lieu ?? des fr??quences entre GHz et THz, parfois appel?? Hypersound.
. Dans les liquides normales, la plupart de ces croix sur a lieu ?? des fr??quences entre GHz et THz, parfois appel?? Hypersound.
A des fr??quences sous-GHz, un liquide normale ne peut pas soutenir des ondes de cisaillement: la limite de fr??quence nulle de la module de cisaillement est 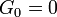 . Ce est parfois consid??r??e comme la propri??t?? la d??finition d'un liquide. Cependant, tout comme le gros module K, le module de cisaillement G est d??pendante de la fr??quence, et ?? des fr??quences de Hypersound il montre une coupe similaire au-dessus de la limite liquide-like
. Ce est parfois consid??r??e comme la propri??t?? la d??finition d'un liquide. Cependant, tout comme le gros module K, le module de cisaillement G est d??pendante de la fr??quence, et ?? des fr??quences de Hypersound il montre une coupe similaire au-dessus de la limite liquide-like 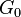 ?? un non-z??ro limite solide comme,
?? un non-z??ro limite solide comme, 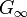 .
.
Selon le Kramers-Kronig rapport, la dispersion de la vitesse du son (donn??e par la partie r??elle de K ou G) va de pair avec un maximum dans l'att??nuation du son (dissipation, donn??e par la partie imaginaire de K ou G). Selon th??orie de r??ponse lin??aire, la transform??e de Fourier de K ou G d??crit la fa??on dont le syst??me retourne ?? l'??quilibre apr??s une perturbation externe; pour cette raison, l'??tape de dispersion dans la zone de GHz..THz est aussi appel??e relaxation structurale. Selon le th??or??me de fluctuation-dissipation, la relaxation vers l'??quilibre est intimement li??e aux fluctuations de l'??quilibre. Les fluctuations de densit?? associ??s avec les ondes sonores peuvent ??tre observ??s exp??rimentalement par diffusion de Brillouin.
Sur surfusion un liquide vers la transition vitreuse, le crossover de type liquide aux mouvements de r??ponse solide comme du GHz ?? MHz, kHz, Hz, ...; de mani??re ??quivalente, le temps caract??ristique de relaxation de structure augmente de ns ?? us, ms, s, ... Ce est l'explication microscopique pour le comportement visco??lastique des liquides mentionn??s ci-dessus de formation de verre.
Effets de l'association
Les m??canismes de atomique / mol??culaire diffusion (ou le d??placement des particules) dans les solides sont ??troitement li??s aux m??canismes de l'??coulement visqueux et la solidification des mat??riaux liquides. Les descriptions de en termes de viscosit?? mol??culaire "espace libre" dans le liquide ont ??t?? modifi??s au besoin pour tenir compte des liquides dont les mol??cules sont connues pour ??tre "associ??e" ?? l'??tat liquide ?? la temp??rature ordinaire. Lorsque plusieurs mol??cules se combinent ensemble pour former une mol??cule associ??e, elles renferment dans un syst??me semi-rigide une certaine quantit?? d'espace qui est disponible avant que l'espace libre pour les mol??cules mobiles. Ainsi, l'augmentation de viscosit?? lors du refroidissement d?? ?? la tendance de la plupart des substances ?? se associer au refroidissement.
Des arguments similaires pourraient ??tre utilis??s pour d??crire les effets de pression sur la viscosit??, o?? on peut supposer que la viscosit?? est principalement fonction du volume pour des liquides ayant un fini compressibilit??. Une augmentation de la viscosit?? ?? l'??l??vation de la pression est donc attendu. En outre, si le volume est dilat?? par la chaleur, mais encore r??duite par la pression, la viscosit?? reste la m??me.
La tendance locale ?? l'orientation de mol??cules en petits groupes pr??te le liquide (comme mentionn?? pr??c??demment) un certain degr?? d'association. Cette association se traduit par une "pression interne" consid??rable au sein d'un liquide, qui est presque enti??rement attribuable ?? ces mol??cules qui, en raison de leurs faibles vitesses temporaires (suite de la distribution de Maxwell) ont coalis??s avec d'autres mol??cules. La pression interne entre plusieurs de ces mol??cules pourrait correspondre ?? celle entre un groupe de mol??cules sous forme solide.