
L'ad??nosine triphosphate
?? propos de ce ??coles s??lection Wikipedia
Cette s??lection Wikipedia est d??connect?? disponibles ?? partir enfants SOS pour la distribution dans le monde en d??veloppement. Avec enfants SOS vous pouvez choisir de parrainer des enfants dans plus de cent pays
| L'ad??nosine triphosphate | |
|---|---|
 | |
 | |
5- (6-aminopurin-9-yl) | |
| Identificateurs | |
| Num??ro CAS | 56-65-5 |
| Propri??t??s | |
| Formule mol??culaire | C 10 H 16 N 5 O 13 P 3 |
| Masse molaire | 507,181 g / mol |
| Acidit?? (p K a) | 6.5 |
| Sauf indication contraire, les donn??es sont donn??es pour le mat??riel dans leur ??tat standard (?? 25 ?? C, 100 kPa) | |
| R??f??rences d'Infobox | |
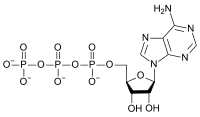
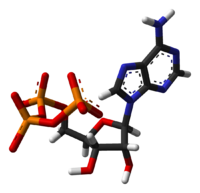
L'ad??nosine 5'-triphosphate (ATP) est un multifonction nucl??otidique qui est le plus important en tant que " mol??culaire monnaie "intracellulaire ??nergie transfert. Dans ce r??le, ATP transporte l'??nergie chimique dans les cellules pour m??tabolisme. Il est produit en tant que source d'??nergie pendant le processus de photosynth??se et la respiration cellulaire et consomm?? par beaucoup enzymes et une multitude de processus cellulaires, y compris r??actions biosynth??tiques, la motilit?? et la division cellulaire. En voies de transduction de signaux, l'ATP est utilis?? comme substrat par kinases phosphoryler des prot??ines et des lipides , ainsi que par l'ad??nylate cyclase, qui utilise de l'ATP pour produire le seconde mol??cule messag??re AMP cyclique.
La structure de cette mol??cule est constitu??e d'une base purique ( ad??nine) fix?? ?? la 1 'atome de carbone d'un sucre pentose ( ribose). Trois groupes phosphate sont fix??s ?? l'extr??mit?? 5 'atome de carbone du sucre pentose. ATP est ??galement incorpor?? dans acides nucl??iques par polymerases dans les processus de r??plication de l'ADN et transcription. Lorsque l'ATP est utilis?? dans la synth??se de l'ADN, le sucre ribose est d'abord converti en d??soxyribose par la ribonucl??otide r??ductase. ATP a ??t?? d??couvert en 1929 par Karl Lohmann, et a ??t?? propos?? pour ??tre la mol??cule principale de transfert d'??nergie dans la cellule par Fritz Albert Lipmann en 1941.
PROPRIETES physiques et chimiques
ATP consiste en ad??nosine - lui-m??me compos?? d'un anneau de l'ad??nine et un ribose sucre - et trois des groupes phosphate (triphosphate). Les groupes phosphoryle, en commen??ant par le groupe le plus proche du ribose, sont d??sign??s sous le nom de alpha (α), b??ta (β) et gamma (γ) phosphates. L'ATP est hautement soluble dans l'eau et est tr??s stable dans des solutions entre pH 6.8 ?? 7.4, mais est rapidement hydrolys?? ?? pH extr??me. Par cons??quent, l'ATP est le meilleur stock??e en tant que sel anhydre.
L'ATP est une mol??cule instable et tend ?? ??tre hydrolys??e dans l'eau. Si l'ATP et ADP sont en ??quilibre chimique , la quasi-totalit?? de l'ATP est converti en ADP. Tout syst??me qui est loin de l'??quilibre contient ??nergie potentielle, et est capable de faire le travail . Cellules biologiques maintenir le rapport de l'ATP en ADP ?? un point dix ordres de grandeur de l'??quilibre, avec des concentrations plus ??lev??es ATP mille fois que la concentration d'ADP. Ce d??placement de l'??quilibre signifie que l'hydrolyse de l'ATP dans la cellule lib??re une grande quantit?? d'??nergie. L'ATP est commun??ment appel?? une ??mol??cule de haute ??nergie??; mais ce est incorrect, comme un m??lange de l'ATP et de l'ADP ?? l'??quilibre dans l'eau ne peut pas faire un travail utile ?? tous. ATP ne contient pas ??obligations de haute ??nergie??, et toute autre mol??cule instable servirait aussi bien comme un moyen de stocker l'??nergie, si la cellule a maintenu sa concentration loin de l'??quilibre.
La quantit?? d'??nergie lib??r??e peut ??tre calcul?? ?? partir des variations de l'??nergie dans des conditions non naturelles. La variation nette de l'??nergie thermique ( enthalpie ) au la temp??rature et la pression de la d??composition de l'ATP ??talon dans hydrat??e ADP et de phosphate inorganique hydrat?? est -20,5 kJ / mol, avec un changement de ??nergie libre de 3,4 kJ / mol. L'??nergie lib??r??e par clivage soit un phosphate (Pi) ou de pyrophosphate (PPi) unit?? de l'ATP, avec tous les r??actifs et les produits lors de leur ??tats standard de 1 M concentration, sont:
- ATP + H 2 O → ADP (hydrat??) + Pi (hydrat??) + H + (hydrat??) AG = -30,54 kJ / mol (-7,3 kcal / mole)
- ATP + H 2 O → AMP (hydrat??) + PPi (hydrat??) + H + (hydrat??) AG = -45,6 kJ / mol (-10,9 kcal / mole)
Ces valeurs peuvent ??tre utilis??es pour calculer la variation de l'??nergie dans des conditions physiologiques et / ADP cellulaire ATP. Les valeurs indiqu??es pour l' ??nergie libre de Gibbs pour cette r??action d??pendent d'un certain nombre de facteurs, y compris la force ionique globale et la pr??sence de m??taux alcalino-terreux tels que les ions Mg 2+ et Ca 2+. Dans des conditions cellulaires typiques, Ag est d'environ -57 kJ / mol (-14 kcal / mole).
Ionisation dans les syst??mes biologiques
ATP a plusieurs groupes ionisables avec diff??rents constantes de dissociation acide. Dans une solution neutre, de l'ATP est ionis?? et existe principalement sous forme d'ATP ?? 4, avec une faible proportion de l'ATP 3-. Comme ATP a plusieurs groupes charg??s n??gativement en solution neutre, il peut m??taux ch??late avec une tr??s forte affinit??. Le constante de liaison pour diff??rents ions m??talliques sont (donn?? comme par mole) que Mg 2+ (9 554), Na + (13), Ca 2+ (3 722), K + (8), Sr 2+ (1 381) et Li + (25). En raison de la force de ces interactions, ATP existe dans la cellule la plupart du temps dans un complexe avec Mg 2+.
Biosynth??se
L'ATP concentration ?? l'int??rieur de la cellule est typiquement de 1 ?? 10 mM. ATP peut ??tre produit par r??actions d'oxydo-r??duction ?? l'aide de simples et complexes sucres ( glucides ) ou les lipides comme source d'??nergie. Pour l'ATP pour ??tre synth??tis?? ?? partir de combustibles complexes, ils doivent d'abord ??tre d??compos??s en leurs ??l??ments de base. Les glucides sont hydrolys?? en sucres simples, comme le glucose et fructose. Graisses ( triglyc??rides) sont m??tabolis??s pour donner des acides gras et glyc??rol.
L'ensemble du processus d'oxyder le glucose en dioxyde de carbone est connu comme la respiration cellulaire et peut produire jusqu'?? 36 mol??cules d'ATP ?? partir d'une seule mol??cule de glucose. ATP peut ??tre produit par un certain nombre de processus cellulaires distinctes; les trois voies principales utilis??s pour produire de l'??nergie dans les eucaryotes sont les organismes et la glycolyse cycle de l'acide citrique / la phosphorylation oxydative, les deux composantes de respiration cellulaire; et b??ta-oxydation. La majorit?? de cette production d'ATP par un non- photosynth??tique eucaryote a??robie a lieu dans la mitochondrie , qui peut faire jusqu'?? pr??s de 25% du volume total d'une cellule typique.
Glycolyse
Dans la glycolyse, le glucose et le glyc??rol sont m??tabolis??s en pyruvate via la voie glycolytique. Dans la plupart des organismes de ce processus se produit dans le cytosol, mais dans certains protozoaires comme le kin??toplastides, cela est effectu?? dans un sp??cialis?? organite appel?? le glycosome. Glycolyse g??n??re un net deux mol??cules d'ATP par substrat phosphorylation catalys??e par deux enzymes: PGK et la pyruvate kinase. Deux mol??cules de NADH sont ??galement produits, qui peut ??tre oxyd?? par le cha??ne de transport d'??lectrons et en r??sultat la g??n??ration d'ATP suppl??mentaire par ATP synthase. Le pyruvate g??n??r?? en tant que produit final de la glycolyse est un substrat pour la Cycle de Krebs.
Cycle de l'acide citrique
Dans la mitochondrie , le pyruvate est oxyd?? par le complexe pyruvate d??shydrog??nase pour l'ac??tyl-CoA, qui est enti??rement oxyd??e en dioxyde de carbone par cycle de l'acide citrique (??galement connu sous le nom de cycle de Krebs). Chaque "tour" du cycle de l'acide citrique produit deux mol??cules de dioxyde de carbone , une mol??cule de l'??quivalent ATP la guanosine triphosphate (GTP) ?? travers la phosphorylation au niveau du substrat, catalys??e par succinyl CoA synth??tase, trois mol??cules de la r??duction coenzyme NADH, et une mol??cule de la coenzyme r??duite FADH 2. Ces deux derni??res mol??cules sont recycl??s ?? leur ??tat oxyd?? (NAD + et FAD, respectivement) par l'interm??diaire du cha??ne de transport d'??lectrons, qui g??n??re plus d'ATP par la phosphorylation oxydative. L'oxydation d'une mol??cule de NADH conduit ?? la synth??se de l'ordre de trois mol??cules d'ATP, et l'oxydation de l'une FADH 2 donne environ deux mol??cules d'ATP. La majorit?? de l'ATP cellulaire est g??n??r?? par ce processus. Bien que le cycle de l'acide citrique ne implique pas elle-m??me mol??culaire oxyg??ne , ce est un obligatoirement processus a??robie parce O 2 est n??cessaire pour recycler le NADH r??duite et FADH 2 ?? leurs ??tats d'oxydation. En l'absence d'oxyg??ne du cycle de acide citrique cessera de fonctionner en raison de l'absence de disposition NAD + et FAD.
La production d'ATP par la mitochondrie de NADH cytosolique repose sur la navette malate-aspartate (et dans une moindre mesure, la navette glyc??rol-phosphate), car la membrane mitochondriale interne est imperm??able aux NADH et NAD +. Au lieu de transf??rer le NADH g??n??r??, un malate convertis de l'enzyme de d??shydrog??nase oxaloac??tate ?? malate, qui est transport?? vers la matrice mitochondriale. Une autre r??action de d??shydrog??nase de malate catalys??e se produit dans la direction oppos??e, produisant l'oxaloac??tate et du NADH ?? partir du malate de nouveau transport?? magasin et l'int??rieur de la mitochondrie de NAD +. Un convertit l'oxaloac??tate transaminase ?? aspartate pour le transport en arri??re ?? travers la membrane et dans l'espace intermembranaire.
Dans la phosphorylation oxydative, le passage des ??lectrons ?? partir de NADH et FADH 2 par les puissances de la cha??ne de transport d'??lectrons le pompage de protons de la matrice mitochondriale et dans l'espace intermembranaire. Cela cr??e un force motrice de protons qui est l'effet net d'un gradient de pH et un gradient de potentiel ??lectrique ?? travers la membrane mitochondriale interne. Flux de protons dans cette gradient de potentiel - ce est, de l'espace intermembranaire ?? la matrice - fournit la force motrice pour la synth??se d'ATP par ATP synthase. Cette enzyme contient une sous-unit?? de rotor qui tourne physiquement par rapport aux parties statiques de la prot??ine au cours de la synth??se d'ATP.
La plupart de l'ATP synth??tis?? dans les mitochondries sera utilis?? pour les processus cellulaires dans le cytosol; il doit donc ??tre export?? ?? partir de son site de synth??se dans la matrice mitochondriale. La membrane interne contient une antiporteur, la translocase ADP / ATP, qui est un prot??ine membranaire int??grale utilis?? pour ??changer nouvellement synth??tis?? ATP en ADP de la matrice dans l'espace intermembranaire. Cette translocase est entra??n?? par le potentiel de membrane, tel qu'il r??sulte du mouvement de l'ordre de 4 charges n??gatives de la membrane mitochondriale en ??change de trois charges n??gatives d??plac??s ?? l'int??rieur. Cependant, il est ??galement n??cessaire de transporter le phosphate dans la mitochondrie; le support de phosphate se d??place avec un proton dans chaque phosphate, partiellement dissiper le gradient de protons.
Le b??ta-oxydation
Les acides gras peuvent ??galement ??tre d??compos??s l'ac??tyl-CoA par b??ta-oxydation. Chaque tour de ce cycle r??duit la longueur de la cha??ne acyle par deux atomes de carbone et produit une NADH et FADH 2 une mol??cule, qui sont utilis??s pour g??n??rer l'ATP par phosphorylation oxydative. Parce que NADH et FADH 2 sont des mol??cules riches en ??nergie, des dizaines de mol??cules d'ATP peuvent ??tre g??n??r??s par la b??ta-oxydation d'une seule longue cha??ne acyle. Le rendement ??nerg??tique ??lev?? de ce processus et le stockage de la graisse compacte expliquent pourquoi il est la source la plus dense de l'alimentation calories.
La respiration ana??robie
La respiration ana??robie ou fermentation entra??ne la production d'??nergie par le proc??d?? de oxydation en l'absence de O 2 en tant que accepteur d'??lectrons. Dans la plupart des eucaryotes, le glucose est utilis?? ?? la fois comme un accumulateur d'??nergie et d'un donneur d'??lectrons. L'??quation de l'oxydation du glucose ?? l'acide lactique est:
- C 6 H 12 O 6
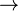 2CH 3 CH (OH) COOH + 2 ATP
2CH 3 CH (OH) COOH + 2 ATP
Chez les procaryotes, des accepteurs d'??lectrons multiples peuvent ??tre utilis??s dans la respiration ana??robie. Ceux-ci comprennent le nitrate , le sulfate ou le dioxyde de carbone. Ces proc??d??s conduisent ?? des processus ??cologiquement importants de d??nitrification, la r??duction du sulfate et ac??tog??n??se, respectivement.
ATP par reconstitution nucl??oside diphosphate kinases
ATP peut ??galement ??tre synth??tis?? par plusieurs r??actions dites "reconstitution" catalys??es par les familles d'enzymes de nucl??osides kinases diphosphate (NDKs), qui utilisent d'autres nucl??osides triphosphates comme un donneur de phosphate ?? haute ??nergie, et l'ATP: la famille guanido-phosphotransf??rase, qui utilise cr??atine.
- ADP + GTP
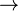 ATP + PIB
ATP + PIB
La production d'ATP lors de la photosynth??se
Chez les plantes, l'ATP est synth??tis?? par membrane des thylako??des de la pendant le chloroplaste r??actions d??pendant de la lumi??re de la photosynth??se dans un processus appel?? photophosphorylation. Ici, l'??nergie lumineuse est utilis??e pour pomper des protons ?? travers la membrane des chloroplastes. Cela produit une force proton-motrice et cela entra??ne l'ATP synthase, exactement comme dans la phosphorylation oxydative. Une partie de l'ATP produit dans les chloroplastes est consomm??e dans la Cycle de Calvin, qui produit trioses sucres.
ATP recyclage
La quantit?? totale d'ATP dans le corps humain est d'environ 0,1 taupe. La majorit?? de l'ATP ne est pas habituellement synth??tis?? de novo, mais est g??n??r?? ?? partir d'ADP par les proc??d??s mentionn??s ci-dessus. Ainsi, ?? un moment donn??, le montant total de l'ATP + ADP reste assez constante.
L'??nergie utilis??e par les cellules humaines n??cessite la hydrolyse de 100 ?? 150 moles d'ATP par jour ce qui est autour de 50 ?? 75 kg. Typiquement, un humain va utiliser leur poids corporel de l'ATP au cours de la journ??e. Cela signifie que chaque mol??cule d'ATP est recycl?? 1000 ?? 1500 fois au cours d'une seule journ??e (100 / 0,1 = 1,000). ATP ne peut pas ??tre stock??e, et donc sa consommation suit de pr??s sa synth??se.
R??gulation de la biosynth??se
La production d'ATP dans une cellule eucaryote a??robie est ??troitement r??gul??e par des m??canismes allost??riques, par effets de r??troaction, et de la d??pendance ?? la concentration de substrat d'enzymes individuels dans les glycolyse et d'oxydation voies de phosphorylation. Principaux points de contr??le se produisent dans les r??actions enzymatiques qui sont si ??nerg??tiquement favorable qu'ils sont irr??versibles dans des conditions physiologiques.
Dans la glycolyse, hexokinase est directement inhib??e par son produit, la glucose-6-phosphate, et la pyruvate kinase est inhib??e par l'ATP lui-m??me. Le point de contr??le principal de la glycolyse est phosphofructokinase (PFK), qui est allost??rique inhib??e par des concentrations ??lev??es d'ATP et activ?? par des concentrations ??lev??es d'AMP. L'inhibition de la PFK de l'ATP est inhabituelle, car l'ATP est ??galement un substrat pour la r??action catalys??e par la PFK; la forme biologiquement active de l'enzyme est une t??tram??re qui existe dans deux conformations possibles, dont un seul, qui se lie au second substrat fructose-6-phosphate (F6P). La prot??ine a deux sites de fixation ?? l'ATP - le site actif est accessible dans chaque conformation de la prot??ine, mais la liaison ?? l'ATP sur le site de l'inhibiteur stabilise la conformation qui se lie faiblement F6P. Un certain nombre d'autres petites mol??cules peut compenser le d??calage induit par l'ATP en ??quilibre conformation et r??activer PFK, y compris AMP cyclique, des ions ammonium, phosphate inorganique, et le fructose biphosphate 1,6 et 2,6.
Le cycle de l'acide citrique est r??gul??e principalement par la disponibilit?? des substrats cl??s, en particulier le rapport de NAD + en NADH et les concentrations de calcium , phosphate inorganique, ATP, ADP, AMP et. Citrate - la mol??cule qui donne son nom au cycle - est un inhibiteur de r??troaction citrate synthase et inhibe ??galement PFK, fournissant un lien direct entre la r??gulation du cycle de l'acide citrique et la glycolyse.
Dans la phosphorylation oxydative, le point de contr??le cl?? est la r??action catalys??e par cytochrome c oxydase, qui est r??glement??e par la disponibilit?? de son substrat-forme r??duite de cytochrome c. Le montant de la r??duction du cytochrome c disponibles est directement li?? aux quantit??s d'autres substrats:
ce qui implique directement l'??quation suivante:
Ainsi, un ratio ??lev?? de [NADH] pour [NAD +] ou un faible ratio de [ADP] [P i] pour [ATP] impliquent une grande quantit?? de cytochrome c r??duit et un niveau ??lev?? de l'activit?? du cytochrome c oxydase. Un niveau suppl??mentaire de r??gulation est introduit par les tarifs de transport de l'ATP et NADH entre la matrice mitochondriale et le cytoplasme.
Fonctionne dans les cellules
ATP est g??n??r?? dans la cellule par des proc??d??s consommant de l'??nergie et est d??compos??e par des processus de lib??ration d'??nergie. De cette fa??on ATP transf??re l'??nergie entre spatialement s??par??e r??actions m??taboliques. L'ATP est la principale source d'??nergie pour la majorit?? des fonctions cellulaires. Cela comprend la synth??se de macromol??cules, y compris ADN, ARN, et prot??ines. ATP joue ??galement un r??le essentiel dans le transport des macromol??cules ?? travers les membranes cellulaires, par exemple, exocytose et endocytose.
Dans la synth??se du acide nucl??ique L'ARN, l'ATP est l'un des quatre nucl??otides incorpor??s directement dans des mol??cules d'ARN par ARN polym??rases. L'??nergie motrice cette polym??risation vient de cliver un pyrophosphate (deux groupes phosphate). Le processus est similaire ?? la biosynth??se de l'ADN, sauf que l'ATP est r??duit ?? la d??soxyribonucl??otide dATP, avant l'incorporation dans l'ADN.
L'ATP est impliqu??e de mani??re critique dans le maintien de la structure cellulaire en facilitant le montage et le d??montage des ??l??ments de la cytosquelette. Dans un proc??d?? apparent??, l'ATP est requis pour la raccourcissement des filaments d'actine et de myosine ponts transversaux n??cessaires ?? la contraction musculaire. Ce dernier proc??d?? est l'une des principales exigences ??nerg??tiques des animaux et est essentiel pour locomotion et la respiration.
Signalisation cellulaire
Signalisation extracellulaire
L'ATP est ??galement un mol??cule de signalisation. ATP, ADP, ou ad??nosine sont reconnus par r??cepteurs purinergiques.
Chez l'homme, ce r??le de signalisation est important ?? la fois dans le syst??me nerveux central et p??riph??rique. D??pendant de l'activit?? lib??ration de l'ATP ?? partir synapses, les axones et les cellules gliales active les r??cepteurs membranaires appel??es purinergiques P2. Les r??cepteurs P2Y sont m??tabotropique, ?? savoir Coupl??s aux prot??ines G et modulent principalement taux d'AMP parfois cycliques calcium intracellulaire et. Quinze membres de la famille de P2Y ont ??t?? rapport??s (P2Y1-P2Y15), m??me si certains ne sont li??s par le biais faible homologie et plusieurs (P2Y5, P2Y7, P2Y9, P2Y10) ne fonctionnent pas comme des r??cepteurs qui soul??vent calcium cytosolique. Le r??cepteur P2X ionotropique sous-groupe compos?? de sept membres (P2X1-P2X7) qui sont Ca 2+ canaux ioniques -permeable ligand-d??pendants qui se ouvrent lorsque li?? ?? un nucl??otide purine extracellulaire. Contrairement aux r??cepteurs P2 (ordre agoniste ATP> ADP> AMP> ADO), purinergique nucl??otides comme ATP ne sont pas fortes agonistes des r??cepteurs P1 qui sont fortement activ??es par ad??nosine et d'autres nucl??osides (ADO> AMP> ADP> ATP). R??cepteurs P1 ont A1, A2a, A2b et A3 sous-types ("A" comme un vestige de l'ancienne nomenclature des r??cepteurs de l'ad??nosine), qui sont tous des G r??cepteurs coupl??s aux prot??ines, A1 et A3 ??tant coupl?? ?? Gi, et A2a et A2b ??tre coupl?? ?? Gs.
Signalisation intracellulaire
L'ATP est critique dans processus de transduction du signal. Il est utilis?? par kinases en tant que source de groupes phosphate dans les r??actions de transfert de phosphate. L'activit?? de kinase sur des substrats tels que des prot??ines ou des lipides membranaires sont une forme courante de transduction du signal. La phosphorylation d'une prot??ine par une kinase peut activer cette cascade tel que le mitogen-activated protein kinase cascade.
ATP est ??galement utilis?? par l'ad??nylate cyclase et est transform?? en le second messager de l'AMP cyclique mol??cule, qui est impliqu?? dans le d??clenchement de signaux de calcium par la lib??ration de calcium des r??serves intracellulaires. Cette forme de la transduction du signal est particuli??rement important dans le fonctionnement du cerveau, m??me si elle est impliqu??e dans la r??gulation d'une multitude d'autres processus cellulaires.
Synth??se d??soxyribonucl??otide
Dans tous les organismes connus, les d??soxyribonucl??otides qui forment ADN sont synth??tis??s par l'action de ribonucl??otide r??ductase (RNR) enzymes sur leurs ribonucl??otides correspondantes. Cette enzyme r??duit la 2 ' un groupe hydroxyle sur le sucre ribose ?? d??soxyribose, formant un d??soxyribonucl??otide (not??e dATP). Toutes les enzymes de la ribonucleotide reductase utilisent une commune sulfhydryle m??canisme radicalaire tributaire r??active r??sidus de cysteine qui se oxydent pour former des liaisons disulfure dans le cours de la r??action. Enzymes RBR sont recycl??s par r??action avec thior??doxine ou glutar??doxine.
La r??gulation des enzymes apparent??es RNR et maintient un ??quilibre de dNTP par rapport ?? l'autre et par rapport ?? la cellule dans PNT. Tr??s bas le dNTP inhibe de concentration la synth??se d'ADN et r??paration de l'ADN et est l??tale pour la cellule, tandis qu'un rapport de dNTP est anormal mutag??ne en raison de la probabilit?? accrue de la ADN polym??rase incorporant le mauvais dNTP pendant la synth??se de l'ADN. R??glement ou diff??rentielle sp??cificit?? de RNR a ??t?? propos??e comme un m??canisme pour les modifications dans la taille relative des pools de dNTP intracellulaires sous stress cellulaire tels que hypoxie.
La liaison aux prot??ines

Certaines prot??ines qui se lient ?? l'ATP faire d'une caract??ristique pliage de la prot??ine connue sous le nom Rossmann pliage, qui est un g??n??ral nucl??otide contraignant domaine structural qui peut ??galement lier le cofacteur NAD. Les prot??ines de liaison ATP plus courantes, connues sous le nom kinases, part un petit nombre de plis communes; la prot??ines kinases, la plus grande superfamille de la kinase, les caract??ristiques structurelles communes de part sp??cialis??s pour la liaison de l'ATP et le transfert de phosphate.
ATP dans des complexes avec des prot??ines n??cessite g??n??ralement la pr??sence d'un divalent cation , presque toujours magn??sium , qui se lie aux groupes phosphate de l'ATP. La pr??sence de magn??sium diminue fortement la constante de dissociation de l'ATP ?? partir de son partenaire de liaison de prot??ine sans affecter la capacit?? de l'enzyme ?? catalyser la r??action une fois que l'ATP est li??. La pr??sence d'ions magn??sium peut servir de m??canisme de r??gulation de la kinase.
Analogues de l'ATP
laboratoires de biochimie utilisent souvent des ??tudes in vitro pour explorer les processus mol??culaires d??pendant de l'ATP. Les inhibiteurs enzymatiques d'enzymes ATP-d??pendants tels que kinases sont n??cessaires pour examiner la des sites de liaison et ??tats de transition impliqu??s dans les r??actions d??pendant de l'ATP. Analogues de l'ATP sont ??galement utilis??s dans Cristallographie aux rayons X pour d??terminer une la structure des prot??ines dans un complexe avec l'ATP, souvent avec d'autres substrats. Analogues de l'ATP plus utiles ne peuvent pas ??tre hydrolyse comme ATP serait; ?? la place ils emprisonnent l'enzyme dans une structure ??troitement li??e ?? l'??tat li??e ?? l'ATP. L'ad??nosine 5 '- (gamma-thiotriphosphate) est un analogue de l'ATP extr??mement commun dans lequel l'un des atomes d'oxyg??ne gamma-phosphate est remplac?? par un soufre atome; cette mol??cule est hydrolys?? ?? un taux consid??rablement plus lent que lui-m??me ATP et fonctionne comme un inhibiteur des processus d??pendant de l'ATP. Dans les ??tudes cristallographiques, ??tats de transition d'hydrolyse sont mod??lis??s par la borne ions vanadate. Toutefois, la prudence se impose dans l'interpr??tation des r??sultats d'exp??riences utilisant analogues de l'ATP, puisque certaines enzymes peuvent les hydrolyser ?? des taux appr??ciables ?? forte concentration.

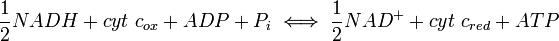
![\ Frac {~ cyt c_ {red}} {~ cyt c_ {}} boeuf = \ left (\ frac {[NADH]} {[NAD] ^ {+}} \ right) ^ {\ frac {1} {2 }} \ left (\ frac {[ADP] [P_ {i}]} {[ATP]} \ right) K_ {eq}](../../images/131/13158.png)
