
Nitrate
Contexte des ??coles Wikip??dia
SOS croit que l'??ducation donne une meilleure chance dans la vie des enfants dans le monde en d??veloppement aussi. Voulez-vous savoir sur le parrainage? Voir www.sponsorachild.org.uk
| Nitrate | |
|---|---|
 | |
 |  |
Nitrate | |
| Propri??t??s | |
| Formule mol??culaire | NO - 3 |
| Masse molaire | 62,0049 g mol -1 |
| Sauf indication contraire, les donn??es sont donn??es pour le mat??riel dans leur ??tat standard (?? 25 ?? C, 100 kPa) | |
| R??f??rences d'Infobox | |
Le nitrate est un ion polyatomique avec la formule mol??culaire est NO 3 - et une masse mol??culaire de 62,0049 g / mol. Nitrates d??crivent ??galement l'organique groupe fonctionnel RONO 2. Ces esters nitrates sont une classe sp??cialis??e d'explosifs.
Structure
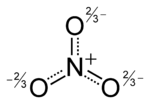
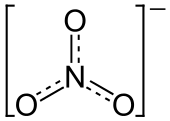
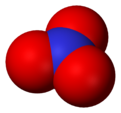
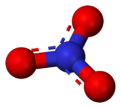
L'anion est de la la base conjugu??e d' acide nitrique , constitu??e d'une centrale azote atome entour?? de trois atomes d'oxyg??ne li??s de fa??on identique dans un agencement plan trigonal. L'ion nitrate porte un accusation formelle de -1. Ceci r??sulte d'une accusation formelle de combinaison dans laquelle chacun des trois oxyg??nes porte un - 2/3 accusation, alors que l'azote porte une charge 1, tous ces ajouter jusqu'?? accusation formelle de l'ion de nitrate polyatomique. Cet agencement est commun??ment utilis?? comme un exemple de r??sonance. Comme le iso??lectronique carbonate ions, l'ion nitrate peut ??tre repr??sent?? par les structures de r??sonance:

Propri??t??s

Presque tous les sels de nitrate inorganique sont solubles dans l'eau ?? temp??rature et pression normales. Un exemple commun d'un sel de nitrate inorganique est le nitrate de potassium (salp??tre).
Occurrence
Sels de nitrate se trouvent naturellement sur la terre comme de grands gisements, en particulier des Chili salp??tre une source majeure de nitrate de sodium.
Les nitrites sont produits par un certain nombre d'esp??ces de nitrifiantes bact??ries, et les compos??s de nitrate pour la poudre (voir ce sujet pour plus) ont ??t?? produites historiquement, en l'absence de sources de nitrates min??raux, au moyen de diverses proc??d??s de fermentation ?? l'aide de l'urine et les excr??ments.
Utilisations
Les nitrates sont produits principalement comme engrais dans l'agriculture en raison de leur grande solubilit?? et la biod??gradabilit??. Les principaux sont les nitrates d'ammonium, de sodium, de potassium, et les sels de calcium. Plusieurs millions de kilogrammes sont produits chaque ann??e ?? cette fin.
D'autres utilisations
La deuxi??me application importante de nitrates comme agents oxydants, notamment en mati??re d'explosifs, o?? l'oxydation rapide de compos??s de carbone lib??re de grandes quantit??s de gaz (voir Gunpowder pour un exemple). Le nitrate de sodium est utilis?? pour ??liminer les bulles d'air ?? partir de verre fondu et certaines c??ramiques. Des m??langes de sel fondu sont utilis??s pour durcir certains m??taux.
D??tection
Ions nitrate libre en solution peuvent ??tre d??tect??s par un nitrate ??lectrode s??lective d'ions. Ces ??lectrodes analogue ?? l'??lectrode de pH s??lective. Cette r??ponse est en partie d??crit par la ??quation de Nernst.
Toxicit??
Toxicose
Nitrate intoxication peut se produire par m??tabolisme ent??ro-h??patique du nitrate en nitrite ??tant un interm??diaire. Nitrites oxyder les fer atomes dans h??moglobine ?? partir de ferreux fer (2+) ?? fer ferrique (3+), le rendant incapable de transporter l'oxyg??ne. Ce processus peut conduire ?? g??n??ralis?? le manque d'oxyg??ne dans les tissus d'organes et une condition dangereuse appel??e m??th??moglobin??mie. Bien que le nitrite est converti en ammoniac , se il ya plus de nitrite peut ??tre converti, l'animal souffre d'un manque lentement de l'oxyg??ne.
Effets sur la sant?? humaine
Les ??tres humains sont soumis ?? la toxicit?? du nitrate, avec les nourrissons ??tant particuli??rement vuln??rables ?? la m??th??moglobin??mie due ?? m??taboliser le nitrate triglyc??rides pr??sents ?? des concentrations sup??rieures ?? d'autres stades de d??veloppement. M??th??moglobin??mie chez les nourrissons est connu comme syndrome du b??b?? bleu. Bien que les nitrates dans l'eau potable ont ??t?? autrefois consid??r??es comme un facteur contributif, il ya maintenant des doutes scientifiques importantes quant ?? savoir se il existe un lien de causalit??. Le syndrome du b??b?? bleu est maintenant consid??r??e comme le produit d'un certain nombre de facteurs, qui peuvent inclure tout facteur qui provoque des troubles gastriques, comme une infection diarrh??ique, intol??rance aux prot??ines, toxicit?? des m??taux lourds, etc., avec des nitrates jouant un r??le mineur. Nitrates, si un facteur dans un cas particulier, serait le plus souvent ??tre ing??r?? par les nourrissons dans l'eau potable ??lev??e en nitrates. Toutefois, l'exposition du nitrate peut ??galement se produire si l'alimentation, par exemple, les l??gumes contenant des niveaux ??lev??s de nitrate. Laitue peut contenir ??lev??s de nitrate dans des conditions de croissance tels que la lumi??re du soleil r??duite, de la p??nurie de molybd??ne micronutriments essentiels (Mo) et le fer (Fe), ou des concentrations ??lev??es de nitrates en raison de l'assimilation r??duite de nitrate dans l'usine. Des niveaux ??lev??s de fertilisation azot??e contribuent ??galement ?? des niveaux ??lev??s de nitrate dans la plante r??colt??e.
Certains adultes peuvent ??tre plus sensibles aux effets de nitrate que d'autres. Le m??th??moglobine r??ductase enzyme peut ??tre sous-produit ou absents chez certaines personnes qui ont une mutation h??r??ditaire. Ces personnes ne peuvent pas briser m??th??moglobine aussi rapidement que ceux qui ont l'enzyme, conduisant ?? des taux circulants accrus de m??th??moglobine (l'implication ??tant que leur sang ne est pas aussi riche en oxyg??ne). Ceux avec de l'acide de l'estomac insuffisante (y compris certains v??g??tariens et les v??g??taliens) peuvent ??galement ??tre ?? risque. Ce est l'augmentation de la consommation de l??gumes verts ?? feuilles qui accompagnent g??n??ralement ces types de r??gimes peuvent entra??ner une augmentation de l'apport de nitrate. Une grande vari??t?? de conditions m??dicales, y compris les allergies alimentaires, l'asthme, l'h??patite et les calculs biliaires peuvent ??tre li??s ?? l'acide gastrique faible; ces personnes peuvent ??galement ??tre tr??s sensibles aux effets de nitrate.
M??th??moglobin??mie peut ??tre trait??e avec le bleu de m??thyl??ne, ce qui r??duit le fer ferrique (3+) dans les globules affect??es arri??re en fer ferreux (2 +).
Toxicit?? Marine
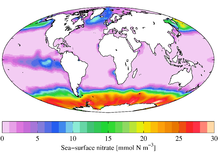
En eau douce ou syst??mes estuariens proches ?? la terre, le nitrate peuvent atteindre des niveaux ??lev??s qui peuvent causer la mort des poissons. Bien que le nitrate est beaucoup moins toxique que l'ammoniac, des niveaux plus de 30 ppm de nitrate peut inhiber la croissance, alt??rent le syst??me immunitaire et provoquent un stress chez certaines esp??ces aquatiques. Toutefois, ?? la lumi??re des probl??mes inh??rents aux protocoles derni??res sur exp??riences de toxicit?? aigu?? de nitrate, la mesure de la toxicit?? des nitrates a ??t?? l'objet d'un d??bat r??cent.
Dans la plupart des cas, des concentrations de nitrates en exc??s dans les syst??mes aquatiques, la principale source est ruissellement provenant agricoles ou de surface paysagers zones qui ont re??u des engrais de nitrate exc??s. Cela se appelle eutrophisation et peut conduire ?? la prolif??ration d'algues. En plus de diriger ?? l'eau anoxie et zones mortes, ces fleurs peuvent causer d'autres changements ?? fonction de l'??cosyst??me, en favorisant certains groupes d'organismes sur les autres. En cons??quence, comme le nitrate forme un composant de les solides dissous totaux, ils sont largement utilis??s comme un indicateur de qualit?? de l'eau.
Le nitrate est ??galement un sous-produit de fosses septiques. Pour ??tre plus pr??cis, ce est une substance chimique naturelle qui est ?? gauche apr??s la rupture ou de la d??composition des d??chets animaux ou humains. Qualit?? de l'eau peut ??galement ??tre affect??e par des ressources d'eaux souterraines qui ont un grand nombre de syst??mes septiques dans un bassin versant. Fosses septiques lixiviation vers le bas dans les ressources en eaux souterraines ou des aquif??res et approvisionnement plans d'eau environnants. Lacs qui se appuient sur les eaux souterraines sont souvent affect??es par la nitrification ?? travers ce processus.
Nitrate dans l'eau potable ?? des niveaux sup??rieurs ?? la norme nationale constitue une menace imm??diate pour les jeunes enfants. Des niveaux excessifs peuvent entra??ner une condition connue sous le nom " syndrome du b??b?? bleu ??. Si non trait??e, la maladie peut ??tre fatale. Faire bouillir l'eau contamin??e avec du nitrate augmente la concentration de nitrate et le risque potentiel.
Toxicit?? nitrates dans l'??levage
Intoxication par les nitrates est une pr??occupation pour les producteurs de bovins essentiellement, mais aussi pour d'autres producteurs ruminants. Le nitrate est naturellement consomm??e par la culture de plantes; Toutefois, lorsque la croissance est interrompue, les racines des plantes continueront ?? prendre le nitrate du sol, et ?? moins que la nouvelle croissance des plantes se produit, le nitrate se accumulent. Ainsi, la r??colte apr??s les r??sultats de l'accumulation de nitrates dans une culture qui est riche en nitrates. Les facteurs qui peuvent causer une accumulation de nitrates dans les plantes sont le gel, la gr??le, la s??cheresse, les vents chauds et secs, les d??g??ts des pesticides, herbicides et dommages de toute autre plante rabougrissement des causes environnementales.
Les sympt??mes de l'empoisonnement par les nitrates comprennent une augmentation de la fr??quence cardiaque et de la respiration; dans les cas avanc??s sang et les tissus peuvent prendre une couleur bleu ou brun. RSS peut ??tre test?? pour les nitrates; traitement consiste en compl??ment ou en remplacement des fournitures existantes avec du mat??riel de nitrate inf??rieur. Les niveaux de s??curit?? de nitrate pour divers types de b??tail sont les suivantes:
| Cat??gorie | NO 3% | % N-NO 3 | % KNO 3 | Effets |
|---|---|---|---|---|
| 1 | <0,5 | <0,12 | <0,81 | G??n??ralement sans danger pour les bovins de boucherie et les moutons |
| 2 | 0,5-1,0 | 0,12 ?? 0,23 | 0,81 ?? 1,63 | Attention - certains sympt??mes subcliniques peut appara??tre chez les chevaux, les moutons et les enceintes bovins de boucherie |
| 3 | 1.0 | 0,23 | 1,63 | Probl??mes ??lev??es de nitrates - les pertes de la mort et les avortements peuvent se produire chez les bovins et les moutons |
| 4 | <1,23 | <0,28 | <2,00 | Niveau de s??curit?? maximum pour les chevaux. Ne pas nourrir les fourrages ??lev??s de nitrate ?? juments enceintes |
Les valeurs sont au-dessus sur un (humidit?? libre) base s??che.
Aper??u Nitrate
| HNO 3 | Il | |||||||||||||||||
| LiNO 3 | Soyez (NO 3) 2 | B (NO 3) 3 | C | N | O | Fa | Ne | |||||||||||
| NaNO 3 | Mg (NO 3) 2 | Al (NO 3) 3 | Si | P | S | ClONO 2 | Ar | |||||||||||
| KNO 3 | Ca (NO 3) 2 | Sc (NO 3) 3 | Ti | V | Cr (NO 3) 3 | Mn (NO 3) 2 | Fe (NO 3) 3 | Co (NO 3) 2 | Ni (NO 3) 2 | Cu (NO 3) 2 | Zn (NO 3) 2 | G??orgie | Ge | Comme | Se | Br | Kr | |
| RbNO 3 | Sr (NO 3) 2 | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd (NO 3) 2 | AgNO 3 | Cd (NO 3) 2 | En | Sn | Sb | Te | CI | Xe | |
| CsNO 3 | Ba (NO 3) 2 | Hf | Ta | W | R?? | Os | Ir | Pt | Au | Hg (NO 3) 2 | Tl | Pb (NO 3) 2 | Bi | Po | ?? | Rn | ||
| Fr | Ra | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Uub | Uut | Uuq | Uup | Uuh | Uus | Uuo | ||
| ↓ | ||||||||||||||||||
| La | Ce | Pr | Dakota du Nord | Pm | Sm | Ue | Gd (NO 3) 3 | Tb | Dy | Ho | Er | Tm | YB | Lu | ||||
| Un C | Th | Pennsylvanie | UO 2 (NO 3) 2 | Np | Pu | Suis | Cm | Bk | Cf | Es | Fm | Md | Aucun | Lr | ||||
