
La química inorgánica
Antecedentes de las escuelas de Wikipedia
Esta selección wikipedia ha sido elegido por los voluntarios que ayudan Infantil SOS de Wikipedia para esta Selección Wikipedia para las escuelas. SOS Children ha cuidado de niños en África durante cuarenta años. ¿Puedes ayudar a su trabajo en África ?
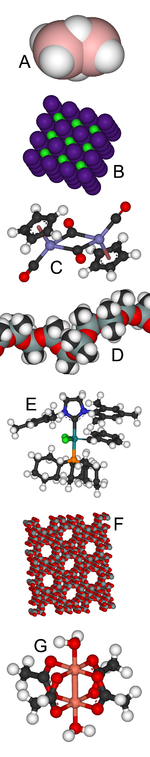
A: Características diborano unión inusual
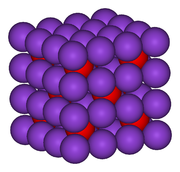
B: De cloruro de cesio tiene un arquetipo estructura cristalina
C: Fp 2 es una complejo organometálico
D: Usos de silicona van desde los implantes mamarios a Plasticina
E: Catalizador de Grubbs 'ganó el Premio Nobel 2005 de su descubridor
F: Las zeolitas encuentran un uso extenso como tamices moleculares
G: Cobre (II) acetato sorprendido teóricos con su diamagnetism
La química inorgánica es la rama de la química que se trate con las propiedades y el comportamiento de los compuestos inorgánicos . Este campo cubre todos los compuestos químicos excepto los innumerables compuestos orgánicos (compuestos que contienen enlaces CH), que son los temas de la química orgánica . La distinción entre las dos disciplinas está lejos de ser absoluta, y hay mucha coincidencia, más importante en la subdisciplina de la la química organometálica.
Conceptos clave
La mayor parte de los compuestos inorgánicos se producen como sales , la combinación de cationes y aniones unidos por enlace iónico. Ejemplos de cationes son sodio Na +, y de magnesio Mg 2+ y ejemplos de aniones son óxido O 2- y cloruro Cl -. Como sales se carga neutra, estos iones forman compuestos tales como óxido de sodio Na 2 O o cloruro de magnesio MgCl 2. Los iones se describen por su estado de oxidación y su facilidad de formación se pueden deducir de la potencial de ionización (por cationes) o desde el afinidad electrónica (aniones) de los elementos primarios.
Clases importantes de compuestos inorgánicos son el óxidos, los carbonatos , los sulfatos y el haluros. Muchos compuestos inorgánicos se caracterizan por altos puntos de fusión . Las sales inorgánicas normalmente son pobres conductores en el estado sólido. Otra característica importante es su solubilidad en agua, por ejemplo (ver: diagrama de solubilidad), y la facilidad de cristalización. Cuando algunas sales (por ejemplo NaCl ) son muy solubles en agua, otros (por ejemplo, SiO 2 ) no lo son.
El más simple de reacción inorgánica es de desplazamiento doble, cuando en la mezcla de dos sales de los iones se intercambian sin un cambio en el estado de oxidación. En reacciones redox un reactivo, el oxidante, reduce su estado de oxidación y otro reactivo, el reductor, ha aumentado su estado de oxidación. El resultado neto es un intercambio de electrones . Intercambio de electrones puede ocurrir indirectamente, así, por ejemplo, en baterías, un concepto clave en electroquímica.
Cuando un reactante contiene átomos de hidrógeno, una reacción puede tener lugar mediante el intercambio de protones en la química ácido-base . En una definición más general, un ácido puede ser cualquier especie química capaces de unirse a pares de electrones se denomina una Ácido de Lewis; por el contrario cualquier molécula que tiende a donar un par de electrones se conoce como una Base de Lewis. Como un refinamiento de las interacciones ácido-base, la Teoría HSAB tiene en cuenta polarizabilidad y el tamaño de los iones.
Los compuestos inorgánicos se encuentran en la naturaleza como los minerales . El suelo puede contener sulfuro de hierro como la pirita o sulfato de calcio como yeso . Los compuestos inorgánicos se encuentran también multitarea como biomoléculas: como electrolitos ( cloruro de sodio ), en el almacenamiento de energía ( ATP ) o en la construcción (la backbone polifosfato en ADN ).
El primer compuesto inorgánico importante hecho por el hombre era nitrito de amonio para la fertilización del suelo a través de la Proceso de Haber. Los compuestos inorgánicos se sintetizan para su uso como catalizadores tales como vanadio (V) y óxido cloruro de titanio (III), o como reactivos en la química orgánica , tales como hidruro de litio y aluminio .
Las subdivisiones de la química inorgánica son la química organometálica, química cluster y química bioinorgánica. Estos campos son áreas activas de investigación en química inorgánica, dirigidos hacia nuevos catalizadores , los superconductores y terapias .
Química inorgánica Industrial
La química inorgánica es una zona muy práctica de la ciencia. Tradicionalmente, la escala de la economía de una nación podría ser evaluado por su productividad de ácido sulfúrico. Los 20 productos químicos inorgánicos fabricados en Canadá, China, Europa, Japón y los EE.UU. (datos de 2005): sulfato de aluminio, amoníaco , nitrato de amonio, sulfato de amonio, negro de carbono, cloro , ácido clorhídrico , de hidrógeno , peróxido de hidrógeno , ácido nítrico , nitrógeno , oxígeno , ácido fosfórico , carbonato de sodio, clorato de sodio, hidróxido de sodio , silicato de sodio, sulfato de sodio , ácido sulfúrico , y dióxido de titanio,
Química inorgánica descriptiva
Química inorgánica descriptiva se centra en la clasificación de los compuestos en función de sus propiedades. Parcialmente la clasificación se centra en la posición en la tabla periódica del elemento más pesado (el elemento con el mayor peso atómico) en el compuesto, en parte mediante la agrupación de compuestos por sus similitudes estructurales. Al estudiar los compuestos inorgánicos, es común encontrar partes de las diferentes clases de química inorgánica (un compuesto organometálico se caracteriza por su química de coordinación, y puede mostrar interesantes propiedades de estado sólido).
Diferentes clasificaciones son:
Compuestos de coordinación

Compuestos de coordinación clásicos cuentan con metales unidos a " pares solitarios de electrones "que residen en los principales grupos de átomos de ligandos tales como H 2 O, NH 3, Cl -, y CN -. En los compuestos de coordinación modernas casi todos los compuestos orgánicos e inorgánicos pueden ser utilizados como ligandos. El "metal" por lo general es un metal de los grupos de 3-13, así como los trans - lantánidos y trans - actínidos , pero desde un cierto punto de vista, todos los compuestos químicos puede ser descrito como complejos de coordinación.
La estereoquímica de los complejos de coordinación puede ser muy rica, como se insinuó en la separación de Werner de dos enantiómeros de [Co ((OH) 2 Co (NH3) 4) 3] 6+, una manifestación temprana de que la quiralidad no es inherente a los compuestos orgánicos. Un tema de actualidad dentro de esta especialización es la química supramolecular coordinación.
- Ejemplos: [Co ( EDTA)] -, [Co (NH 3) 6] 3+, TiCl 4 ( THF) 2.
Compuestos del grupo de principales

Estas especies incluyen elementos de grupos 1, 2 y 13-18 (excluyendo el hidrógeno) de la tabla periódica. Debido a su reactividad a menudo similares, los elementos en el grupo 3 ( Sc , Y , y La ) y el grupo 12 ( Zn , Cd y Hg ) están también generalmente incluidas.
Compuestos del grupo de principales se conocen desde los inicios de la química, por ejemplo elemental de azufre y el blanco destilable fósforo . Los experimentos en oxígeno, O 2 , por Lavoisier y Priestley no sólo identificó un importante gas diatómico, pero abrió el camino para la descripción de los compuestos y las reacciones de acuerdo con relaciones estequiométricas. El descubrimiento de una síntesis práctica de amoniaco usando catalizadores de hierro por Carl Bosch y Fritz Haber en la década de 1900 profundamente afectada la humanidad, lo que demuestra la importancia de la síntesis química inorgánica. Compuestos del grupo de principales típicos son SiO2, SnCl4, y N 2 O. Muchos compuestos del grupo principal también se pueden clasificar como "organometálico", ya que contienen grupos orgánicos, por ejemplo B ( CH 3) 3). Compuestos del grupo principal también se producen en la naturaleza, por ejemplo, fosfato en el ADN , y por lo tanto puede ser clasificado como bioinorgánica. Por el contrario, los compuestos orgánicos que carecen de ligandos (muchos) de hidrógeno pueden ser clasificados como "inorgánicos", tales como los fullerenos, buckytubes y óxidos de carbono binario.
- Ejemplos: Tetranitruro de tetraazufre S 4 N 4, diborano B 2 H 6, siliconas, buckminsterfullereno C 60.
Compuestos de metales de transición
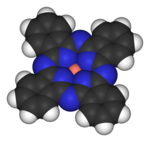
Los compuestos que contienen metales del grupo 4 a 11 se consideran compuestos de metales de transición. Los compuestos con un metal del grupo 3 o 12 veces también se incorporan a este grupo, pero también a menudo clasificados como compuestos del grupo principal.
Compuestos de metales de transición muestran una rica química de coordinación, que van desde tetraédrica de titanio (por ejemplo TiCl4) para cuadrar plana para algunos complejos de níquel a octaédricos de complejos de coordinación de cobalto. Una gama de metales de transición se puede encontrar en compuestos biológicamente importantes, tales como el hierro en la hemoglobina.
- Ejemplos: pentacarbonilo de hierro, tetracloruro de titanio, cisplatino
Los compuestos organometálicos
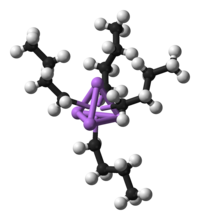
Por lo general, los compuestos organometálicos se considera que contienen el grupo de MCH. El metal (M) en estas especies puede ser un elemento del grupo principal o un metal de transición. Operativamente, la definición de un compuesto organometálico es más relajado para incluir también altamente complejos lipófilos tales como carbonilos metálicos e incluso metales alcóxidos.
Los compuestos organometálicos se consideran principalmente una categoría especial porque ligandos orgánicos suelen ser sensibles a la hidrólisis o la oxidación, lo que exige que la química organometálica emplea métodos de preparación más especializada que era tradicional en los complejos de tipo Werner. Metodología sintética, especialmente la capacidad de manipular los complejos en disolventes de baja potencia de coordinación, activar la exploración de ligandos muy débilmente coordinación tales como hidrocarburos, H 2 y N 2. Debido a que los ligandos son la petroquímica, en cierto sentido, el área de la química organometálica ha beneficiado mucho de su importancia para la industria.
- Ejemplos: Ciclopentadienilhierro dicarbonilo dímero (C 5 H 5) Fe (CO) 2 CH 3, El ferroceno Fe (C 5 H 5) 2, Hexacarbonilo Molibdeno Mo (CO) 6, Diborano B 2 H 6, Se añadió tetrakis (trifenilfosfina) paladio (0) Pd [P (C 6 H 5) 3] 4
Compuestos de racimo

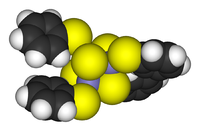
Las agrupaciones se pueden encontrar en todas las clases de compuestos químicos . De acuerdo con la definición comúnmente aceptada, un grupo consta como mínimo de un conjunto triangular de los átomos que están unidos directamente entre sí. Pero metal-metal en condiciones de servidumbre complejos dimetallic son muy importantes para la zona. Las agrupaciones se producen en sistemas inorgánicos "puros", la química organometálica, química grupo principal, y la química bioinorgánica. La distinción entre grandes conglomerados y sólidos a granel es cada vez más borrosa. Esta interfaz es la base química de la nanociencia o nanotecnología y específicamente surgen del estudio de efectos cuánticos en tamaño racimos de seleniuro de cadmio. Por lo tanto, grandes grupos pueden ser descritas como una matriz de átomos unidos de carácter intermedio entre una molécula y un sólido.
- Ejemplos: Fe 3 (CO) 12, B 10 H 14, [Mo 6 Cl 14] 2-, 4Fe-4S
Compuestos Bioinorgánicos
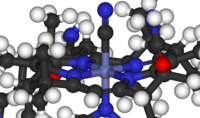
Ver también Química Bioorganometallic
Estos compuestos se producen (por definición) en la naturaleza, pero el subcampo incluye especies antropogénicas, como los contaminantes y las drogas, por ejemplo, El cisplatino. El campo incluye muchos compuestos, por ejemplo, los fosfatos en el ADN, sino también complejos metálicos que contienen ligandos que van desde las macromoléculas biológicas, comúnmente péptidos, a las especies mal definidos, tales como ácidos húmicos, y al agua (por ejemplo, coordinado a gadolinio complejos empleado para MRI).
- Ejemplos: hemoglobina, metilmercurio, carboxipeptidasa
Compuestos de estado sólido
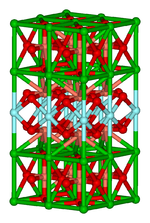
Esta importante área se centra en estructura, de unión, y las propiedades físicas de los materiales. En la práctica, la química inorgánica en estado sólido utiliza técnicas como cristalografía para ganar una comprensión de las propiedades que resultan de interacciones colectivos entre las subunidades del sólido. Incluido en química del estado sólido son los metales y su aleaciones intermetálicas o derivados. Los campos relacionados son la física de la materia condensada , mineralogía, y ciencia de los materiales .
- : Ejemplos chips de silicio , zeolitas, YBa 2 Cu 3 O 7
Química inorgánica Teórica
Una perspectiva alternativa sobre el área de la química inorgánica se inicia con la Modelo de Bohr del átomo y, utilizando las herramientas y modelos de la química teórica y la química computacional , se expande en la unión en moléculas más complejas simples cuando. Descripciones mecánicas cuánticas precisos para las especies multielectrónicos, la provincia de química inorgánica, es difícil. Este desafío ha dado lugar a muchos enfoques semi-cuantitativos o semi-empíricos incluidos teoría de orbitales moleculares y la teoría del campo ligando, En paralelo con estas descripciones teóricas, se emplean metodologías aproximadas, incluyendo teoría del funcional de la densidad.
Excepciones a las teorías, cualitativos y cuantitativos, son extremadamente importantes en el desarrollo del campo. Por ejemplo, Cu II 2 (OAc) 4 (H 2 O) 2 es casi diamagnético debajo de temperatura ambiente mientras que la teoría Crystal Campo predice que la molécula tendría dos electrones desapareados. El desacuerdo entre teoría cualitativa (paramagnético) y observación (diamagnética) condujo al desarrollo de modelos de "acoplamiento magnético." Estos modelos mejorados condujeron al desarrollo de nuevos materiales magnéticos y nuevas tecnologías.
Teorías cualitativas

La química inorgánica se ha beneficiado enormemente de las teorías cualitativas. Estas teorías son más fáciles de aprender, ya que requieren poco de historia en la teoría cuántica. Dentro de los compuestos del grupo principal, TREPEV predice poderosamente, o al menos racionaliza, la estructuras de los compuestos del grupo principal, como una explicación de por qué NH 3 es piramidal que ClF3 tiene forma de T. Para los metales de transición, la teoría del campo cristalino permite comprender el magnetismo de muchos complejos simples, como por qué [Fe III (CN) 6] 3- sólo tiene un electrón no apareado, mientras que [Fe III (H 2 O) 6] 3+ tiene cinco. Un particularmente poderoso enfoque cualitativo para evaluar la estructura y reactividad comienza con moléculas que clasifican según recuento de electrones, centrándose en los números de electrones de valencia, por lo general en el átomo central en una molécula.
Teoría Molecular Symmetry Grupo
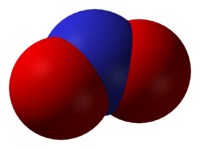
Una construcción de central en la química inorgánica es la teoría de la simetría molecular. Matemática teoría de grupos ofrece el lenguaje para describir las formas de las moléculas de acuerdo a su " grupo de puntos de simetría ". La teoría de grupos también permite factoring y simplificación de los cálculos teóricos.
Características espectroscópicas se analizan y se describen con respecto a las propiedades de simetría de la, entre otras cosas, de vibración o estados electrónicos. El conocimiento de las propiedades de simetría de los estados fundamental y excitado permite predecir los números y las intensidades de absorción en el espectro de vibración y electrónicos. Una aplicación clásica de la Teoría de Grupos es la predicción del número de vibraciones de CO en complejos carbonilos metálicos sustituidos. Las aplicaciones más comunes de simetría a la espectroscopia implican espectros vibracionales y electrónicos.
Como una herramienta de instrucción, la Teoría de Grupos destaca aspectos comunes y las diferencias en la unión de las especies dispares, tales como WF 6 y Mo (CO) 6 o CO 2 y NO 2.
Caminos de reacción
La teoría de las reacciones químicas es más difícil que la teoría de una molécula estática. Teoría Marcus ofrece un poderoso vínculo entre la unión, el mecanismo, y reactividad. Las fuerzas relativas de enlaces metal-ligando, que pueden calcularse teóricamente, anticipa las vías cinéticamente accesibles.
Termodinámica y química inorgánica
Un enfoque cuantitativo alternativo a la química inorgánica se centra en las energías de reacciones. Este enfoque es muy tradicional y empírica, pero también es útil. Conceptos generales que se formulan en términos termodinámicos incluyen potencial redox, la acidez , la fase cambios. Un concepto clásico de la termodinámica inorgánicos es la Ciclo de Born-Haber, que se utiliza para la evaluación de las energías de los procesos elementales como afinidad electrónica, algunos de los cuales no se puede observar directamente.
Química inorgánica mecanicista
Un aspecto importante y cada vez más popular de la química inorgánica se centra en vías de reacción. Los mecanismos de las reacciones se discuten de forma diferente para diferentes clases de compuestos.
Elementos del grupo principal y lantánidos
Los mecanismos de compuestos del grupo principal de los grupos 13-18 generalmente se discuten en el contexto de la química orgánica (compuestos orgánicos son compuestos grupo principal, después de todo). Elementos más pesados que el C, N, O y F a menudo se forman compuestos con más electrones que lo predicho por la regla del octeto, como se explica en el artículo sobre moléculas hipervalentes. Los mecanismos de sus reacciones difieren de los compuestos orgánicos por esta razón. Elementos más ligero que el de carbono ( B , Be , Li ), así como Al y Mg a menudo forman estructuras deficientes en electrones que son electrónicamente similar a carbocationes. Tales especies deficientes en electrones tienden ro reaccionan a través de vías asociativas. La química de los lantánidos refleja muchos aspectos de la química visto para el aluminio.
Complejos de metales de transición
Mecanismos de las reacciones de los metales de transición se discuten de forma diferente a partir de compuestos del grupo principal. El importante papel de los orbitales d en unión influye fuertemente en las vías y las tasas de sustitución de ligandos y la disociación. Estos temas se tratan en artículos en química de coordinación y ligando. Ambos se observan vías asociativas y disociativas.
Un aspecto fundamental de la química del metal de transición mecanicista es la labilidad cinética del complejo ilustrado por el intercambio de agua libre y unido en los complejos prototípicos [M (H 2 O) 6] n +:
- [M (H 2 O) 6] + n + 6 H 2 O * → [M (H 2 O *) 6] + n + 6 H 2 O
- donde H 2 O * denota isotópicamente agua enriquecida, por ejemplo H 2 17 O
Las tasas de intercambio de agua varía por 20 órdenes de magnitud a través de la tabla periódica, con complejos de lantánidos en una especie extremas e Ir (III) siendo el más lento.
Las reacciones redox
Las reacciones redox son frecuentes para los elementos de transición. Dos clases de reacción redox se consideran: las reacciones de transferencia de átomo, como la adición oxidante / eliminación reductora, y de transferencia de electrones. Una reacción redox fundamental es "auto-cambio", que implica la degenerada reacción entre un oxidante y un reductor. Por ejemplo, permanganato y su pariente de un electrón reducida intercambio manganato un electrón:
- [MnO 4] - + [Mn * O 4] 2- → [MnO 4] 2- + [Mn * O 4] -
Las reacciones en ligandos
Ligandos coordinados muestran reactividad distinto de los ligandos libres. Por ejemplo, la acidez de los ligandos de amoníaco en [Co (NH 3) 6] 3+ es elevada en relación con NH 3 en sí. Los alquenos unidos a cationes metálicos son reactivos hacia nucleófilos mientras que alquenos normalmente no lo son. El área grande e industrialmente importante de la catálisis depende de la capacidad de los metales para modificar la reactividad de ligandos orgánicos. Catálisis homogénea se produce en solución y catálisis heterogénea se produce cuando gaseosos o disueltos sustratos interactúan con superficies de sólidos. Tradicionalmente catálisis homogénea se considera parte de la química organometálica y catálisis heterogénea se discute en el contexto de la ciencia de superficies, un subcampo de la química del estado sólido. Pero los principios químicos básicos inorgánicos son el mismo. Los metales de transición, casi únicamente, reaccionan con las moléculas pequeñas como el CO, H 2, O 2 y C 2 H 4. La importancia industrial de estas materias primas impulsa el área activa de la catálisis.
Caracterización de compuestos inorgánicos
Debido a la amplia gama de elementos y la correspondientemente diversas propiedades de los derivados resultantes, química inorgánica está estrechamente asociado con muchos métodos de análisis. Los métodos más antiguos tendían a examinar las propiedades a granel, tales como la conductividad eléctrica de soluciones, puntos de fusión , solubilidad , y la acidez . Con el advenimiento de la teoría cuántica y la expansión correspondiente de aparatos electrónicos, herramientas nuevas se han introducido para investigar las propiedades electrónicas de moléculas inorgánicas y sólidos. A menudo, estas mediciones proporcionan ideas relevantes para los modelos teóricos. Por ejemplo, las mediciones en el espectro de fotoelectrones de metano demostró que describe la unión de los dos-centro, enlaces de dos electrones predijeron entre el carbono y el hidrógeno utilizando Teoría del enlace de valencia no es apropiado para describir los procesos de ionización de una manera simple. Estas ideas llevaron a la popularización de teoría de orbitales moleculares como orbitales totalmente deslocalizados son una simple descripción más apropiada de eliminación de electrones y la excitación de electrones.
Técnicas comúnmente encontrados son:
- Cristalografía de rayos X: Esta técnica permite la determinación de 3D estructuras moleculares.
- Varias formas de espectroscopía
- Espectroscopia ultravioleta-visible: Históricamente, esto ha sido una herramienta importante, ya que muchos compuestos inorgánicos son fuertemente coloreados
- Espectroscopía de RMN : Además de 1 H y 13 C muchas otras "buenas" núcleos de RMN (por ejemplo, 11 B , 19 C , 31 P , y 195 Pt ) dar información importante sobre las propiedades de compuestos y estructura. También la RMN de especies paramagnéticas puede dar lugar a una importante información estructural. RMN de protones también es importante porque el núcleo de hidrógeno luz no se detecta fácilmente por cristalografía de rayos X.
- La espectroscopía infrarroja: Mayormente para absorciones de ligandos carbonilo
- Doble resonancia electrónica nuclear espectroscopia (ENDOR)
- Espectroscopia Mössbauer
- Electron-spin resonancia: ESR (o EPR) permite la medición del medio ambiente de centros metálicos paramagnéticos.
- Electroquímica: Voltametría cíclica y técnicas relacionadas sondean las características redox de compuestos.
Química inorgánica sintética
Aunque algunas especies inorgánicas se pueden obtener en forma pura de la naturaleza, la mayoría se sintetizan en las plantas químicas y en el laboratorio.
Métodos sintéticos inorgánicos se pueden clasificar más o menos según la volatilidad o la solubilidad de los reactivos de los componentes. Compuestos inorgánicos solubles se preparan usando métodos de síntesis orgánica. Para los compuestos que contienen metales que son reactivos hacia el aire, Línea Schlenk y se siguen las técnicas guantera. Compuestos y gases volátiles son manipulados en "distribuidores de vacío" que consta de tuberías de vidrio interconectados a través de válvulas, la totalidad de los cuales puede ser evacuado a 0,001 mm Hg o menos. Los compuestos se condensan usando nitrógeno líquido (78K pb) u otro criogénicos. Los sólidos se preparan típicamente utilizando hornos tubulares, los reactivos y productos están sellados en contenedores, a menudo hecha de sílice fundida (SiO2 amorfo), pero a veces los materiales más especializados, como tubos Ta soldadas o "barcos" Pt. Productos y reactivos se transportan entre las zonas de temperatura para conducir reacciones.
Enlaces
Enlaces a Online Química Inorgánica Revistas
| |||||||||||||||||
