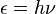La qu??mica cu??ntica
Sab??as ...
SOS Children ha intentado que el contenido de Wikipedia m??s accesible por esta selecci??n escuelas. Apadrina un ni??o para hacer una diferencia real.
La qu??mica cu??ntica es una rama de la qu??mica te??rica, que se aplica la mec??nica cu??ntica y la teor??a cu??ntica de campos para abordar cuestiones y problemas en la qu??mica . La descripci??n de la electr??nica comportamiento de ??tomos y mol??culas como perteneciente a su reactividad es una de las aplicaciones de la qu??mica cu??ntica. La qu??mica cu??ntica encuentra en la frontera entre la qu??mica y la f??sica , y las contribuciones significativas se han realizado por cient??ficos de ambos campos. Tiene una superposici??n fuerte y activo con el campo de la f??sica at??mica y la f??sica molecular , as?? como fisica quimica.
La qu??mica cu??ntica describe matem??ticamente el comportamiento fundamental de la materia en el molecular escala. Es, en principio, posible describir todos los sistemas qu??micos utilizando esta teor??a. En la pr??ctica, s??lo los sistemas qu??micos m??s simples pueden ser investigadas de manera realista puramente mec??nica cu??ntica t??rminos y aproximaciones deben hacerse a efectos pr??cticos (por ejemplo, Hartree-Fock, puesto de Hartree-Fock o Densidad teor??a funcional, ver la qu??mica computacional para m??s detalles). Por lo tanto una comprensi??n detallada de la mec??nica cu??ntica no es necesario para la mayor??a de la qu??mica, como las implicaciones importantes de la teor??a (principalmente la aproximaci??n orbital) puede ser entendido y aplicado en t??rminos m??s simples.
En la mec??nica cu??ntica (varias aplicaciones en qu??mica computacional y la qu??mica cu??ntica), la Hamiltoniano, o el estado f??sico, de una part??cula se pueden expresar como la suma de dos operadores, uno correspondiente a la energ??a cin??tica y el otro a energ??a potencial. La Hamiltoniano en la ecuaci??n de onda de Schr??dinger usado en qu??mica cu??ntica no contiene t??rminos para la esp??n del electr??n.
Las soluciones de la ecuaci??n de Schr??dinger para el ??tomo de hidr??geno da la forma de la funci??n de onda para orbitales at??micos, y la energ??a relativa de los diversos orbitales. La aproximaci??n orbital se puede utilizar para comprender los otros ??tomos, por ejemplo, helio , litio y de carbono .
Historia
La historia de la qu??mica cu??ntica esencialmente comenz?? con el descubrimiento de 1838 los rayos cat??dicos por Michael Faraday , la declaraci??n 1859 de la problema de la radiaci??n del cuerpo negro por Gustav Kirchhoff, la sugerencia de 1877 Ludwig Boltzmann que los estados de energ??a de un sistema f??sico podr??a ser discreto, y la hip??tesis cu??ntica 1900 por Max Planck que cualquier energ??a que irradia sistema at??mico te??ricamente se puede dividir en un n??mero de elementos discretos de energ??a ε tal que cada uno de estos elementos de energ??a es proporcional a la frecuencia ν con la que cada uno de ellos individualmente irradian energ??a , tal como se define por la siguiente f??rmula:
donde h es un valor num??rico llamado Constante de Planck. Luego, en 1905, para explicar el efecto fotoel??ctrico (1839), es decir, que la luz de ciertos materiales que brilla puede funcionar para expulsar los electrones de la materia, Albert Einstein postul??, en base a la hip??tesis cu??ntica de Planck, que la luz en s?? consta de part??culas cu??nticas individuales, que m??s tarde fueron llamados fotones ( 1926). En los a??os siguientes, esta base te??rica lentamente comenz?? a ser aplicado a la estructura qu??mica, reactividad, y la uni??n.
Estructura electr??nica
El primer paso para resolver un problema de qu??mica cu??ntica generalmente se resuelve el Ecuaci??n de Schr??dinger (o Ecuaci??n de Dirac en qu??mica cu??ntica relativista) con el Hamiltoniano molecular electr??nico. Esto se llama la determinaci??n de la estructura electr??nica de la mol??cula. Se puede decir que la estructura electr??nica de una mol??cula o cristal implica esencialmente sus propiedades qu??micas.
Modelo Wave
La base de la mec??nica cu??ntica y la qu??mica cu??ntica es el modelo de onda, en el que el ??tomo es un peque??o denso, cargado positivamente n??cleo rodeado por electrones. A diferencia de la anterior Modelo at??mico de Bohr, sin embargo, el modelo de onda describe electrones como " nubes "se mueven en orbitales, y sus posiciones est??n representadas por distribuciones de probabilidad en lugar de puntos discretos. La fuerza de este modelo reside en su poder predictivo. En concreto, se predice el patr??n de elementos qu??micamente similares que se encuentran en la tabla peri??dica . El modelo de onda se llama as?? porque los electrones exhiben propiedades (como la interferencia) tradicionalmente asociados con las ondas. Ver la dualidad onda-part??cula .
Enlace de valencia
Aunque la base matem??tica de la qu??mica cu??ntica hab??a sido colocado por Schr??dinger en 1926 , en general se acepta que el primer verdadero c??lculo en qu??mica cu??ntica era la de los f??sicos alemanes Walter Heitler y Fritz London en el hidr??geno (H 2) mol??cula en 1927 . M??todo Heitler y de Londres se extendi?? por el f??sico te??rico estadounidense John C. Slater y el qu??mico te??rico estadounidense Linus Pauling para convertirse en el Valence-Bond (VB) [o Heitler-Londres-Slater-Pauling (HLSP)] m??todo. En este m??todo, la atenci??n es dedicado principalmente a las interacciones entre pares de ??tomos, y por lo tanto este m??todo se correlaciona estrechamente con dibujos de qu??micos cl??sicos " bonos .
Molecular orbital
Un enfoque alternativo fue desarrollado en 1929 por Friedrich Hund y Robert S. Mulliken, en el que los electrones se describen por funciones matem??ticas deslocalizada sobre toda una mol??cula . El enfoque Hund-Mulliken o m??todo orbital molecular (MO) es menos intuitivo para los qu??micos, pero ha resultado capaz de predecir propiedades espectrosc??picas mejor que el m??todo VB. Este enfoque es la base conceptual de la M??todo de Hartree-Fock y m??s m??todos de post Hartree-Fock.
Teor??a funcional de la densidad
La Modelo de Thomas-Fermi fue desarrollado independientemente por Thomas y Fermi en 1927 . Este fue el primer intento para describir sistemas de muchos de electrones sobre la base de densidad electr??nica en lugar de funciones de onda, aunque no fue muy exitoso en el tratamiento de las mol??culas enteras. El m??todo proporcion?? la base para lo que hoy se conoce como la teor??a funcional de la densidad. Aunque este m??todo es menos desarrollada que colocar nuestros m??todos Hartree-Fock, sus requerimientos computacionales bajos permiten hacer frente a grandes mol??culas poliat??micas e incluso macromol??culas, que se ha convertido en el m??todo m??s utilizado en la qu??mica computacional en la actualidad.
Chemical Dynamics
Un paso adicional puede consistir en resolver el Ecuaci??n de Schr??dinger con el total hamiltoniano molecular con el fin de estudiar el movimiento de las mol??culas. Soluci??n directa de la ecuaci??n de Schr??dinger se llama din??mica molecular cu??ntica, dentro del aproximaci??n semicl??sico din??mica molecular semicl??sicos, y dentro de la mec??nica cl??sica marco din??mica molecular (MD). Enfoques estad??sticos, utilizando por ejemplo el m??todo de Monte Carlo , tambi??n son posibles.
Din??mica qu??mica adiab??ticos
En la din??mica adiab??ticas, interacciones interat??micas est??n representados por un solo escalar potenciales llamados superficies potenciales de energ??a. Este es el Born-Oppenheimer aproximaci??n introducida por Nacido y Oppenheimer en 1927 . Aplicaciones pioneras de esta en la qu??mica fueron realizadas por Rice y Ramsperger en 1927 y Kassel en 1928 , y generalizada en el Teor??a RRKM en 1952 por Marcus quien tom?? la la teor??a del estado de transici??n desarrollado por Eyring en 1935 en cuenta. Estos m??todos permiten estimaciones simples de unimoleculares velocidades de reacci??n de unas pocas caracter??sticas de la superficie potencial.
Din??mica qu??mica no adiab??ticos
Din??mica no adiab??tico consiste en tomar la interacci??n entre varios superficie de energ??a potencial acoplada (correspondientes a diferentes electr??nica estados cu??nticos de la mol??cula). Los t??rminos de acoplamiento se llaman acoplamientos vibr??nicas. El trabajo pionero en este campo fue realizado por Stueckelberg, Landau, y Zener en los a??os 1930 , en su trabajo en lo que ahora se conoce como la Transici??n de Landau-Zener. Su f??rmula permite la probabilidad de transici??n entre dos curvas de potencial diab??ticos en el barrio de un cruce evitado a ser calculado.
La qu??mica cu??ntica y la teor??a cu??ntica de campos
La aplicaci??n de la teor??a cu??ntica de campos (QFT) a los sistemas qu??micos y teor??as se ha vuelto cada vez m??s com??n en las ciencias f??sicas modernas. Uno de los primeros y m??s fundamentalmente expl??citas apariciones de esto se ve en la teor??a de la photomagneton. En este sistema, los plasmas , que son omnipresentes en la f??sica y la qu??mica, son estudiados con el fin de determinar la base cuantificaci??n del subyacente campo bosonic. Sin embargo, la teor??a cu??ntica de campos es de inter??s en muchos campos de la qu??mica, incluyendo: qu??mica nuclear, astroqu??mica, sonoqu??mica, y hidrodin??mica cu??ntica. M??todos te??ricos de campo tambi??n han sido fundamentales en el desarrollo de la ab initio eficaz hamiltoniano teor??a de los m??todos de electrones pi semi-emp??ricos.