
Trifosfato de adenosina
Acerca de este escuelas selecci??n Wikipedia
Esta selecci??n Wikipedia est?? disponible sin conexi??n de SOS Children para su distribuci??n en el mundo en desarrollo. Con Infantil SOS se puede elegir a apadrinar a los ni??os en m??s de cien pa??ses
| Trifosfato de adenosina | |
|---|---|
 | |
 | |
5- (6-aminopurin-9-il) | |
| Identificadores | |
| CAS | 56-65-5 |
| Propiedades | |
| F??rmula molecular | C 10 H 16 N 5 O 13 P 3 |
| Masa molar | 507.181 g / mol |
| Acidez (p K a) | 6.5 |
| Excepto cuando se indique lo contrario, los datos se den materiales en su condiciones normales (25 ?? C, 100 kPa) | |
| Exenciones y referencias | |
La adenosina 5'-trifosfato (ATP) es un multifuncional nucle??tidos que es m??s importante como " molecular moneda "intracelular de energ??a de transferencia. En este papel, el ATP transporta energ??a qu??mica dentro de las c??lulas para metabolismo. Se produce como una fuente de energ??a durante los procesos de la fotos??ntesis y la respiraci??n celular y consumido por muchos enzimas y una multitud de procesos celulares incluyendo reacciones biosint??ticas, motilidad y divisi??n celular. En las v??as de transducci??n de se??al, el ATP se utiliza como sustrato por quinasas que fosforilar prote??nas y l??pidos , as?? como por adenilato ciclasa, que utiliza ATP para producir el segunda mol??cula mensajera AMP c??clico.
La estructura de esta mol??cula consiste en una base de purina ( adenina) unido al ??tomo de carbono 1 'de una az??car pentosa ( ribosa). Tres grupos fosfato est??n unidos al ??tomo de carbono 5 'del az??car pentosa. ATP tambi??n se incorpora en ??cidos nucleicos por polimerasas en los procesos de Replicaci??n del ADN y la transcripci??n. Cuando se utiliza ATP en la s??ntesis de ADN, el az??car ribosa se convierte primero desoxirribosa por ribonucle??tido reductasa. ATP fue descubierto en 1929 por Karl Lohmann, y se propuso para ser la principal mol??cula de transferencia de energ??a en la c??lula por Fritz Albert Lipmann en 1941.
Propiedades f??sicas y qu??micas
ATP consiste en adenosina - compuesto a su vez de un anillo de adenina y una ribosa az??car - y tres grupos fosfato (trifosfato). Los grupos fosforilo, comenzando con el grupo m??s cercano a la ribosa, se conocen como la alfa (α), beta (β) y gamma (γ) fosfatos. ATP es altamente soluble en agua y es bastante estable en soluciones de pH entre 6.8 a 7.4, pero es r??pidamente hidrolizada a pH extremo. En consecuencia, el ATP se almacena mejor como una sal anhidra.
ATP es una mol??cula inestable y tiende a hidrolizarse en agua. Si ATP y ADP est??n en equilibrio qu??mico , casi todo el ATP se convierte en ADP. Cualquier sistema que est?? lejos del equilibrio contiene energ??a potencial, y es capaz de hacer el trabajo . Las c??lulas biol??gicas mantener la relaci??n de ATP a ADP en un punto diez ??rdenes de magnitud del equilibrio, con concentraciones de ATP mil veces mayor que la concentraci??n de ADP. Este desplazamiento del equilibrio significa que la hidr??lisis de ATP en la c??lula libera una gran cantidad de energ??a. ATP se conoce com??nmente como una "mol??cula de alta energ??a"; sin embargo, esto no es correcto, como una mezcla de ATP y ADP en equilibrio en el agua puede hacer ning??n trabajo ??til en absoluto. ATP no contiene "enlaces de alta energ??a", y cualquier otra mol??cula inestable servir??a igualmente bien como una forma de almacenamiento de energ??a, si la c??lula mantiene su concentraci??n lejos del equilibrio.
La cantidad de energ??a liberada puede calcularse a partir de los cambios en la energ??a, en condiciones no naturales. La variaci??n neta de energ??a t??rmica ( entalp??a ) en temperatura y presi??n de la descomposici??n de ATP est??ndar en hidratado ADP y fosfato inorg??nico hidratado es -20.5 kJ / mol, con un cambio en energ??a libre de 3,4 kJ / mol. La energ??a liberada por escisi??n o bien un fosfato (Pi) o pirofosfato (PPi) unidad de ATP, con todos los reactivos y productos en su estados est??ndar de concentraci??n 1 M, se encuentran:
- ATP + H 2 O → ADP (hidratado) + Pi (hidratado) + H + (hidratado)? G = -30,54 kJ / mol (-7,3 kcal / mol)
- ATP + H 2 O → AMP (hidratado) + PPi (hidratado) + H + (hidratado)? G = -45,6 kJ / mol (-10,9 kcal / mol)
Estos valores se pueden utilizar para calcular el cambio en la energ??a en condiciones fisiol??gicas y la relaci??n celular ATP / ADP. Los valores dados para la energ??a libre de Gibbs para esta reacci??n son dependientes de un n??mero de factores, incluyendo la fuerza i??nica global y la presencia de metales alcalinot??rreos , tales como iones Mg 2+ y Ca 2+. En condiciones t??picas celulares,? G es de aproximadamente -57 kJ / mol (-14 kcal / mol).
Ionizaci??n en los sistemas biol??gicos
ATP tiene m??ltiples grupos ionizables con diferente constantes de disociaci??n de ??cido. En soluci??n neutra, ATP se ioniza y existe principalmente como ATP 4-, con una peque??a proporci??n de ATP 3-. Como ATP tiene varios grupos cargados negativamente en soluci??n neutra, puede metales quelatos con afinidad muy alta. La constante de uni??n para diversos iones met??licos son (dados como por mol) como Mg 2+ (9 554), Na + (13), Ca 2+ (3 722), K + (8), Sr 2+ (1 381) y Li + (25). Debido a la fuerza de estas interacciones, existe ATP en la c??lula principalmente en un complejo con Mg 2+.
Bios??ntesis
La ATP concentraci??n dentro de la c??lula es t??picamente 1 - 10 mM. ATP puede ser producido por reacciones redox utilizando simples y complejas az??cares ( carbohidratos ) o l??pidos como fuente de energ??a. Para ATP que se sintetiza a partir de combustibles complejas, primero tienen que ser dividido en sus componentes b??sicos. Los hidratos de carbono son hidrolizado en az??cares simples, como la glucosa y fructosa. Las grasas ( triglic??ridos) se metabolizan para dar ??cidos grasos y glicerol.
El proceso global de oxidaci??n de la glucosa para el di??xido de carbono se conoce como la respiraci??n celular y puede producir hasta 36 mol??culas de ATP a partir de una sola mol??cula de glucosa. ATP puede ser producido por una serie de procesos celulares distintas; las tres v??as principales usados para generar energ??a en eucariotas son organismos la gluc??lisis y la ciclo del ??cido c??trico / la fosforilaci??n oxidativa, ambos componentes de respiraci??n celular; y beta-oxidaci??n. La mayor parte de esta producci??n de ATP por un no fotosint??tica eucariota aer??bico tiene lugar en la mitocondria , lo que puede hacer casi el 25% del volumen total de una c??lula t??pica.
La gluc??lisis
En la gluc??lisis, la glucosa y el glicerol se metabolizan a piruvato a trav??s de la v??a glucol??tica. En la mayor??a de los organismos de este proceso se produce en el citosol, pero en algunos protozoos tales como el kinetoplastids, esto se lleva a cabo en un especializado org??nulo llamado glicosoma. La gluc??lisis genera una cifra neta de dos mol??culas de ATP a trav??s de la fosforilaci??n del sustrato catalizada por dos enzimas: PGK y piruvato quinasa. Dos mol??culas de NADH tambi??n se producen, que puede oxidarse a trav??s de la cadena de transporte de electrones y el resultado en la generaci??n de ATP adicional por ATP sintasa. El piruvato generado como un producto final de la gluc??lisis es un sustrato para la Ciclo de Krebs.
Ciclo del ??cido c??trico
En la mitocondria , el piruvato se oxida por el complejo piruvato deshidrogenasa a acetil CoA, que se oxida completamente a di??xido de carbono por el ciclo del ??cido c??trico (tambi??n conocido como el ciclo de Krebs). Cada "giro" del ciclo del ??cido c??trico produce dos mol??culas de di??xido de carbono , una mol??cula del equivalente ATP trifosfato de guanosina (GTP) a trav??s fosforilaci??n a nivel de sustrato catalizada por succinil CoA sintetasa, tres mol??culas de la reducida coenzima NADH, y una mol??cula de la coenzima reducida FADH 2. Ambos de estos ??ltimos mol??culas se reciclan a sus estados oxidada (NAD + y FAD, respectivamente) a trav??s de la cadena de transporte de electrones, que genera ATP adicional por la fosforilaci??n oxidativa. La oxidaci??n de una mol??cula de NADH resulta en la s??ntesis de aproximadamente 3 mol??culas de ATP, y la oxidaci??n de uno FADH 2 produce alrededor de 2 mol??culas de ATP. La mayor??a de ATP celular es generado por este proceso. Aunque el ciclo del ??cido c??trico en s?? no implica molecular de ox??geno , que es un obligately proceso aer??bico porque O 2 es necesaria para reciclar el NADH y FADH 2 reducido a sus estados oxidados. En ausencia de ox??geno que el ciclo del ??cido c??trico dejar?? de funcionar debido a la falta de disposici??n NAD + y FAD.
La generaci??n de ATP por la mitocondria de NADH citos??lico se basa en la lanzadera del malato-aspartato (y en menor medida, la lanzadera de glicerol-fosfato), porque la membrana mitocondrial interna es impermeable al NADH y NAD +. En lugar de transferir el NADH generado, una malato deshidrogenasa conversos enzim??ticos oxaloacetato a malato, que se transloca a la matriz mitocondrial. Otra reacci??n catalizada malato deshidrogenasa se produce en la direcci??n opuesta, la producci??n de oxaloacetato y NADH a partir de la malato reci??n transportado y almacenar el interior de la mitocondria de NAD +. La transaminasa convierte el oxaloacetato a aspartato para el transporte de regreso a trav??s de la membrana hacia el espacio intermembrana.
En la fosforilaci??n oxidativa, el paso de electrones de NADH y FADH 2 a trav??s de los poderes de la cadena de transporte de electrones el bombeo de protones fuera de la matriz mitocondrial y en el espacio intermembrana. Esto crea una la fuerza motriz de protones que es el efecto neto de una gradiente de pH y una gradiente de potencial el??ctrico a trav??s de la membrana mitocondrial interna. El flujo de protones hacia abajo este gradiente de potencial - es decir, desde el espacio intermembrana de la matriz - proporciona la fuerza motriz para la s??ntesis de ATP por ATP sintasa. Este enzima contiene una subunidad rotor que gira f??sicamente con respecto a las partes est??ticas de la prote??na durante la s??ntesis de ATP.
La mayor parte del ATP sintetizado en las mitocondrias se utilizar?? para los procesos celulares en el citosol; por lo que debe ser exportada desde su lugar de s??ntesis en la matriz mitocondrial. La membrana interna contiene una antiporter, la translocasa ADP / ATP, que es una prote??na integral de membrana utilizado para intercambiar reci??n sintetizado ATP en la matriz de ADP en el espacio intermembrana. Este translocasa es impulsada por el potencial de membrana, tal como resulta en el movimiento de alrededor de 4 cargas negativas de la membrana mitocondrial a cambio de 3 cargas negativas se movieron dentro. Sin embargo, tambi??n es necesario para el transporte de fosfato en la mitocondria; el portador de fosfato mueve un prot??n en cada fosfato, disipando parcialmente el gradiente de protones.
Beta-oxidaci??n
Los ??cidos grasos tambi??n se pueden desglosar para acetil-CoA por beta-oxidaci??n. Cada ronda de este ciclo reduce la longitud de la cadena de acilo por dos ??tomos de carbono y produce una NADH y FADH 2 una mol??cula, que se utilizan para generar ATP por la fosforilaci??n oxidativa. Debido a NADH y FADH 2 son mol??culas ricas en energ??a, decenas de mol??culas de ATP pueden ser generados por la beta-oxidaci??n de una sola cadena de acilo largo. El rendimiento energ??tico de alta de este proceso y el almacenamiento compacto de grasa explican por qu?? es la m??s densa fuente de la dieta calor??as.
La respiraci??n anaer??bica
La respiraci??n anaer??bica o fermentaci??n implica la generaci??n de energ??a a trav??s del proceso de la oxidaci??n en ausencia de O 2 como una aceptor de electrones. En la mayor??a de los eucariotas, la glucosa se utiliza como un acumulador de energ??a y un donador de electrones. La ecuaci??n para la oxidaci??n de la glucosa para ??cido l??ctico es:
- C 6 H 12 O 6
 2CH 3 CH (OH) COOH + 2 ATP
2CH 3 CH (OH) COOH + 2 ATP
En procariotas, m??ltiples aceptores de electrones pueden ser utilizados en la respiraci??n anaerobia. Estos incluyen nitrato , sulfato o di??xido de carbono. Estos procesos dan lugar a los procesos ecol??gicamente importantes de desnitrificaci??n, la reducci??n de sulfato y acetog??nesis, respectivamente.
Reposici??n de ATP por difosfato quinasas de nucle??sidos
ATP tambi??n se puede sintetizar a trav??s de varios de los llamados reacciones "reposici??n" catalizadas por las familias de enzimas de difosfato quinasas de nucle??sidos (NDKs), que utilizan otros nucle??sidos trifosfato como donante fosfato de alta energ??a, y el ATP: familia guanido-fosfotransferasa, que utiliza creatina.
- ADP + GTP
 ATP + PIB
ATP + PIB
La producci??n de ATP durante la fotos??ntesis
En las plantas, el ATP se sintetiza en membrana tilacoide de la durante el cloroplasto reacciones dependientes de la fotos??ntesis en un proceso llamado fotofosforilacion. Aqu??, la energ??a de luz se utiliza para bombear protones a trav??s de la membrana del cloroplasto. Esto produce una fuerza prot??n-motriz y esto impulsa la ATP sintasa, exactamente como en la fosforilaci??n oxidativa. Algunos de la ATP producida en los cloroplastos se consume en el Ciclo de Calvin, que produce az??cares triosa.
Reciclaje ATP
La cantidad total de ATP en el cuerpo humano es de aproximadamente 0,1 mol. La mayor??a de ATP no se sintetiza generalmente de novo, sino que se genera a partir de ADP por los procesos antes mencionados. Por lo tanto, en un momento dado, la cantidad total de ATP + ADP mantiene bastante constante.
La energ??a utilizada por las c??lulas humanas requiere la hidr??lisis de 100 a 150 moles de ATP al d??a, que es alrededor de 50 a 75 kg. T??picamente, un humano utilizar?? encima de su peso corporal de ATP en el transcurso del d??a. Esto significa que cada mol??cula de ATP se recicla 1000-1500 veces durante un solo d??a (100 / 0,1 = 1.000). ATP no puede almacenarse, por lo tanto, su consumo sigue de cerca su s??ntesis.
Regulaci??n de la bios??ntesis
La producci??n de ATP en una c??lula eucariota aer??bico est?? estrechamente regulada por mecanismos alost??ricos, por efectos de retroalimentaci??n, y por la dependencia de la concentraci??n de sustrato de las enzimas individuales dentro de las v??as oxidativas glicolisis y fosforilaci??n. Puntos clave de control se producen en reacciones enzim??ticas que son tan energ??ticamente favorable que son efectivamente irreversible en condiciones fisiol??gicas.
En la gluc??lisis, hexoquinasa se inhibe directamente por su producto, la glucosa-6-fosfato, y piruvato quinasa se inhibe por s?? mismo ATP. El punto de control principal de la v??a glucol??tica es fosfofructoquinasa (PFK), que se alost??ricamente inhibida por altas concentraciones de ATP y activado por altas concentraciones de AMP. La inhibici??n de la PFK por ATP es inusual, ya que el ATP es tambi??n un sustrato en la reacci??n catalizada por la PFK; la forma biol??gicamente activa de la enzima es una tetr??mero que existe en dos conformaciones posibles, s??lo uno de los cuales se une al segundo sustrato fructosa-6-fosfato (F6P). La prote??na tiene dos sitios de uni??n a ATP - la sitio activo es accesible, ya sea en la conformaci??n de prote??nas, pero la uni??n al sitio de inhibidor de la ATP estabiliza la conformaci??n que se une F6P mal. Un n??mero de otras mol??culas peque??as puede compensar el desplazamiento inducido por ATP-en la conformaci??n de equilibrio y reactivar PFK, incluyendo AMP c??clico, iones de amonio, fosfato inorg??nico, y la fructosa 1,6 bifosfato y 2,6.
El ciclo del ??cido c??trico se rige principalmente por la disponibilidad de sustratos clave, en particular la relaci??n de NAD + a NADH y las concentraciones de calcio , fosfato inorg??nico, ATP, ADP, AMP y. Citrato - la mol??cula que da nombre al ciclo - es un inhibidor de la retroalimentaci??n de citrato sintasa y tambi??n inhibe la PFK, proporcionando un enlace directo entre la regulaci??n del ciclo del ??cido c??trico y la gluc??lisis.
En la fosforilaci??n oxidativa, el punto de control clave es la reacci??n catalizada por citocromo c oxidasa, que est?? regulado por la disponibilidad de su sustrato, la forma reducida de citocromo c. La cantidad de citocromo c reducido disponible est?? directamente relacionada con las cantidades de otros sustratos:
lo que implica directamente esta ecuaci??n:
Por lo tanto, una alta proporci??n de [NADH] a [NAD +] o una baja relaci??n de [ADP] [P i] a [ATP] implican una alta cantidad de citocromo c reducido y un alto nivel de actividad de la citocromo c oxidasa. Un nivel adicional de regulaci??n se introduce por las tarifas de transporte de ATP y NADH entre la matriz mitocondrial y el citoplasma.
Las funciones en las c??lulas
ATP es generado en la c??lula mediante procesos que consumen energ??a y se divide por los procesos de liberaci??n de energ??a. De esta manera ATP transfiere energ??a entre espacialmente separada reacciones metab??licas. ATP es la fuente principal de energ??a para la mayor??a de las funciones celulares. Esto incluye la s??ntesis de macromol??culas, incluyendo ADN, ARN, y prote??nas. ATP tambi??n juega un papel fundamental en el transporte de macromol??culas a trav??s de las membranas celulares, por ejemplo, exocitosis y endocitosis.
En la s??ntesis de la ??cido nucleico ARN, ATP es uno de los cuatro nucle??tidos incorporados directamente en las mol??culas de ARN por ARN polimerasas. La energ??a que impulsa esta polimerizaci??n procede de la escisi??n de un pirofosfato (dos grupos fosfato). El proceso es similar en la bios??ntesis de ADN, excepto que el ATP se reduce a la desoxirribonucle??tidos dATP, antes de la incorporaci??n en el ADN.
ATP es cr??ticamente involucradas en el mantenimiento de la estructura celular, facilitando el montaje y desmontaje de elementos de la citoesqueleto. En un proceso relacionado, se requiere ATP para la acortamiento de la actina y la miosina de filamentos de enlaces cruzados necesarios para contracci??n muscular. Este ??ltimo proceso es uno de los principales requisitos de energ??a de los animales y es esencial para locomoci??n y la respiraci??n.
Se??alizaci??n celular
De se??alizaci??n extracelular
ATP es tambi??n una mol??cula de se??alizaci??n. ATP, ADP, o la adenosina son reconocidos por receptores purin??rgicos.
En los seres humanos, este papel de se??alizaci??n es importante tanto en el sistema nervioso central y perif??rico. Dependiente de la actividad de liberaci??n de ATP a partir de sinapsis, axones y c??lulas gliales activa los receptores de membrana purinergic conocido como P2. Los receptores P2Y metabotr??picos son, es decir, Acoplado a prote??nas G y modular los niveles de AMP c??clico a veces, principalmente de calcio intracelular y. Quince miembros de la familia P2Y se han reportado (P2Y1-P2Y15), aunque algunos s??lo est??n relacionados a trav??s de homolog??a d??bil y varios (P2Y5, P2Y7, P2Y9, P2Y10) no funcionan como receptores que aumentan el calcio citos??lico. El subgrupo de receptores ionotr??picos P2X comprende siete miembros (P2X1-P2X7), que son canales de Ca2 + iones permeables por ligando que se abren cuando se une a un nucle??tido de purina extracelular. A diferencia de los receptores P2 (orden agonista ATP> ADP> AMP> ADO), purin??rgico nucle??tidos como ATP no son fuertes agonistas de los receptores P1 que est??n fuertemente activados por adenosina y otra nucle??sidos (ADO> AMP> ADP> ATP). Receptores P1 tienen A1, A2a, A2b y A3 subtipos ("A" como un remanente de la vieja nomenclatura del receptor de adenosina), todos los cuales son receptores acoplados a prote??nas G, A1 y A3 est??n acoplados a Gi, y A2a y A2b ser acoplado a Gs.
Se??alizaci??n intracelular
ATP es cr??tico en procesos de transducci??n de se??ales. Es utilizado por quinasas como la fuente de grupos fosfato en sus reacciones de transferencia de fosfato. La actividad quinasa en sustratos tales como prote??nas o l??pidos de membrana son una forma com??n de transducci??n de se??ales. La fosforilaci??n de una prote??na por una quinasa puede activar esta cascada como la activada por mit??geno cascada de prote??na quinasa.
ATP tambi??n es utilizado por adenilato ciclasa y se transforma a la segundo mensajero AMP c??clico mol??cula, que est?? implicado en la activaci??n de las se??ales de calcio por la liberaci??n de calcio desde los dep??sitos intracelulares. Esta forma de transducci??n de la se??al es particularmente importante en la funci??n cerebral, aunque est?? implicado en la regulaci??n de una multitud de otros procesos celulares.
S??ntesis de desoxirribonucle??tidos
En todos los organismos conocidos, los desoxirribonucle??tidos que componen el ADN se sintetizan por la acci??n de ribonucle??tido reductasa (RNR) enzimas en sus correspondientes ribonucle??tidos. Esta enzima reduce la 2 ' grupo hidroxilo en el az??car ribosa a desoxirribosa, formando un desoxirribonucle??tido (denotado dATP). Todas las enzimas de la ribonucle??tido reductasa utilizan un com??n sulfhidrilo mecanismo de radicales dependiente de reactivo residuos de ciste??na que se oxidan para formar enlaces disulfuro en el curso de la reacci??n. Enzimas RNR se reciclan por reacci??n con tiorredoxina o glutaredoxina.
La regulaci??n de RNR y enzimas relacionadas mantiene un equilibrio de dNTPs respecto a la otra y con respecto a los PNT en la c??lula. Muy inhibe de concentraci??n baja de dNTP S??ntesis de ADN y la reparaci??n del ADN y es letal para la c??lula, mientras que una relaci??n anormal de dNTPs es mutag??nico debido a la mayor probabilidad de que el ADN polimerasa que incorpora el dNTP mal durante la s??ntesis de ADN. Reglamento de o diferencial especificidad de RNR se ha propuesto como un mecanismo para alteraciones en los tama??os relativos de los focos de dNTP intracelulares menores de estr??s celular, tales como hipoxia.
La uni??n a prote??nas

Algunas prote??nas que se unen ATP hacen de una caracter??stica prote??na veces conocido como el Rossmann veces, que es un general nucle??tidos vinculante dominio estructural que tambi??n se puede unir el cofactor NAD. Las prote??nas de uni??n a ATP m??s comunes, conocidos como quinasas, comparten un peque??o n??mero de pliegues comunes; la prote??nas quinasas, la mayor superfamilia quinasa, todos comparten caracter??sticas estructurales comunes especializados para la uni??n de ATP y la transferencia de fosfato.
ATP en complejos con prote??nas generalmente requiere la presencia de una divalente cati??nico , casi siempre de magnesio , que se une a los grupos fosfato de ATP. La presencia de magnesio disminuye en gran medida la constante de disociaci??n de ATP a partir de su pareja de uni??n de prote??na sin afectar a la capacidad de la enzima para catalizar la reacci??n una vez que el ATP se ha unido. La presencia de iones de magnesio puede servir como un mecanismo para la regulaci??n de la quinasa.
An??logos de ATP
Laboratorios de bioqu??mica utilizan a menudo Los estudios in vitro para explorar procesos moleculares dependientes de ATP. Inhibidores de la enzima de las enzimas dependientes de ATP como Se necesitan quinasas para examinar la sitios de uni??n y estados de transici??n que participan en las reacciones dependientes de ATP. An??logos de ATP tambi??n se utilizan en Cristalograf??a de rayos X para determinar una estructura de la prote??na en el complejo con ATP, a menudo junto con otros sustratos. M??s ??tiles an??logos de ATP no pueden ser hidrolizados como ATP ser??a; En su lugar, la trampa de la enzima en una estructura estrechamente relacionada con el estado unido a ATP. La adenosina 5 '- (gamma-tiotrifosfato) es un an??logo de ATP extremadamente com??n en el que uno de los ox??genos gamma-fosfato es reemplazado por un azufre ??tomo; esta mol??cula se hidroliza a una velocidad dram??ticamente m??s lento que en s?? y las funciones de ATP como un inhibidor de los procesos dependientes de ATP. En los estudios de cristalograf??a, estados de transici??n de hidr??lisis son modelados por la cota ion vanadato. Sin embargo, se recomienda precauci??n en la interpretaci??n de los resultados de los experimentos con an??logos de ATP, ya que algunas enzimas pueden hidrolizar ellos a tasas apreciables en alta concentraci??n.

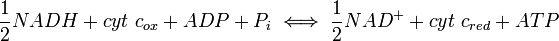
![\ Frac {cyt ~ c_ {red}} {cyt ~ c_ {ox}} = \ left (\ frac {[NADH]} {[NAD] ^ {+}} \ right) ^ {\ frac {1} {2 }} \ left (\ frac {[ADP] [P_ {i}]} {[ATP]} \ right) K_ {eq}](../../images/131/13158.png)
