Diamant
|
|
Cet article ou cette section doit être recyclé. (février 2012) Une réorganisation et une clarification du contenu paraissent nécessaires.
Discutez des points à améliorer en page de discussion.
|
| Diamant Catégorie I : Éléments natifs[1] | |
|---|---|
 | |
| Numéro CAS | |
| Classe de Strunz | 1.CB.10a
|
| Classe de Dana | 01.03.06.01
|
| Formule chimique | C |
| Masse formulaire[2] | 12,0107 ± 0,0008 uma C 100 %, |
| Couleur | Typiquement jaune, brun ou gris à incolore. Plus rarement, bleu, vert, noir, translucide, blanc, rose, violet, orange ou rouge |
| Système cristallin | Cubique |
| Réseau de Bravais | Cubique à faces centrées (diamant) |
| Clivage | 111 (parfait dans quatre directions) |
| Cassure | Conchoïdale |
| Échelle de Mohs | 10 |
| Éclat | Adamantin |
| Indice de réfraction | 2,407 à 2,451, selon la longueur d'onde de la lumière |
| Pléochroïsme | Non |
| Biréfringence | Non |
| Dispersion | 2 vz ~ 0,044 |
| Spectre d'absorption | Pour les diamants jaune pâle, la raie 415,5 nm est typique. Les diamants irradiés ou chauffés montrent souvent une raie vers 594 nm lorsqu'ils sont refroidis aux basses températures. |
| Transparence | Transparent |
| Densité | 3,517 |
| Température de fusion | 3 546,85 °C |
| Solubilité | Insoluble dans l'eau, les acides et les bases |
| Comportement chimique | Se transforme en graphite dans une flamme |
Le diamant est un minéral composé de carbone (tout comme le graphite et la lonsdaléite), dont il représente l'allotrope de haute pression, qui cristallise dans le système cristallin cubique. C'est le matériau naturel le plus dur (dureté de 10 (maximum) selon l'échelle de Mohs).
Étymologie et dénominations
Le terme diamant est issu du bas latin diamas, -antis, probablement issu par métathèse de *adimas, -antis (« aimant », le terme désignant à l'origine le métal le plus dur puis, toute matière très dure, comme la magnétite qui agit comme un aimant) sous l'influence des mots grecs commençant par dia-, lui-même dérivé du grec ancien Ἀδάμας (adamas : « indomptable », de adamastos[3] : inflexible, inébranlable[4], qui a donné l'adjectif adamantin, l'ancien nom du diamant adamant et également la désignation adamantane, hydrocarbure tricyclique de formule C10H16)[5].
Le terme qualifie initialement un état d'âme indomptable avant de désigner les métaux les plus durs avec lequel sont forgés les armes et les instruments des dieux (les seuls à posséder le secret de leur préparation) : le casque d'Héraclès de la Théogonie d'Hésiode[6], la faucille de Cronos, la charrue d'Æétès ou les chaînes de Prométhée (Eschyle)[7]. Le Pseudo-Platon parle de l'adamant dans l’Épinomis[8].
Son sens de brillance étincelante qu'évoque ce « minéral dur » et l’« éclat adamantin » expliquent qu'il a servi de référence pour désigner une grande variété de gemmes comme :
- Le corindon synthétique : « diamant d'alumine » ;
- L’hématite : « diamant noir du Névada », « diamant d'Alaska » (hématite noire) ;
- L’obsidienne décolorée : « diamant du Névada » ;
- La pyrite : « diamant alpin », « diamant de Pennsylvanie » ;
- Le quartz :
- Le « diamant de Bohême », « diamant de Briançon », « diamant de Brighton », « diamant de Bristol », « diamant de Buxton », « diamant de Hawaii » ; « diamant irlandais », « diamant mexicain », « diamant occidental » ;
- Le « diamant Marmorosch » (variété de quartz) ;
- Le « diamant d'Alaska », « diamant du Brésil » (cristal de roche) ;
- Le « diamant d'Alençon », « diamant allemand » (quartz enfumé) ;
- Le « diamant d'Arkansas » (quartz nommé également « Horatio Diamond ») ;
- Le « diamant du Colorado » (quartz fumé transparent) ;
- Le « diamant du Dauphiné », « diamant de Rennes » (quartz hyalin) ;
- Le zircon : « diamant de Ceylan » (incolore), « diamant de Matura » (zircon décoloré).
Toutes ces dénominations sont en fait abusives[9] (sauf évidemment pour indiquer la provenance d'un véritable diamant).
L’appellation « adamas » pour « diamant », se précise cependant dans le traité Sur les pierres[10] du philosophe grec Théophraste[7] ; elle est reprise dans l’œuvre Histoire naturelle du romain Pline l'Ancien[11], les deux auteurs réservant au mot diamant la pierre actuellement connue sous ce nom.
Du terme adamas dérivent les dénominations occidentales (français diamant, anglais diamond, espagnol et italien diamante), sanskrits et arabes (almas), russe (алмаз)[12].
En France, l'usage commercial du terme « diamant de culture » est interdit, à la place diamant synthétique doit être utilisé (voir gemme).
Histoire


La légende raconte que le diamant est exploité depuis 6 000 ans en Inde (cas du Koh-i Nor)[14]. Historiquement, les premiers diamants sont extraits il y a 3 000 ans en Inde[15] où ils sont trouvés uniquement dans les gisements alluvionnaires (rives des cours d'eau)[16] tels le Pennar, le Godâvarî, le Mahânadî ou le Krishnâ dans la région mythique de Golconde, principal centre de commerce du diamant pendant des siècles[17]. Il est représenté comme le « fruit des étoiles » ou provenant de sources sacrées, aussi orne-t-il les objets religieux[18]. Des textes bouddhistes révèlent tout son symbolisme : Sūtra du Diamant (pour qui le diamant est, comme la vérité, éternel), textes du Vajrayana. Il est aussi un objet de culte hindou, représentant symboliquement les vajras, et fait partie du mysticisme du jaïnisme et du lamaïsme tibétain[19]. Les Dravidiens pensent que les diamants poussent dans le sol comme des légumes, c'est pourquoi ils utilisent le caroubier dont les fèves servent d'étalon de masse pour peser les diamants, pratique à l'origine du carat[20].
Le diamant est à l'origine un élément de parure comme d'autres, (la taille du diamant (en) en facettes qui lui donne sa brillance caractéristique n'apparaît pas avant le milieu du XIVe siècle[21], probablement par crainte que cette technique ne lui fasse perdre de ses pouvoirs[22]), aussi est-il surtout utilisé comme amulette et talisman à cause de ses pouvoirs magiques et pour sa grande dureté dans la taille d'outils en fer ou la perforation de gemmes (jades, saphirs), comme en Chine, au Yémen vers -400 où ont été trouvées des perles percées par des diamants et au Kalimantan, partie indonésienne de Bornéo où le diamant est découvert vers 600[23].
L'Antiquité
En Égypte, Grèce et Rome antique, il est considéré comme indestructible chimiquement et représente les « larmes de Dieu ». Il est porté comme amulette à laquelle on attribue la vertu d'être un anti-poison, la poudre de diamant est utilisée en glyptique. Sa rareté lui donne de plus en plus de valeur et il gagne son statut de pierre précieuse[18]. Ses formes naturelles, sa dureté et sa transparence obtenue par un polissage partiel le rendent suffisamment attrayant pour qu'il soit monté en bijou pour la première fois vers le IIe siècle, la mythologie gréco-romaine l'associant à l’amour éternel : les flèches de Cupidon auraient en effet été surmontées de pointes de diamant[24].
Le Moyen Âge et la Renaissance
Au début du Moyen Âge, son commerce devient limité : l'expansion de l'Islam a pour effet que les marchands arabes contrôlent les routes caravanières vers l'Inde et l'Église chrétienne condamne l'usage des diamants comme amulette païenne. Le commerce du diamant se redéveloppe à partir des Grandes découvertes qui voient l'ouverture de la route des Indes par les Européens, les républiques maritimes prenant progressivement le monopole des épices et la République de Venise devenant le centre de commerce du diamant en Occident[25].
Au Moyen Âge et à la Renaissance, il est porté au sommet des couronnes ou en pendentif, orne les regalia et symbolise le « troisième œil » des mahârâjas. Les rois européens se le procurent pour sa rareté mais aussi pour son pouvoir d'anti-poison, panacée ultime[26]. En 1270, Louis IX institue des lois somptuaires réservant le diamant au seul souverain[27]. Jusqu'en 1477, date à la laquelle l'archiduc d'Autriche, Maximilien Ier de Habsbourg offre comme bague de fiançailles un diamant à Marie de Bourgogne, le diamant est porté uniquement[28] par des souverains hommes[29]. François Ier constitue les diamants de la Couronne en important des diamants d'Inde comme le Régent, puis d'autres ont été ajoutés par ses successeurs comme le Sancy et le diamant bleu de la Couronne.
En 1534, le pape Clément VII meurt en avalant un médicament à base de poudre de diamant. Dès lors le diamant paré de vertus curatives est utilisé comme poison (poudre de diamant utilisée dans des bagues à poison)[30]. Un diamant imparfait (brillant moins) est supposé porter malheur (ainsi le Bleu de France acheté par Jean-Baptiste Tavernier en 1668 pour le compte de Louis XIV n'est que de 220 000 livres, prix très inférieur aux gros diamants incolores). En fait, il s'agit le plus souvent pour les propriétaires de mine de créer une légende de malédiction pour dissuader les voleurs de vouloir les dérober ou pour les joaillers de créer toute une mythologie qui augmente la cote de vente du joyau[31].
Les époques moderne et contemporaine
Les gisements indiens s'épuisant, la découverte et exploration de l'Amérique ouvre de nouveaux horizons, ce qui entraîne la découverte de gisements au Brésil à partir de 1725 : jusqu'à cette date de leur découverte à Tejuco, l'Inde et l'Indonésie détiennent les seuls gisements exploités, la découverte brésilienne provoquant une véritable « ruée vers le diamant »[32]. Ces diamants brésiliens font chuter le prix du joyau de deux tiers aux trois quarts selon le type de pierre brute : jusqu'alors monté en pièce unique sur des chatons métalliques, il devient désormais une pièce de parure cousue à même le vêtement et portée au milieu du XVIIIe siècle surtout par les reines ou les aristocrates puis au XIXe siècle également par la haute bourgeoisie[33].
En 1772, Antoine Lavoisier utilise une lentille pour focaliser les rayons solaires sur un diamant dans une atmosphère riche en oxygène. Le produit de la combustion est du dioxyde de carbone, Lavoisier montrant la nature carbonée du diamant. En 1797, Smithson Tennant répète l'expérience sur le charbon : la combustion du diamant produisant le même volume de dioxyde de carbone qu'une masse équivalente de charbon, il montre que le diamant est du carbone pur[34].
En 1866, à Hopetown, à 120 kilomètres au sud de Kimberley, le diamant Eureka (en) (baptisé ainsi à l'Exposition universelle de Paris la même année) est découvert par un jeune garçon, Erasmus Jacobs, dans une kimberlite[35]. La mise au jour dans cette région de nombreuses mines diamantifères donne naissance en 1888 à la De Beers, plus grande entreprise diamantaire du monde.
Alors que la découverte de la composition du diamant au XVIIIe siècle marque le début de l'épopée de sa synthèse, il faut attendre le milieu du XXe siècle pour qu'enfin des chimistes réussissent à le fabriquer. Dès lors, le diamant est devenu un matériau industriel dont la production annuelle atteint aujourd'hui 570 millions de carats, soit 114 tonnes (chiffres 2007) [36].
En 1932, Gabrielle Chanel lance la collection « Bijoux de diamants » dans laquelle elle supprime la parure, les diamants étant montés sur platine. Elle est la première à désacraliser le diamant en imaginant des bijoux fantaisie (bijoux faux mélangés avec les vrais)[33].
Le 2 octobre 1979 est découverte la mine de diamant d'Argyle en Australie-Occidentale qui est à ce jour la plus importante mine de diamants au monde en volume[37].
En septembre 2012, la Russie rend publique l'existence d'un gisement de diamants sans équivalent, tenu secret durant 40 ans. Situé à Popigaï, il a été découvert au début des années 1970 dans une zone inhabitée de la Sibérie orientale, à 400 km de Khantiga et à 2 000 km au nord de Krasnoïarsk, le chef-lieu de la région. Il serait 110 fois supérieur aux réserves mondiales de diamants.
La planète 55 Cancri e serait constituée en grande partie par du diamant.
-
.jpg)
Parures de diamants sur le portrait de Pierre III et Catherine II peint par Georg Christoph Grooth (1716-1749), vers 1745, Odessa
-

Collier de diamants Napoléon, Smithsonian Institution, Washington D.C.
-

Diadème de la duchesse d'Angoulême (or, argent doré, 40 émeraudes et 1031 diamants) réalisé à Paris en 1819-1820 pour compléter une parure d'émeraude créée par Paul-Nicolas Menière en 1814
-

Collier de saphirs et diamant, National Museum of Natural History, Washington D.C.
-

Pièce de joaillerie avec diamants, place Vendôme, Paris
Formation et gisements
Origine du manteau terrestre
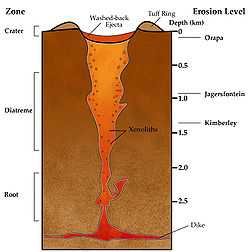
Les diamants sont constitués de carbone. Ils se forment lorsque ce dernier se trouve dans des conditions de température et de pression extrêmes, entre 1 100 °C et 1 400 °C pour la température, et pour la pression, entre 4,5 GPa et 6 GPa (selon des expériences de synthèse en laboratoire dans les années 1970), ce qui correspond à des profondeurs d'environ 150 à 1 000 km dans le manteau terrestre. L'analyse d'inclusions minérales et gazeuses (impuretés comme l'azote, le soufre ou des métaux colorant) permet d'être plus précis. La majorité des diamants cristallise entre 150 et 200 km de profondeur.
La plupart des diamants sont extraits de la kimberlite présente dans les régions les plus anciennes de la croûte continentale (au moins 1,5 milliard d'années)[38] (voir craton).
Dans les parties les plus internes des chaînes de collision (voir tectonique des plaques) comme les Alpes, l'Himalaya ou la chaîne hercynienne, on trouve des roches continentales contenant des microdiamants[39]. Ces diamants se forment au cours du métamorphisme dit d'ultrahaute pression en contexte subduction-collision : températures modérées de l'ordre de 800 à 900 °C et pression de l'ordre de 4 GPa.
La nature minéralogique des inclusions, leur contenu en éléments-trace et la composition isotopique (carbone et azote) des diamants eux-mêmes sont de précieux indices pour comprendre la genèse de ce minéral. Tout porte à croire que la croissance des diamants dans le manteau lithosphérique ne résulte pas d'une transformation directe à partir du graphite mais impliquerait plutôt l'entremise d'un fluide COH (fluide aqueux contenant du carbone dans une forme moléculaire non spécifiée : CH4, CO, CO2) ou d'un magma carbonaté (un panache venant percuter une racine continentale riche en carbonatite). Le mode de cristallisation des diamants issus du manteau inférieur est bien moins contraint. Les caractéristiques en éléments en traces des inclusions de pérovskites calciques dans ces diamants suggèrent à certains auteurs une croissance associée à la présence de croûte océanique, dans une zone du manteau où elle pourrait effectivement s'accumuler[40].
Les diamants formés sont de tailles micrométriques et ne peuvent donc pas être concernés par l'exploitation minière. Cependant, ils offrent des objets uniques pour l'étude du comportement d'un système rocheux en profondeur.
Deux grandes catégories de diamants sont distinguées selon la nature de leur cortège d'inclusions, caractéristiques de l'environnement de cristallisation. Dans la plupart des cas, ces inclusions représentent une minéralogie de péridotite. Une seconde catégorie d'inclusions est caractéristique d'association éclogitiques.
Origine volcanique de la roche vectrice
La roche diamantifère se forme à partir du manteau terrestre, en profondeur. Le magma provient d'une profondeur à laquelle les diamants peuvent se former (soit trois fois ou plus la profondeur du magma source de la plupart des volcans). Il s'agit donc d'un phénomène relativement rare. Le magma lui-même ne contient pas de diamants. Le magma qui remonte par volcanisme se refroidit dans les roches ignées (kimberlite ou lamproïte).
Les cratères volcaniques constituent généralement de petites surfaces à partir de cheminées volcaniques. Du matériel rocheux est transportée vers la surface. Les diamants sont remontés par des éruptions volcaniques puissantes, ne laissant pas le temps au diamant de se transformer. Elles ont occasionné la formation de brèches volcaniques, constituées de débris de roches d'origines profondes. Les diamants sont ainsi retrouvés en inclusion dans des roches appelées kimberlites.
Parce que les cratons sont très épais, ils sont très stables. Leur manteau lithosphérique se développe à une assez grande profondeur et, cette stabilité permet la formation des diamants. Toutes les cheminées volcaniques ne contiennent pas des diamants, et encore moins, en contiennent suffisamment pour permettre une exploitation minière économiquement viable.
Origine organique du carbone composant le diamant
Les diamants naturels sont souvent composés de carbone qui se trouvait dans le manteau depuis la formation de la Terre mais certains sont constitués de carbone provenant d'organismes comme des algues. C'est ce que révèle la composition isotopique du carbone[41]. Ce carbone organique a été enfoui jusqu'au manteau terrestre par le mouvement des plaques tectoniques, dans les zones de subduction.
Les diamants formés dans le manteau contiennent parfois des inclusions microscopiques d'olivine, minéral typique de la roche composant principalement le manteau: la péridotite. À l'inverse, les diamants formés lors de subductions, dans des roches éclogitiques, sont parfois porteurs d'inclusions de grenat ou d'omphacite par exemple, qui sont les minéraux typiques de ces roches-ci.
Processus extraterrestres de création de diamants

Les diamants peuvent également apparaître naturellement lors d'un violent impact d'un astéroïde. Le graphite alors comprimé se transforme en diamant.
Un gisement particulièrement riche a été découvert en Sibérie du Nord dans les années 1970. En raison de la guerre froide et pour ne pas remettre en cause les projets russes de construction d'usines de diamants synthétiques, l'information a été tenue secrète jusqu'en 2012[42]. Il s'agit d'un site de cratère d'impact, le cratère Popigaï, dû à un astéroïde il y a 35 millions d'années. La quantité de diamants serait dix fois supérieure à l'ensemble des réserves mondiales (ou beaucoup plus encore selon les sources[43],[44]) mais utilisable uniquement en industrie, de petites tailles (max. 10 mm) et deux fois plus durs[45].
Depuis 1984, des télescopes ont capté un rayonnement infrarouge émis par des étoiles mourantes riches en carbone et caractéristique de nano-diamants extrasolaires. En 1987, la météorite d'Orgueil révèle des nano-diamants pré-solaires qui seraient issus d'une géante rouge dont l'explosion est à l'origine de la formation du système solaire[46]. En 1997, de tels nano-diamants sont trouvés dans la météorite d'Allende[47].
D'après une récente étude américaine de 2013, dirigée par Mona Delitsky de l'University of Wisconsin–Madison, des diamants se formeraient dans l'atmosphère de Jupiter et de Saturne à partir du méthane atmosphérique. Cette étude rejoint toutes celles suggérant la production hypothétique de diamants dans les planètes gazeuses massives mais, leur observation étant absente, elles restent purement théoriques.
Origine sédimentaire de roches porteuses de diamants
Une fois que les diamants ont été transportés à la surface par le magma dans une cheminée volcanique, le matériau peut s'éroder et les diamants sont alors répartis sur une grande surface.
Une cheminée volcanique contenant des diamants est une source primaire de diamants. Les sources secondaires concernent toutes les régions où un nombre important de diamants a été érodé à partir de la kimberlite ou la matrice lamproïte et accumulé par l'eau ou le vent c'est-à-dire dans les dépôts alluviaux et lacustres, actuels et anciens. Les diamants libérés de leur matrice s'accumulent en fonction de leurs taille et densité dans ses sédiments.
Des diamants ont également été plus rarement trouvés dans des dépôts glaciaires (Wisconsin et Indiana). Contrairement aux dépôts alluviaux, les dépôts glaciaires ne constituent pas de bonnes sources d'exploitation.
Les gisements
Jusqu'au XVIe siècle, l'Inde et, plus particulièrement la région de Golkonda, (Golconde) comme la région de Bornéo étaient les seules régions de production. C'est en Inde qu'ont été extraits les plus célèbres diamants anciens. Puis les gisements du Brésil ont été découverts. Ils ont alimenté le marché occidental jusqu'à la fin du XIXe siècle, date de la découverte des gisements sud-africains.
Depuis cette époque, la plupart des diamants viennent d'Afrique (62,1 % en 1999). Cette situation a été l'origine de plusieurs guerres comme celle du Sierra Leone, où les objectifs stratégiques étaient le contrôle des principaux gisements du pays pour financer le conflit.
-

Cristal presque octaédrique dans sa matrice
-
.jpg)
Diamant dans une gangue de kimberlite, Afrique du Sud
-
.jpg)
Cristal octaédrique de diamant verdâtre
-
.jpg)
Macle de diamants, Afrique du Sud
-

Diamant octaédrique, approx. 1.8 carat (6 mm), sur une matrice de kimberlite, Finsch Diamond Mine, Afrique du Sud
La production des diamants

Les pays producteurs

En 2005, la production mondiale de diamants était de 173,5 millions de carats et les principaux producteurs sont la Russie, le Botswana, l'Australie et la République démocratique du Congo qui produisent à eux quatre un peu plus de 73 % de la production mondiale[48].
| Pays | Millions de carats | % du total |
|---|---|---|
| |
38,000 | 21,9 |
| |
31,890 | 18,4 |
| |
30,678 | 17,7 |
| |
27,000 | 15,6 |
| |
16,455 | 10,1 |
| |
15,775 | 9,1 |
| |
12,300 | 7,1 |
| |
10,000 | 5,8 |
| |
1,902 | 1,1 |
| |
1,190 | 0,7 |
| |
1,065 | 0,6 |
L'exploitation minière

Il existent principalement trois catégories de mines : à ciel ouvert, souterraines ou sous-marines[49].
Le processus d'extraction est très diversifié, puisqu'il dépend de la région dans laquelle le diamant est exploité. Mais, en général, les opérations se divisent en trois parties :
- l'élimination des éléments stériles (sol et roches qui couvrent le sable diamantifère) ;
- l'extraction ;
- le concassage ;
- le lavage.
En raison du coût de l'exploitation minière (en moyenne 250 tonnes[49] de minerai permettent d'extraire seulement un carat de diamant), seules les entreprises investissent dans les régions qui leur garantissent une production importante car des kilomètres carrés de terrain sont généralement excavés pour obtenir une gemme de taille et de qualité appréciables.
En dehors, l'extraction est rudimentaire et donc limitée à de petites concessions. Dans certains pays, africains notamment, l'absence d'encadrement législatif et la corruption ouvrent une brèche à la prospection, l'extraction et à un commerce incontrôlés du diamant.
L'exploitation alluviale est une alternative moins onéreuse[49], mais elle n'est possible que lorsque les mouvements géologiques ont élevé la roche diamantifère vers la surface, érodée par le lit d'une rivière.
Les diamants de synthèse
Depuis que l'on sait que le diamant n'est qu'une forme particulière du carbone, les physiciens et chimistes ont essayé de le synthétiser. La première synthèse artificielle du diamant eut lieu en 1953 à Stockholm par l'inventeur Baltzar von Platen et le jeune ingénieur civil Anders Kämpe travaillant pour la compagnie suédoise ASEA.
En soumettant le carbone à une forte pression et à une haute température pendant plusieurs heures, il est possible de réaliser un diamant de synthèse. Au départ, en raison de leur petite taille, ces derniers n'étaient utilisés que dans l'industrie[50].
Les propriétés
Le diamant est une forme métastable du carbone dans les conditions de température et de pression normales. Il brûle dès 500 °C dans un courant d'air, mais s'il est maintenu à 1 100 °C sous atmosphère neutre, il se transforme en graphite.[réf. nécessaire]
Structure cristalline
-

Structure cristalline du diamant (chaque côté mesure 3.6 Å)
-

Structures respectives du diamant et du graphite (carbone)
-
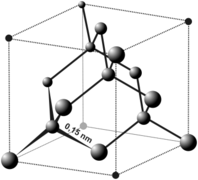
Maille d'un cristal de diamant
-
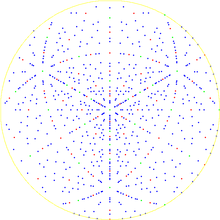
Projection stéréographique de la figure de pôles de la structure cristalline du diamant selon l'axe [111] qui démontre sa symétrie au long de la diagonale d'espace du cube élémentaire
Dans son état naturel, le diamant possède une structure dérivée de la structure cubique à faces centrées (cfc), appelée structure type diamant où en plus des atomes aux sommets du cube et au centre de chaque face, quatre des huit sites tétraédriques définis par une telle structure sont occupés, ce qui donne finalement huit atomes par maille (contre 4 pour une structure cfc classique), et fait que chaque atome de carbone a quatre voisins.
Cette structure est notée A4 en notation Strukturbericht. Son groupe d'espace est Fd3m (no 227 dans les tables internationales), son symbole de Pearson est 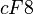 . Son paramètre de maille est a = 3,566 7 Å. Le volume d'une maille est de 45,37 Å3, la densité théorique est de 3,517.
. Son paramètre de maille est a = 3,566 7 Å. Le volume d'une maille est de 45,37 Å3, la densité théorique est de 3,517.
Propriétés physiques
Sa masse molaire est de 12,02 g⋅mol-1, sa masse volumique mesurée est de 3 520 kg/m3.
Dans l'édifice cristallin du diamant, les liaisons entre atomes de carbones résultent de la mise en commun des électrons de la couche périphérique afin de former des couches saturées. Chaque atome de carbone est ainsi associé de façon tétraédrique à ses quatre voisins les plus proches (hybridation sp3 du carbone), et complète ainsi sa couche extérieure. Ces liaisons covalentes, fortes et donc difficiles à casser, couvrent tout le cristal, d'où sa très grande dureté.
La forme liquide du diamant aurait la particularité comme l'eau d'être plus dense que la forme solide d'après un article paru dans la revue Nature Physics. Les conditions pour la phase liquide pourraient être réunies sur Uranus et Neptune[51].
La conductivité électrique est basse, car les électrons ne se regroupent pas comme dans un métal : ils restent liés aux atomes et ne peuvent pas, par exemple sous l'action d'un champ électrique extérieur, former un nuage électronique qui transporterait le courant de façon continue. En d'autres termes, le diamant est un très bon isolant. Néanmoins, il fait l'objet d'études en tant que semi-conducteur à large bande pour l'électronique de puissance.
La conductivité thermique du diamant est exceptionnelle, ce qui explique pourquoi il paraît si froid au toucher. Le diamant est un excellent conducteur thermique, toutefois le graphène avec 5 300 W/(m·K) détient le record. Dans un cristal isolant électrique comme le diamant, la conductivité thermique est assurée par les vibrations cohérentes des atomes de la structure. Des valeurs de 2 500 W/(m·K) ont été mesurées, que l'on peut comparer aux 401 W/(m·K) du cuivre et aux 429 W/(m·K) de l'argent. Cette propriété en fait un candidat comme substrat pour le refroidissement des semi-conducteurs.
Enfin, le coefficient de dilatation du diamant, lié aux propriétés des vibrations de la structure de ce matériau, est très faible. Pour le diamant pur, l'accroissement relatif de longueur par degré est d'environ un millionième à température ambiante, que l'on peut comparer aux 1,2 millionièmes de l'Invar, alliage constitué de 64 % de fer et de 36 % de nickel, qui est réputé pour sa très faible dilatation. Le fer est très loin derrière, avec 11,7 millionièmes.
Le diamant possède néanmoins un gros défaut pour l'industrie : tout d'abord, il est fragile. Sa dureté (inverse à l'élasticité) l'empêche en effet d'absorber les chocs, il peut donc être brisé à force de chocs répétés. Contrairement aux idées reçues, il faut donc éviter de le frapper avec un marteau, car il peut se briser.
Propriétés chimiques
Le diamant est une des formes allotropiques du carbone solide. Il est métastable, c'est-à-dire en équilibre thermodynamique avec les autres formes allotropiques : assez pour exister en l'état dans les conditions normales mais pas assez pour le demeurer. En effet, le diamant se transforme spontanément en graphite, la réaction étant favorisée thermodynamiquement par l'énergie de formation très basse du graphite, la forme la plus stable de toutes les formes du carbone. Une modification des paramètres (T, P) peut favoriser la transformation en question et son inverse (fait utilisé pour la conception des diamants de synthèse). Toutefois, la transformation du diamant en graphite est un processus cinétiquement lent, trop lent d'ailleurs pour qu'il puisse être observé, d'où sa stabilité apparente. Par conséquent, diamant n'est pas éternel -contrairement au proverbe !
De plus, certains diamants réagissent chimiquement (certains pierres peuvent être corrodées par les acides gras contenus dans certaines crèmes de beauté ou parfums, les lapis-lazuli peuvent être corrodés par des acides forts, etc.).
Le diamant ne réagit normalement pas avec les acides et les alcalins, mais il est soluble dans la soude fondue et surtout dans le nitrate de potassium. Plongé dans ces substances, le diamant se dissout et il est complètement détruit.
Enfin, il est sensible à l'oxydation et peut réagir avec certains métaux ou alliages métalliques.
Ces défauts ont conduit l'industrie à créer des matériaux d'une dureté comparable, mais plus stables, moins réactifs chimiquement, comme par exemple le nitrure de bore cubique.
Propriétés optiques
Le diamant est transparent, translucide ou opaque.
Son indice de réfraction est particulièrement élevé et varie en fonction de la longueur d'onde : ce sont ces propriétés, associées avec une taille particulière des facettes [52]qui lui donnent son éclat caractéristique, dit « adamantin ». Cet indice est de :
- 2,407 pour la lumière rouge (687 nm),
- 2,417 pour la lumière jaune (589 nm),
- 2,426 pour la lumière verte (527 nm) et
- 2,451 pour la lumière violette (431 nm).
Les diamants synthétiques sont en général fluorescents, vert, jaune, mauve ou rouge, en raison des impuretés présentes (azote, bore, nickel) ou après irradiation, au contraire de la plupart des diamants naturels.
Les utilisations
Après avoir eu des usages médicinaux, le diamant a toujours un usage symbolique et technique. Outre la joaillerie, le diamant est utilisé dans l'industrie en raison de ses propriétés, notamment de dureté.
Industrie
Dureté
L'industrie utilise beaucoup le diamant en raison de sa dureté. Depuis les outils de coupe et d'usinage fondés sur les propriétés mécaniques du diamant, jusqu'aux enclumes à diamant permettant de recréer des pressions titanesques, les applications en sont multiples. Cette dureté intervient aussi dans la précision que l'on peut atteindre avec des outils en diamant : notamment, les bistouris en diamant, permettent de créer des incisions ultraprécises (en ophtalmologie par exemple), car le moindre effleurement découpe la peau.
Biocompatibilité
N'étant pas réactif, il est biocompatible et ne génère pas de rejet ou de toxicité.
Neutralité
La chimie s'intéresse fortement au diamant : il possède des propriétés qui le rendent tout à fait approprié pour des applications en électrochimie:
- D'une part, il est résistant aux acides et aux bases, ce qui permet une utilisation dans des milieux corrosifs.
- D'autre part, les électrodes de diamant plongées dans de l'eau pure ne subissent aucune réaction électrochimique ; elles sont donc très efficaces.
Transparence et conductivité thermique
De nombreux dispositifs optiques utilisent la transparence du diamant, tandis que les dispositifs électroniques exploitent notamment ses propriétés thermiques.
Conduction des diamants dopés
En raison de sa faible conductivité électrique, le diamant peut être utilisé dans l'industrie des semi-conducteurs lorsqu'il est dopé avec des impuretés de bore ou de phosphore.
Utilisations envisagées
Les diamants sont actuellement à l'étude pour une utilisation comme détecteurs :
- de rayonnements dans des installations de recherche scientifique. Le CERN devait recevoir plusieurs mètres carrés de détecteurs en diamants synthétiques. La technologie n'ayant pas avancé assez vite, ils seront en silicium ;
- de rayonnements dans les installations de radiothérapie. Le carbone du diamant est le même que celui du corps (carbone 12 normal) et permet donc des mesures de dose plus proche de la dose réellement reçue par les tissus ;
- de produits divers, par les méthodes de type SAW (Surface Acoustic Waves), car le diamant est un très bon transducteur, grâce à sa rigidité. Il est cependant nécessaire de déposer (par des méthodes de CVD-Magnétron[53], notamment) un film mince de nitrure d'aluminium, qui est un piézoélectrique, au contraire du diamant. La forme du dépôt influe sur les produits détectables.
En revanche, et malgré leur stabilité considérable, les diamants ne peuvent pas servir dans un cœur de centrale nucléaire, car le bombardement est bien trop important et le matériau serait détruit.
-

Agrandissement des diamants sertis dans une lame
-

Un scalpel diamant, lame de diamant synthétique
Joaillerie
Intérêt des caractéristiques physiques
Les qualités (pureté, taille importante et couleur) de certains diamants en font la plus célèbre des pierres précieuses en joaillerie.
La beauté de son brillant est due au fait qu'il possède un haut indice de réfraction de la lumière et un grand pouvoir dispersif : en pénétrant, les rayons de lumière sont réfléchis à l'intérieur de la pierre à l'infini et la lumière blanche se disperse, retourne à l'intérieur transformée en un éventail de couleurs. Les diamants (comme les gouttes d'eau) fonctionnent comme des prismes en freinant, plus ou moins en fonction des longueurs d'onde (violette au maximum, rouge au minimum), de façon que les couleurs soient dispersées sous forme d'arc-en-ciel.
Tous les diamants ne sont pas utilisés en bijouterie. Le moindre défaut peut leur ôter de la valeur et ils sont alors employés pour des applications industrielles. Il s'agit de bulles internes ou de particules étrangères, de médiocre coloration ou lorsqu'ils présentent une forme irrégulière.
Tailles
-

Diagramme de tailles anciennes de diamants : évolution de la plus primitive à plus avancée, pré-Tolkowsky, vieille taille européenne
-
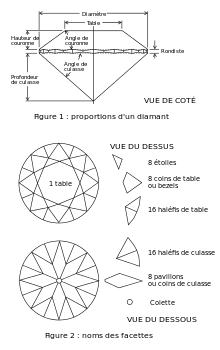
Taille brillant[1], selon Marcel Tolkowsky, 1919
-
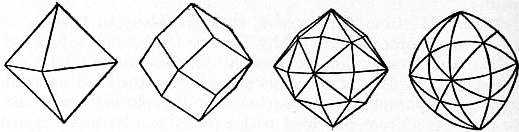
Formes de diamant : (1) octaèdre, (2) dodecaèdre rhombique, (3) hexakis-octaèdre, (4) et (3) facettes arrondies (Encyclopædia Britannica, 1911)
-

Diamants taillés
- Pour les termes en français : [1]
La taille des diamants s'effectue surtout à Anvers (Belgique), à Tel-Aviv (Israël) et au Gujarat (Inde) par la communauté jaïn. En Thaïlande, ce sont les pierres précieuses comme les rubis et les saphirs qui sont taillées. Alors qu'en Inde des méthodes de fabrication industrielles sont mises en place, à Anvers l'industrie conserve des méthodes artisanales pour les diamants de plus de 0.50 carats[54].
Le degré de la beauté de la dispersion (effet arc-en-ciel) du diamant dépend, en grande partie, de la taille et du poli de la pierre. Bien que naturellement les diamants aient leurs éclats propres, ceux-ci peuvent être améliorés et multipliés par la taille experte d'un diamantaire.
Du fait de son extrême dureté, le diamant ne peut être usiné que par un autre diamant, c'est pourquoi la taille et le poli de la pierre en sont les éléments les plus importants.
Avant de le tailler, on examine la gemme pour déterminer ses plans de clivage. On trace ensuite sur elle une ligne qui marque le périmètre de ces plans. Sur celui-ci, on fait une petite cannelure avec une espèce de bois qui porte dans son extrémité un diamant. Par cette ouverture, on introduit une fine lame d'acier, on donne un coup sec et la pierre se divise en deux.
Il existe de nombreuses façons de tailler le diamant. Du XVe au XVIIe siècle, on pratique la taille en pointe (polissage de la pointe de l'octaèdre) et celle en table (polissage des faces du cristal à la poudre de diamant). Les peintures de portraits de l'époque montrent un diamant noir car ces techniques sont peu efficaces. Au XVIIe siècle apparaît la taille « brillant », taille la plus connue, celle qui met le mieux en valeur la beauté du diamant et qui est de ce fait la plus utilisée. Cette technique perfectionnée permet de transformer les pierres brutes en véritables joyaux de lumière, en faisant apparaître 58 facettes (57 si l'on ne tient pas compte de la collette) : 33 sur la couronne et 24 sur la culasse, régulières et de tailles définies précisément, à la surface du diamant.
En effet, si les notions de pureté et de couleur paraissent familières, les proportions de taille le sont plus rarement. Pourtant, ces dernières sont un facteur de qualité essentiel. Elles conditionnent directement le rendu de brillance et le « feu » du diamant. À couleur identique, un diamant possédant de bonnes proportions sera bien plus éclatant qu'un diamant pur incorrectement taillé.
Depuis l'apparition de la taille Tolkovsky en 1919, les diamantaires n'ont cessé de chercher à optimiser le rendu de brillance du diamant. De toutes les tailles du diamant, c'est certainement la forme ronde brillant qui a été la plus étudiée et qui est la plus aboutie ; aujourd'hui, les proportions appliquées à cette taille résultent directement de la compréhension des lois optiques du matériau et de la maîtrise de la technique de taille et du polissage.
Au Japon, la taille flèche et cœurs est très appréciée et nommée ainsi en raison des formes des jeux de lumière produits. Les apprentis tailleurs sont au XXIe siècle très rares, la taille étant de plus en plus réalisée par des lasers à l'aide de systèmes informatiques.[réf. nécessaire]
Couleur
Les diamants sont aussi classés par couleurs. La couleur la plus commune étant « le blanc » (absence de couleur : c'est-à-dire que le diamant est transparent et incolore). Ces couleurs sont notées en allant de D (blanc le plus pur) à Z (teinte la plus foncée) :
| Code | Couleur |
|---|---|
| D | Blanc exceptionnel + |
| E | Blanc exceptionnel |
| F | Blanc extra + |
| G | Blanc extra |
| H | Blanc |
| I et J | Blanc nuancé |
| K et L | Légèrement teinté |
| M à Z | Couleur marquée |
L'origine de la classification moderne n'est pas clairement établie.[réf. nécessaire] D'aucuns[Qui ?] prétendent qu'elle daterait de la fin du XIXe siècle. Elle aurait été mise en place en remplacement de celle qui était utilisée, basée sur les trois premières lettres de l'alphabet A, B et C mais qui ne permettait pas de nuancer suffisamment la perception des couleurs. L'origine[Laquelle ?] de l'utilisation du D comme diamant comme premier niveau de classification serait une légende[réf. nécessaire].
Un des types de diamants de couleur les plus communs est le diamant brun. Ils proviennent en grande partie de la mine de diamant d'Argyle en Australie-occidentale. Pour promouvoir ce type de diamant auprès de la bijouterie/joaillerie, le propriétaire de la mine Rio Tinto, le Japon et les États-Unis ont mis en place dans les années 1990, une échelle de couleur pour les diamants brun allant de « Champagne » à « Cognac »[55].
| Code | Échelle de classification de la couleur brune des diamants bruns d’Argyle « Champagne » |
|---|---|
| C1 | « light champagne » |
| C2 | « light champagne » |
| C3 | « medium champagne » |
| C4 | « medium champagne » |
| C5 | « dark champagne » |
| C6 | « dark champagne » |
| C7 | « fancy cognac » |
Type
La classification des diamants s’organise aussi selon qu’il y ait ou non une présence d’azote dans sa structure, ce qui modifie ses propriétés optiques. On distingue deux types[56] : le type I où la présence d’azote est avérée, et le type II sans azote, très rare et qui correspond à des durées de formation plus longues[57].
On peut résumer cette classification, essentiellement scientifique, dans le tableau suivant :
| Type | Définition | Couleur | Particularité | Population |
|---|---|---|---|---|
| I a | Petits groupes d'azote Contient 0,3 % d'azote |
Incolore, jaune, brun, rose, vert et bleu | Fluorescence bleue Raies d’absorption étroites |
98 % |
| I b | Azote isolé Contient 0,1 % d'azote |
Jaune intense, orange, brun et incolore | Plupart des diamants synthétiques Raies d’absorption larges |
Rare Environ 1 % |
| II a | Pure sans azote | Incolore, brun, rose, violet, vert et doré Blanc exceptionnel + |
Transparent aux UV < 230 μm Quelques grands diamants célèbres[57] |
Environ 0,8 % Très rare |
| II b | Sans azote avec 0,1 % de bore | Bleu et gris | Semi-conducteur type P | Environ 0,2 % Extrêmement rare |
Pureté
Les diamants contiennent aussi une grande variété d'inclusions qui peuvent modifier son apparence. Une inclusion ou impureté était appelée en France un crapaud, mais cette appellation tend à disparaître dans le langage professionnel à la suite de la demande de la Confédération des Horlogers Bijoutiers Joailliers et Orfèvres (CHBJO)[réf. nécessaire] de ne plus l'utiliser. Les inclusions sont indiquées en utilisant les codes suivants[58] :
| Code | Signification |
|---|---|
| FL (Flawless) | Absence d'inclusions internes et de surface, avec un grossissement de 10 fois |
| IF (Internally Flawless) | Absence d'inclusions avec un grossissement de 10 fois |
| VVS1-VVS2 (Very Very Slightly Included) | Minuscule(s) inclusion(s) très difficilement visible(s) à la loupe avec un grossissement de 10 fois (1 étant la meilleure qualité) |
| VS1-VS2 (Very Slightly Included') | Très petite(s) inclusion(s) difficilement visible(s) à la loupe avec un grossissement de 10 fois |
| SI1-SI2-SI3 (Slightly Included) | Petite(s) inclusion(s) facilement visible(s) à la loupe avec un grossissement de 10 fois |
| I1-I2-I3 (Included) | Grande(s) et/ou nombreuses inclusion(s) visible(s) à l'œil nu |
Lorsqu'un diamant contient de l'hydrogène comme impureté, il apparaîtra généralement violet ou pourpre mais, dans de très rare cas, il apparaîtra rouge [59][60]. Enfin, les diamants verts résultent d'une irradiation par des particules alpha qui entraînent une déformation du réseau cristallin.
Masse
La masse d'un diamant se mesure en carats, qui équivaut à 0,20 gramme. La valeur d'un diamant est exponentielle par rapport à sa masse. Autrement dit, un diamant de deux carats a une valeur supérieure à deux diamants d'un carat, puisqu'il est considéré comme plus rare.
Diamantaires et gemmologues
Le classement en catégories du diamant (les 4C)[61] est réalisé par des professionnels. On appelle les personnes chargées de ce travail les gemmologues. Il existe peu de laboratoires mondiaux de gemmologie, les plus connus sont :
- Gemological Institute of America (GIA) à New York ;
- Hoge Raad voor Diamant (HRD) à Anvers ;
- GGTL Laboratories - à Genève et au Liechtenstein;
- Fellow of gemmological Association (FGA) à Londres ;
- International Gemological Institute (IGI) à Anvers ;
- American Gem Society (AGS) à New York.
Il existe deux types de certificats émis par les laboratoires.
- Le premier est un certificat de gradation pour diamants incolores. Ce document rend compte uniquement de la qualité du diamant, fonction des critères retenus par la profession et partant du postulat que la pierre est naturelle.
- Le deuxième type de certificat concerne principalement les diamants de couleur, mais également certains diamants incolores traités à haute pression et haute température (HPHT) pour les décolorer. Il confirme que la pierre est naturelle mais surtout rend compte de l'origine de la couleur, à savoir d'origine naturelle ou induite par un/des traitement/s (irradiation, chauffage, HPHT, éventuellement cumulés).
Ce type de certificat implique l'usage d'instruments modernes : spectroscopie infrarouge (IRTF), spectrométrie ultraviolet-proche infrarouge à basse température (UV-PIR), photoluminescence (PL), etc. Le diamantaire (terme désignant initialement le tailleur de diamant) a contrario du gemmologue n'étudie pas le diamant mais le négocie. En fonction de sa spécialité, son activité concernera les pierres taillées ou les bruts, certains cumulant les deux.
Diamants célèbres
Liste de quelques diamants célèbres :
| Couleur | Pierre brute | Pierre taillée | ||||
|---|---|---|---|---|---|---|
| Nom | Carats | Lieu de découverte | Année | Nom | Carats | |
| Incolore | Cullinan | 3 106 | Afrique du Sud (mine Premier) |
1905 | Grande Étoile d'Afrique (Cullinan I) |
530,20 |
| Petite Étoile d'Afrique (Cullinan II) |
317,40 | |||||
| 793,62 | Inde (mine de Kollur) |
XVIIe siècle | Grand Mogol | 279,56 | ||
| 787,50 | Inde | XVIIe siècle | Orloff | 194,75 | ||
| 410 | Inde | 1698 | Régent | 140,50 | ||
| Koh-i Nor | 105,602 | |||||
| Excelsior | 995,2 | Afrique du Sud (Jagersfontein) |
1893 | Excelsior I | 69,68 | |
| Sancy | 55,23 | |||||
| Beau Sancy | 34,98 | |||||
| Rose | Inde | avant 1642 | Grande Table | 242,31 (anciens carats) | ||
| Inde | Daria-e nour | entre 175 et 195 | ||||
| Inde | Noor-ol-Ain (en) | env. 60 | ||||
| 132,5 | Afrique du Sud | 1999 | Pink Star, puis Pink Dream (en) | 59.60 | ||
| Inde | Princie (en) | 34,65 | ||||
| Graff pink | 24,78 | |||||
| Hortensia | 21,32 | |||||
| Martian Pink | 12,04 | |||||
| Vert | 119,50 | Inde | 1743 | Dresde vert | 40,70 | |
| Bleu | 115 | Inde | 1668 | Diamant bleu de la Couronne (taillé en 1671) |
69 | |
| Hope (diamant bleu de la Couronne volé et retaillé vers 1812)[62] |
44,50 | |||||
| Bleu-gris | Inde | 1664 | Wittelsbach | 35,56 | ||
| 1559 | El Estanque (es) | 100 | ||||
| Noir | Orloff noir | 67,50 | ||||
| 587 | Afrique centrale | XXe siècle | L'esprit de De Grisogono | 312,24 | ||
| Tablet of Islam | 160,18 | |||||
| Jaune-marron | Florentin (disparu depuis 1922) | 137,27 | ||||
| 755 | Afrique du Sud | 1985 | Golden Jubilee (couronne royale de Thaïlande) |
545.67 | ||

Les plus grosses enchères
- Le 14 novembre 2007, un diamant de 84,37 carats a été adjugé 16,2 millions de dollars (11 millions d'euros) au fondateur de la chaîne de vêtements Guess, Georges Marciano, lors d'une vente aux enchères chez Sotheby's à Genève. Le diamant se place ainsi à la troisième place au classement des pierres précieuses et bijoux ayant remporté les plus grosses enchères[63].
- En mai 1995, un diamant de 100,1 carats a été adjugé 16,5 millions de dollars lors d'une vente à la même branche de Sotheby's, à Genève.
- Ce record est largement battu par un diamant bleu-gris déjà connu au XVIIe siècle, le Wittelsbach, adjugé 16,4 millions de livres sterling (18,7 millions d'euros) au célèbre joaillier londonien Laurence Graff par Christie’s, à Londres, le 10 décembre 2008[64].
- Le 17 novembre 2010, Laurence Graff acquiert à nouveau, un diamant rose de 24,78 carats, pour 46,16 millions de dollars (soit plus de 30 millions d'euros) et qu'il baptise Graff pink[65].
Symbolique
-

L'Étoile du sud de Jules Verne, dessin de Léon Benett (1884)
-

Médaillon représentant un diamant, Faculté de médecine de Zaragoza, Espagne
Le diamant est un symbole utilisé dans plusieurs domaines artistiques et fait l'objet de plus d'une légende ou histoire.
- Les noces de diamant symbolisent les 60 ans de mariage dans la tradition française.
- Le diamant est le 13e niveau dans la progression de la sarbacane sportive.
- Le disque de diamant est symbole de 500 000 albums vendus, en France.
Notes et références
- ↑ La classification des minéraux choisie est celle de Strunz, à l'exception des polymorphes de la silice, qui sont classés parmi les silicates.
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ Issu du privatif a et du verbe grec damazo signifiant « dompter ».
- ↑ Cet adjectif qualifie à l'origine l'état d'âme auquel tout homme se doit d'aspirer
- ↑ Définition diamantCentre National de Ressources Textuelles et Lexicales
- ↑ 161
- 1 2 Article adamas tiré du Dictionnaire des Antiquités grecques et romaines Daremberg et Saglio (1877)
- ↑ 982c (Luc Brisson n'est pas certain que l'on parle de diamant lorsque l'on évoque l'adamant, qu'il considère comme un métal
- ↑ (en)Diamonds Law & Legal Definition
- ↑ en grec ancien Περὶ Λίθων
- ↑ Pline L'Ancien (trad. Émile Littré), Histoire naturelle, vol. XXXVII : Au sujet des pierres précieuses, Paris, coll. « Collection des Auteurs latins », (lire en ligne), chap. XV
- ↑ E. Jannettaz, E. Fontenay, E. Vanderheym et A. Countance, Diamant et pierres precieuses, Editorial MAXTOR, (lire en ligne), p. 179
- ↑ (en) John Blair, English Medieval Industries : Craftsmen, Techniques, Products, Continuum International Publishing Group, (lire en ligne), p. 137
- ↑ (en) J. Willard Hershey, The Book Of Diamonds : Their Curious Lore, Properties, Tests And Synthetic Manufacture, Kessinger Publishing, (lire en ligne), p. 23-24
- ↑ (en) Nicholas D. Kristof, « Digging a Bucket of Diamonds a Day », sur New York Times,
- ↑ Les gisements dans la roche-mère même ne seront trouvés qu'à partir du XIXe siècle, lors de la ruée vers les mines de diamants de Kimberley
- ↑ (en)Richard W. Wise, « The Golconda Diamond », 2007
- 1 2 Marijan Dundek, Les Diamants, (lire en ligne), p. 11
- ↑ Claire König, « Diamants sur canapé ! », sur Futura-Sciences,
- ↑ (en) P. Daniel, « The carat - its origin as a unit of weight for diamond », Physics Education, vol. 7, no 7, , p. 454-455
- ↑ Le joailler flamand Lodewyk van Berken est considéré à tort par ses contemporains comme le père de la taille du diamant qu'il réalise en 1479.
- ↑ (en) George E. Harlow, The Nature of Diamonds, Cambridge University Press, (lire en ligne), p. 130
- ↑ (en) C.B. Smith et al., « Nature and genesis of Kalimantan diamonds », Lithos, vol. 112, no 822-832, (DOI 10.1016/j.lithos.2009.05.014)
- ↑ Le mythe du diamant
- ↑ (en) Joan Y. Dickinson, The Book of Diamonds, Courier Dover Publications, (lire en ligne), p. 5-12
- ↑ La fabuleuse histoire du diamant bleu, émission La Marche des Sciences, France Culture, 23 décembre 2010 : intervention de François Farges
- ↑ Isambert Decrusy, Recueil général des anciennes lois françaises, Volume 29, Berlin-Le-Prieur, (lire en ligne), p. 107
- ↑ En France jusqu'en 1792, les diamants étaient portés principalement par le roi.
- ↑ (en) Nikki van der Gaag, Trigger Issues : Diamonds, New Internationalist, (lire en ligne), p. 14
- ↑ Le diamant : Pierre des dieux, pierre de légendes !
- ↑ Franck Ferrand, « La malédiction du diamant bleu » dans l'émission Au cœur de l'histoire, 27 avril 2011
- ↑ L'histoire du diamant
- 1 2 Vincent Meylan, Bijoux de Reines, Assouline, , 205 p. (ISBN 2843233631)
- ↑ (en) R. M. Hazen, The diamond makers, Cambridge University Press, , 244 p. (ISBN 9780521654746, lire en ligne), p. 7-10
- ↑ Diamant Eureka
- ↑ J.-C. Michel, « Les diamants synthétiques ou de culture », Écomine, , p. 35-39 (lire en ligne)
- ↑ James E. Shigley, John Chapman et Robyn K. Ellison, « Discovery and Mining of the Argyle Diamond Deposit, Australia », Gems & Gemology, vol. 37, no 1, , p. 26-41 (DOI 10.5741/GEMS.37.1.26)
- ↑ (en) Site de l'American Museum of Natural history
- ↑ (en) N. Sobolev et V. S. Shatsky, « Diamond inclusions in garnets from metamorphic rocks: a new environment for diamond formation », Nature, vol. 343, no 6260, , p. 742-746 (ISSN 0028-0836 et 1476-4687, DOI 10.1038/343742a0)
- ↑ F. Brunet, D. Andrault et al., La Terre interne : Roches et matériaux en conditions extrêmes, Société géologique de France, coll. « Interactions », , 202 p. (ISBN 9782711753970, présentation en ligne), p. 110
- ↑ (en) Where does the carbon come from?, sur le site de l'American Museum of Natural History
- ↑ Dépêche ITAR-TASS du 16 septembre 2012
- ↑ AFP, « Une mine de diamants en Sibérie suscite tous les fantasmes », sur lesechos.fr, Les Échos, (consulté le 19 septembre 2012)
- ↑ Romain Renier, « Le cratère russe à 10 000 milliards de carats », sur latribune.fr, La Tribune, (consulté le 19 septembre 2012)
- ↑ Diamant du cratère Popigaï
- ↑ F. Denhez et V. Sautter, « Les diamants », La Recherche, no 343, (ISSN 0029-5671, lire en ligne)
- ↑ (en) T. L. Daulton, D. D. Eisenhour et al., « Genesis of presolar diamonds: Comparative high-resolution transmission electron microscopy study of meteoritic and terrestrial nano-diamonds », Geochim. Cosmochim. Acta, vol. 60, no 23, , p. 4853-4872 (ISSN 0016-7037, DOI 10.1016/S0016-7037(96)00223-2)
- 1 2 (en) World Mineral Production (2001-2005), British Geological Survey (ISBN 9780852725924, lire en ligne), « Production of diamond », p. 22
- 1 2 3 « Extraction - Exploitation minière », sur DiamAlps, (consulté le 22 avril 2015)
- ↑ Note du BRGM, 2008 :
- ↑ (en) J. H. Eggert, D. G. Hicks et al., « Melting temperature of diamond at ultrahigh pressure », Nat. Phys., vol. 6, no 1, , p. 40-43 (ISSN 1745-2473 et 1745-2481, DOI 10.1038/nphys1438)
- ↑ « back to basic: les diamants », sur La Recherche
- ↑ CVD pour Chemical Vapor Deposition où l'on fait croître un diamant, atome après atome, dans un plasma de carbone à haute température
- ↑ « La fabrication, l'artisanat diamantaire », sur DiamAlps (consulté le 26 avril 2015)
- ↑ Les diamants bruns
- ↑ « Histoire du diamant et sa commercialisation », DIAMPREST (consulté le 27 novembre 2010)
- 1 2 (en) « Optical Properties of Diamond: Type I & Type II Diamond », AllAboutGemstones.com,
- ↑ (en) « Diamond quality factors », sur GIA (consulté le 26 avril 2015)
- ↑ http://www.1-diamant.com/les-diamants-de-couleur/
- ↑ caractéristiques des diamants de couleurs|http://www.diamant-gems.com/french/differentes-couleurs-diamant.php
- ↑ « Les diamants et les pierres de couleur », sur Union française de la bijouterie, joaillerie, orfèvrerie, des pierres et des perles (consulté le 1er novembre 2011)
- ↑ P. Riché, « On a retrouvé le mythique « diamant bleu de la couronne » », Rue89, (lire en ligne)
- ↑ (en) « Guess Founder Georges Marciano Buys 84.37-Carat White Diamond for $16.2 Million at Auction », sur foxnews.com, Fox News Channel,
- ↑ « 18,7 millions d'euros pour un diamant », sur ouest-france.fr, Ouest-France,
- ↑ « Un diamant rose exceptionnel vendu pour 46 millions de dollars », TF1,
Articles connexes
- Carbonado (diamant noir)
- Diamite
- Carbure de silicium
- Carbure de tungstène
- Nitrure de bore
- Hétérodiamant
- Diamantaire
- Diamants de conflits
- Solitaire (bijou)
- Diamant et antidiamant, en mathématique
- BPM 37093
Diamants célèbres :
- Koh-i Nor
- Trône du Paon
- Martian Pink
- Grand Mogol
Liens externes
- Un dossier pluridisciplinaire sur les diamants
-
 « Le diamant :science, beauté, technologies de pointe et géopolitique » Enregistrement du cours dispensé par Daniel Demaiffe au Collège Belgique.
« Le diamant :science, beauté, technologies de pointe et géopolitique » Enregistrement du cours dispensé par Daniel Demaiffe au Collège Belgique. - Les diamants bruts naturels (Site de l'ENS de Lyon)
- Portail des minéraux et roches
- Portail de la chimie