Linus Pauling

| Naissance |
Portland, Oregon (États-Unis) |
|---|---|
| Décès |
(à 93 ans) Big Sur, Californie (États-Unis) |
| Nationalité | Américain |
| Pays de résidence |
|
| Diplôme |
Docteur du California Institute of Technology |
| Profession |
Chimiste et pacifiste |
| Distinctions |
Prix Nobel de chimie 1954 Prix Nobel de la paix 1962 |
Linus Carl Pauling ( à Portland, Oregon, États-Unis - à Big Sur, Californie) était un chimiste et physicien américain. Il fut l'un des premiers chimistes quantiques, et reçut le prix Nobel de chimie en 1954 pour ses travaux décrivant la nature de la liaison chimique[1]. Il publie en 1939 un ouvrage majeur La Nature de la liaison chimique (The Nature of the Chemical Bond) dans lequel il développe le concept d'hybridation des orbitales atomiques. Ses travaux sur les substituts de plasma sanguin (avec Harvey Itano) durant la Seconde Guerre mondiale, ainsi que ses recherches concernant l'anémie falciforme (ou drépanocytose qu'il qualifie du terme révolutionnaire de « maladie moléculaire ») ont grandement influencé la recherche en biologie pour la seconde moitié du XXe siècle. Il découvrira notamment la structure de l'hélice alpha (motif d'enroulement secondaire des protéines) et manquera de peu la découverte de la structure en double hélice de l'acide désoxyribonucléique (ADN). Il proposera en effet une structure en hélice triple, structure dont l'amélioration d'après l'étude de l'ADN par radiocristallographie aurait vraisemblablement pu l'amener à l'élaboration du modèle en double hélice proposé par James Dewey Watson et Francis Crick en 1953[2]. Il est l'un des fondateurs de la médecine orthomoléculaire et a popularisé l'utilisation de la vitamine C. Il décède le d'un cancer de la prostate.
Il reçut aussi le prix Nobel de la paix en 1962, pour sa campagne contre les essais nucléaires, devenant ainsi l'une des deux seules personnes à avoir reçu un prix Nobel dans deux catégories différentes (l'autre étant Marie Curie)[3].
Jeunesse

Pauling est né à Portland (Oregon) le . Il est le fils de Herman Henry William Pauling (1876-1910) de Concordia dans le Missouri (originaire d'Allemagne), et de Lucy Isabelle Darling (1881-1926)[4] de Lonerock dans l'Oregon. Son père, un pharmacien sans succès, déplace sa famille dans différentes villes de l'Oregon[5]. Quand il meurt en 1910 d'un ulcère perforé, la mère de Linus se retrouve seule pour l'élever lui et ses deux sœurs, Pauline Pauling (1901-2003) et Frances Lucille Pauling (1904-1992)[6]. La famille revient s'installer à Portland.
Dans son enfance, Linus Pauling est un lecteur vorace, au point que son père écrit un jour au journal local pour demander des suggestions de livres pour l'occuper[7]. Un de ses amis, Lloyd Jeffress, possède un petit laboratoire de chimie dans sa chambre, et les petites expériences menées dans ce laboratoire donnent à Pauling l'envie de devenir ingénieur chimiste[8].
Au lycée, Pauling continue d'effectuer des expériences de chimie en empruntant la plupart des matériaux et de l'équipement à une aciérie abandonnée proche du lieu où son grand-père travaille comme gardien de nuit.
Pauling échoue dans l'obtention de son diplôme en raison de résultats insuffisants en histoire des États-Unis. Son école lui décernera finalement le diplôme 45 ans plus tard, après l'obtention de ses deux prix Nobel[9].
Études

En 1917, Pauling entre à l'université agricole de l'Oregon à Corvallis (OAC, maintenant université d'État de l'Oregon)[10]. Du fait de ses besoins financiers, il doit travailler à plein temps en parallèle de ses études, notamment comme distributeur de lait, projectionniste et même sur un chantier naval[11]. À l'issue de sa deuxième année, il projette de chercher un emploi à Portland pour soutenir sa mère, mais l'université lui propose d'effectuer un enseignement d'analyse quantitative (un cours que lui-même vient de terminer) ce qui lui permet de continuer d'étudier à l'OAC[12].
Au cours de ses deux dernières années d'études à l'OAC, Pauling prend connaissance des travaux de Gilbert Newton Lewis et Irving Langmuir sur la configuration électronique des atomes et de la manière dont ils se lient pour former des molécules[12]. Il décide alors de concentrer sa carrière de chercheur sur la compréhension du rapport entre la structure des atomes constituant la matière et ses propriétés physiques et chimiques, ce qui le conduira par la suite à devenir l'un des pionniers d'une nouvelle discipline, la chimie quantique. À l'OAC, il a l'occasion d'effectuer ses premières recherches en travaillant sur l'effet d'un champ magnétique sur l'orientation de cristaux de fer.
En 1922, Pauling reçoit son Bachelor of Science de l'OAC en génie des procédés[13] et il poursuit ses études par un doctorat au California Institute of Technology (le Caltech) à Pasadena. Ses travaux de recherche concernent l'utilisation de la diffraction des rayons X pour la détermination de la structure des cristaux. Au cours de ses trois années au Caltech, il publie sept publications sur la structure cristalline de minéraux, la première d'entre elle, publiée dans Journal of the American Chemical Society concernant la structure de la molybdénite MoS2. Il reçoit son Ph.D. de chimie en 1925 summa cum laude.
Le 17 juin 1923, Pauling épouse Ava Helen Miller (1903-1981), qu'il a rencontrée lors de sa dernière année à l'OAC, et avec qui il aura trois fils et une fille.
Débuts de la carrière scientifique
À la suite de son Ph.D., Pauling obtient une bourse de la Fondation Guggenheim qui lui permet de voyager en Europe, où il travaille sous la direction d'Arnold Sommerfeld à Munich, rencontre brièvement Niels Bohr à Copenhague, mais échoue à rencontrer Erwin Schrödinger à Zurich, tous trois faisant partie des fondateurs et pionniers de la mécanique quantique que Pauling a eu l'occasion de découvrir au cours de ses études à l'OAC. Il a également l'occasion d'observer l'une des premières études de la liaison de la molécule d'hydrogène par la mécanique quantique, effectuée par Walter Heitler et Fritz London. Pauling consacre ses deux années en Europe à ces travaux et décide d'en faire le sujet principal de ses futures recherches. En 1927, il rentre aux États-Unis et obtient un poste de professeur assistant de chimie théorique au California Institute of Technology.
Pauling xommence sa carrière au Caltech par cinq années très productives, en appliquant la mécanique quantique à l'étude d'atomes et de molécules, tout en poursuivant ses études de cristaux par diffraction des rayons X. En cinq ans, il produit environ cinquante publications. En 1929, il est nommé professeur associé, puis il obtient le titre de professeur en 1930.
Durant l'été 1930, Pauling effectue un nouveau voyage en Europe, au cours duquel il travaille notamment dans l'institut d'Arnold Sommerfeld, et durant lequel il apprend la possibilité d'utiliser les électrons pour les études de diffraction, de la même manière qu'étaient utilisés jusque là les rayons X. À son retour, il construit un appareillage de diffraction des électrons, aidé par l'un de ses étudiants, L. O. Brockway, et l'utilise pour étudier la structure moléculaire d'un grand nombre de substances chimiques. En 1931, l'American Chemical Society lui décerne le prix Langmuir des travaux scientifiques les plus marquants effectués par un chercheur de moins de 30 ans[14].
En 1932, Pauling introduit la notion d'électronégativité. En utilisant plusieurs propriétés des molécules, notamment leur moment dipolaire et l'énergie nécessaire pour rompre des liaisons, il établit une échelle d'électronégativité (connue maintenant sous le nom d’échelle d'électronégativité de Pauling, utile pour la prédiction de la nature des liaisons chimiques) et associe une valeur d'électronégativité à la plupart des éléments chimiques. Cette même année, Pauling publie ce qu'il considère comme sa publication la plus importante, dans laquelle il développe pour la première fois le concept d'hybridation des orbitales atomiques et effectue une analyse du caractère tétravalent de l'atome de carbone[15]. Il présente notamment ces résultats dans un congrès au cours duquel il rencontre Albert Einstein.
Au Caltech, Pauling se lie d'amitié avec Robert Oppenheimer, qui travaille à Berkeley mais vient régulièrement à Pasadena effectuer des recherches et des enseignements. Les deux hommes projettent de faire équipe pour l'étude de la nature de la liaison chimique : Oppenheimer effectuerait les calculs mathématiques et Pauling interpréterait les résultats. Cependant cette relation prend fin lorsque Pauling commence à soupçonner Oppenheimer d'être trop proche de sa femme Ava Helen. Un jour que Pauling travaille, Oppenheimer se rend au foyer du couple et laisse échapper une invitation à Ava Helen pour un rendez-vous au Mexique. Celle-ci refuse mais rapporte l'incident à son mari. Cette invitation liée à la nonchalance d'Ava Helen au sujet de l'incident inquiète Pauling et il rompt sur-le-champ ses relations avec Oppenheimer, créant alors entre eux un froid qui durera jusqu'à la fin de leurs vies, et ce bien qu'Oppenheimer lui proposera par la suite de prendre la tête du département chimie du projet Manhattan (ce que Pauling refusera se présentant comme pacifiste).
La nature de la liaison chimique
Au début des années 1930, Pauling commence à publier ses travaux sur la nature de la liaison chimique, qui aboutissent à son fameux livre The Nature of the Chemical Bond en 1939. Ce livre est probablement l'un des plus importants livres de chimie jamais publiés[16]. Pour donner une idée de son influence, il suffit de remarquer que dans les 30 années qui ont suivi sa première édition en 1939, il a été cité plus de 16 000 fois ce qui en fait l'ouvrage le plus souvent cité dans la littérature scientifique. Au début du XXIe siècle, plus de soixante ans après sa publication, de nombreux articles scientifiques le citent encore. C'est principalement en récompense de ces travaux qu'il recevra le prix Nobel de chimie en 1954, « ses recherches sur la nature de la liaison chimique et leurs applications à la détermination de la structure de substances complexes[1] ».

Au cours de ses travaux sur la nature de la liaison chimique, Pauling introduit notamment le concept d'hybridation des orbitales atomiques[17]. Alors que les électrons dans les atomes sont décrits par des orbitales s, p, (…), il montre que pour décrire les liaisons au sein des molécules il est préférable de construire des fonctions qui sont des mélanges de ces orbitales. Par exemple, les orbitales 2p et 2s d'un atome de carbone peuvent se combiner pour former quatre orbitales équivalentes (appelées orbitales hybrides sp³) qui permettent mieux de décrire des composés comme le méthane, à géométrie tétraédrique. De même, l'orbitale 2s peut se combiner avec deux orbitales 2p pour former trois orbitales équivalentes (orbitales hybrides sp²) tandis que la troisième orbitale 2p ne s'hybride pas, ce qui permet de mieux décrire des composés insaturés comme l'éthylène.
L'un des autres domaines auquel il s'intéresse est la compréhension du rapport entre les liaisons ioniques, dans lesquelles les électrons sont transférés d'un atome à l'autre, et les liaisons covalentes, dans lesquelles les électrons sont mis en commun par les atomes. Il montre que ces deux types de liaison sont en réalité des cas extrêmes et que la plupart des liaisons sont en fait un mélange de liaison ionique et de liaison covalente. C'est dans ce domaine que la notion d'électronégativité qu'il développe est la plus utile : la différence d'électronégativité entre deux atomes s'avère être la grandeur la plus pertinente pour prédire le degré d'ionicité d'une liaison[18].
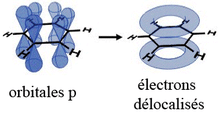
Le troisième sujet auquel travaille Pauling dans le domaine de la liaison chimique est la compréhension de la structure des composés aromatiques, et notamment du plus simple d'entre eux, le benzène[19].
Jusque là, la meilleure description de la structure du benzène avait été faite par le chimiste allemand Friedrich Kekulé von Stradonitz. Celui-ci avait décrit cette structure comme résultant de la transition rapide entre deux structures dans lesquelles les liaisons simples et doubles seraient alternées, les liaisons simples venant prendre la place des doubles et réciproquement. Pauling montre qu'une description intermédiaire entre les deux structures, basée sur la mécanique quantique, est plus pertinente : plutôt que deux structures en transition rapide, il s'agit plutôt de la superposition de deux structures. Ce phénomène sera plus tard baptisé du nom de résonance[20]. D'un certain côté, ce phénomène est analogue à celui d'hybridation des orbitales atomiques, puisqu'il consiste en la combinaison de plusieurs structures électroniques : les orbitales atomiques des différents atomes de carbone se combinent entre elles et forment des orbitales moléculaires.
Recherches en biologie moléculaire
Au milieu des années 1930, Pauling décide de s'intéresser à un nouveau domaine scientifique. Au début de sa carrière, il avait mentionné un manque d'intérêt pour l'étude des molécules biologiques. Mais le Caltech développant des compétences solides en biologie, Pauling a l'occasion d'y côtoyer des biologistes de renom comme Thomas Hunt Morgan, Theodosius Dobzhansky, Calvin Bridges ou Alfred Sturtevant et commence à s'intéresser à l'étude des molécules biologiques, notamment grâce à une bourse de la fondation Rockefeller. Ses premiers travaux dans le domaine concernent la structure de l'hémoglobine. Il parvient à montrer que cette structure change lorsque la molécule capte ou perd une molécule de dioxygène. À la suite de ce résultat, il décide d'étudier de manière plus précise la structure des protéines en utilisant la diffraction des rayons X. Cependant, la structure des protéines s'avère beaucoup plus difficile à déterminer par cette technique que celle des minéraux cristallisés auxquels il s'est intéressé précédemment. Dans les années 1930, les meilleurs clichés de rayons X de protéines ont été effectués par le cristallographe britannique William Astbury, mais lorsque Pauling essaie d'interpréter ses observations à l'aide de la mécanique quantique en 1937, il n'y parvient pas.
Il faut onze ans à Pauling pour comprendre l'origine du problème. Son analyse mathématique est correcte, mais les clichés d'Astbury ont été pris d'une manière telle que les protéines sont inclinées par rapport aux positions attendues. Pauling formule un modèle pour la structure de l'hémoglobine dans lequel les atomes étaient positionnés en hélice et avait appliqué ce concept de manière correcte aux protéines.
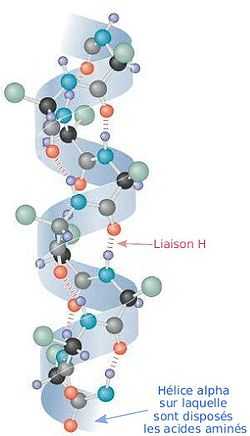
En 1951, sur la base de la structure des acides aminés et des peptides et de la planéité de la liaison peptidique, Pauling et ses collègues proposent l'hélice alpha[21] et le feuillet bêta comme motifs structuraux principaux de la structure secondaire des protéines. Ce résultat illustre la capacité de Pauling à penser de manière non conventionnelle : à la base de la structure se trouve l'idée selon laquelle un tour de l'hélice peut correspondre à un nombre d'acides aminés non entier.
Pauling propose alors une structure hélicoïdale pour l'ADN, mais il fait quelques erreurs dans la description de cette structure[22]. William Lawrence Bragg avait été déçu que Pauling gagne la course pour la découverte de l'hélice alpha : son équipe avait fait une erreur fondamentale en construisant un modèle des protéines sans prendre en compte la planéité de la liaison peptidique. Lorsqu'il apprend au Laboratoire Cavendish que Pauling travaille sur des modèles moléculaires de la structure de l'ADN, il autorise Watson et Crick à proposer un modèle moléculaire en utilisant des travaux non publiés de Maurice Wilkins et Rosalind Elsie Franklin du King's College of London. En 1953, James Dewey Watson et Francis Crick proposent une structure correcte pour la double hélice d'ADN, ce qui leur vaudra le prix Nobel de physiologie ou médecine en 1962. L'un des obstacles auxquels Pauling a dû faire face au cours de son travail est l'impossibilité de consulter les clichés de diffraction de l'ADN de bonne qualité pris par Rosalind Elsie Franklin auxquels Watson et Crick ont eu accès. Il a bien projeté de se rendre à un congrès en Angleterre durant lequel il aurait pu les voir, mais il n'a pas pu le faire, son passeport lui ayant été refusé par le département d'État américain pour des suspicions de sympathies communistes. Cette période marque le début du maccarthisme aux États-Unis.
Durant cette période, Pauling étudie également les réactions enzymatiques. Il est parmi les premiers à montrer que les enzymes agissent en stabilisant les états de transitions au cours des réactions, un comportement à la base de leur mécanisme d'action. Il est également parmi les premiers à proposer que la liaison entre les anticorps et les antigènes pourrait être due à des structures complémentaires. Dans le même ordre d'idée, il cosigne une publication avec le biologiste Max Delbrück qui suggère que la réplication de l'ADN trouve sa source dans des complémentarités structurales plutôt que dans des similarités, comme le proposent certains chercheurs. Le modèle de Watson et Crick viendra corroborer cette proposition. Par ailleurs, il contribue avec d'autres chercheurs à la fabrication d'anticorps artificiels et à celle d'un substitut de plasma sanguin.
Un positionnement moins connu et moins glorieux de Linus Pauling concerne les personnes hétérozygotes pour le gêne de la drépanocytose (porteur sain de la maladie) ; Linus en effet, écrit, en 1969, un article dans une revue de droit les propos suivants : "je suggère qu'on appose un symbole tatoué sur le front de chaque jeune personne porteuse du gène...celui chez qui on l'a trouvé en simple dose...Si cela était fait, deux jeunes gens portant le même gène, réellement délétère, seraient informés de la situation au premier coup d'oeil et se retiendraient de tomber amoureux l'un de l'autre...La législation dans le domaine, le dépistage avant le mariage et quelque forme de marque publique ou semi-publique de ce caractère, doivent être adoptés"[2]
Engagement politique
Jusqu'à la Seconde Guerre mondiale, Pauling n'a pas d'engagement politique. Au cours de la guerre, il contribue à la mise au point d'explosifs et de carburant pour missiles. Il met également au point un détecteur de niveau d'oxygène pour les sous-marins. Au commencement du Projet Manhattan, Robert Oppenheimer lui propose de prendre la tête du département de chimie du projet, proposition qu'il refuse. À la suite de ces contributions à l'effort de guerre américain, il recevra la médaille présidentielle du mérite en 1948 des mains de Harry Truman[23],[24]. Cependant, les bombardements de Hiroshima et Nagasaki le marquent profondément. En 1946, il rejoint le Comité d'urgence des scientifiques atomistes, dirigé par Albert Einstein[25], et dont le but est d'avertir l'opinion publique des dangers associés au développement des armes nucléaires. Son activisme politique conduit le Département d'État américain à lui refuser un passeport en 1952 lorsqu'il est invité à un congrès scientifique à Londres[26],[27]. Son passeport lui est rendu en 1954, peu avant la cérémonie lui attribuant son prix Nobel de chimie à Stockholm. En 1955, il signe le manifeste Russell-Einstein, en compagnie d'Einstein, de Bertrand Russell et de huit autres scientifiques et intellectuels de premier plan[28].
En 1957, Pauling lance une pétition en collaboration avec le biologiste Barry Commoner, qui a étudié la présence de strontium 90 radioactif dans les dents de lait des enfants et conclut que les essais nucléaires dans l'atmosphère présentent des risques pour la santé publique du fait des retombées radioactives[29],[30]. Il participe également à un débat public avec le physicien atomiste Edward Teller au sujet des risques réels de mutations causées par les retombées[31]. En 1958, Pauling et sa femme présentent aux Nations unies une pétition signée par plus de 11 000 scientifiques et appelant à l'arrêt des essais nucléaires. La pression de l'opinion publique conduit à un moratoire sur les essais en surface, suivi par la signature du traité d'interdiction partielle des essais nucléaires par John Fitzgerald Kennedy et Nikita Khrouchtchev. En 1963, le jour de l'entrée en vigueur du traité, le comité Nobel décerne à Pauling le prix Nobel de la paix pour 1962 (mis en réserve jusque-là), le décrivant comme « Linus Pauling, qui depuis 1946 a fait sans cesse campagne, non seulement contre les essais nucléaires, non seulement contre la prolifération des armes nucléaires, non seulement contre leur utilisation, mais contre l'usage des guerres comme moyen de résoudre des conflits internationaux. »[32] Le département de chimie du Caltech, circonspect devant ses engagements politiques, ne le félicite pas officiellement. En revanche, le département de biologie lui offre une petite réception, montrant ainsi sa sympathie pour son travail sur les mutations induites par les radiations. En 1964, il doit quitter son poste au Caltech sous la pression du conseil d'administration qui désapprouve ses engagements politiques. Il travaille alors successivement à San Diego de 1967 à 1969 et à l'université Stanford de 1969 à 1973.
Beaucoup des détracteurs de Pauling, parmi lesquels des scientifiques appréciant ses travaux de chimie, sont en désaccord avec ses positions politiques et se le représentent comme un porte-parole naïf du communisme soviétique. En 1955, il est cité à comparaître devant le Sous-comité pour la sécurité intérieure du Sénat, qui le décrit comme « la personnalité scientifique numéro un dans toutes les activités importantes de l'offensive pacifiste communiste dans le pays » . Il sera convoqué plusieurs fois devant cette commission, notamment après la pétition contre les essais nucléaires. Le magazine Life décrit en une son prix Nobel de la paix comme « A Weird Insult from Norway » (« une étrange insulte de la part de la Norvège »). En 1970, Pauling est lauréat du prix Lénine pour la paix décerné par l'URSS.
Jusqu'à la fin de sa vie, il se sert de sa notoriété pour s'élever contre les conflits armés, depuis des protestations contre la guerre du Viêt Nam, jusqu'à un « appel pour la paix en Croatie » en 1991. Il est également un critique féroce de l'interventionnisme américain en Amérique latine, notamment au Nicaragua.
Autres travaux
Voiture électrique

À la fin des années 1950, Pauling commence à s'intéresser au problème de la pollution de l'air, en particulier à cause du phénomène du smog en pleine croissance à Los Angeles. À cette époque, la plupart des scientifiques pensent que le smog est dû aux rejets des usines chimiques et des raffineries. Les travaux de Pauling, Arie Haagen-Smit et d'autres scientifiques du Caltech montrent qu'il est dû à la pollution automobile. Peu après cette découverte, Pauling commence à travailler sur la mise au point d'une voiture électrique censée être fonctionnelle et bon marché. Pour ce faire, il joint ses efforts à ceux des ingénieurs de l'entreprise Eureka Williams pour le développement de la première voiture électrique à vitesse contrôlable, la Henney Kilowatt. Après avoir travaillé sur le système de propulsion, Pauling montre que les batteries classiques acide-plomb ne peuvent pas fournir une puissance suffisante pour que les performances de la voiture électrique puissent rivaliser avec celles des voitures à essence. Il prévoit que la faible vitesse de pointe et la faible autonomie de la Henney Kilowatt la rendront peu fonctionnelle et peu populaire. Il insiste auprès de Eureka Williams pour attendre d'avoir développé une voiture plus fonctionnelle avant de la proposer au public, et recommande d'interrompre le projet le temps que des batteries plus performantes soient disponibles sur le marché. Cependant, l'entreprise préfère lancer la production de la voiture, et celle-ci conduit à un échec commercial.
Médecine et vitamines
En 1941, Pauling, âgé alors de 40 ans, découvre qu'il est atteint d'une forme grave de la maladie de Bright, une maladie des reins potentiellement mortelle que les médecins considèrent à l'époque comme incurable. Avec l'aide du Dr Thomas Addis (en) de Stanford, il parvient à contrôler l'évolution de la maladie en suivant un régime faible en protéines et sans sel, inhabituel pour l'époque. Comme tous les patients d'Addis, il se voit également prescrire des vitamines et des sels minéraux.
À la fin des années 1950, Pauling étudie l'action des enzymes sur les fonctions cérébrales. Il pense que les maladies mentales pourraient être en partie causées par des dysfonctionnements enzymatiques. Lorsqu'il lit la publication d'Abram Hoffer (en) de 1965, Utilisation de la vitamine B3 en psychiatrie, il se rend compte que les vitamines pourraient avoir des effets biochimiques importants en plus de ceux liés à la prévention des maladies liées à leurs carences. En 1968, il publie dans Science sa publication la plus importante dans ce domaine : Orthomolecular psychiatry. […] (), dans laquelle il invente le mot « orthomoléculaire » pour décrire le concept de contrôle de la concentration des composés présents dans le corps humain pour prévenir et guérir les maladies.
Vitamine C, rhume et cancer
Les recherches effectuées par Pauling au cours des années suivantes sur la vitamine C génèrent des controverses. Lorsqu'il découvre le concept de cures de vitamine C à hautes doses développé par le biochimiste Irwin Stone en 1966, il commence à en prendre plusieurs grammes par jour en prévention des rhumes. Enthousiasmé par les résultats, il s'intéresse à la littérature sur le sujet et publie Vitamin C and the Common Cold en 1970. En 1971, il commence une longue collaboration avec le cancérologue écossais Ewan Cameron (en) au sujet de l'utilisation de la vitamine C en injection intraveineuse ou par voie orale pour le soin de malades du cancer en phase terminale. Cameron et Pauling écrivent de nombreuses publications ainsi qu'un livre de vulgarisation, intitulé Vitamine C et cancer, qui décrivent leurs observations. Malgré des résultats qui semblent favorables, la campagne de publicités négatives menée à son encontre sape la crédibilité de Pauling et de ses travaux sur la vitamine C pour de nombreuses années. Toujours sur la corde raide depuis sa campagne de lutte contre les essais nucléaires en surface des années 1950 menée sur la base de la biologie moléculaire, Pauling se retrouve en 1985 privé de ses sources de financements institutionnelles et du soutien de ses pairs. Il collabore tout de même ensuite avec le biochimiste et médecin canadien Abram Hoffer (en) sur un régime incluant de la vitamine C à haute dose comme traitement d'appoint du cancer.
De fait, Pauling est le promoteur de l'idée selon laquelle des doses élevées et étalées dans le temps de vitamine C seraient efficaces contre les rhumes et autres maladies, ce qui est encore controversé de nos jours (QuackWatch[33], Plos[34], WebMD[35]). La méta-analyse la plus récente (janvier 2013) du groupe Cochrane[36] offre une conclusion mitigée. Elle différencie l'utilisation au long cours, la prise lors d'épisodes de stress répétés (entraînement sportif intense, activités militaires) et l'administration ponctuelle lors d'un rhume. Ainsi le groupe Cochrane recommande une approche individuelle et rappelle la nécessité de nouveaux essais contrôlés randomisés.
Les injections de vitamine C par voie intraveineuse pourrait avoir un effet positif pour le traitement de certaines formes de cancer[37], ce qui reste encore controversé[38]. Des études cliniques sont en cours à l'heure actuelle pour tenter de déterminer les effets exacts[39].
En 1973, Pauling et deux de ses collègues fondent un institut de médecine orthomoléculaire à Menlo Park en Californie, rapidement rebaptisé Institut de sciences et de médecine Linus Pauling. Il y dirige des recherches sur la vitamine C, mais poursuit également ses travaux théoriques en chimie et physique jusqu'à sa mort en 1994. Au cours de ses dernières années, il s'intéresse particulièrement au rôle éventuel de la vitamine C dans la prévention de l'artériosclérose, et publie trois rapports sur l'utilisation de la vitamine C et de la lysine pour soulager l'angine de poitrine.
Pendant plusieurs années, le principal donateur de l'institut était le groupe pharmaceutique Hoffmann-La Roche, qui produisait le plus de vitamine C dans le monde. Plusieurs dépliants des campagnes de collecte de fonds de l'institut contenaient des renseignements douteux. Durant les années 1980, par exemple, il y était faussement affirmé qu'aucun progrès n'avait été fait dans le traitement du cancer dans les vingt dernières années[40]. En 1996, deux ans après sa mort, l'Institut Linus Pauling déménage pour Corvallis (Oregon) où il fait maintenant partie de l'université d'État de l'Oregon.
Prix et distinctions
Pauling fut lauréat à la fois du prix Nobel de chimie (le 3 novembre 1954)[41] et du prix Nobel de la paix en 1962.
Il fait donc partie des quatre seules personnes, avec Marie Curie, John Bardeen et Frederick Sanger, à avoir reçu deux prix Nobel. Marie Curie et Linus Pauling sont les deux seules personnes ayant reçu leurs prix Nobel dans deux catégories différentes. Linus Pauling est le seul à n'avoir partagé aucun de ses deux prix avec une autre personne.
Linus Pauling a également été lauréat d'un grand nombre de prix et de distinctions honorifiques, notamment :
- 1933 : membre de l'Académie des sciences des États-Unis
- 1936 : membre de l'American Philosophical Society
- 1946 : lauréat de la médaille Gibbs de l'American chemical society, section de Chicago
- 1947 : lauréat de la médaille Davy de la Royal Society
- 1948 : membre étranger de la Royal Society de Londres[42]
- 1951 : lauréat de la médaille Lewis de l'American chemical society, section de Californie
- 1960 : « homme de l'année » dans Time Magazine
- 1962 : lauréat du prix Gandhi pour la paix
- 1970 : lauréat du prix Lénine pour la paix
- 1974 : lauréat de la National Medal of Science, remise par le président Gerald Ford
- 1977 : lauréat de la médaille Lomonosov de l'Académie des sciences de Russie
- 1979 : premier lauréat de la médaille de chimie de l'Académie des sciences des États-Unis
- 1984 : lauréat de la médaille Priestley de l'American chemical society
Il fut également nommé docteur honoris causa des universités d'Oregon, Chicago, Princeton, Londres, Cambridge, Sheffield, Yale, Oxford, Paris, Tampa, Toulouse, Liège, Montpellier, Bruxelles, Cracovie[43], Melbourne, Delhi, Lyon…
Héritage et postérité
La contribution de Pauling aux développements de la science du XXe siècle est exceptionnelle. Avec Albert Einstein, il est le seul chercheur du XXe siècle à figurer sur la liste des 20 plus grands scientifiques de tous les temps du magazine britannique New Scientist. Gautam R. Desiraju, l'auteur de l'éditorial du millénaire dans Nature[44], y écrit que Pauling a été l'un des plus grands penseurs et visionnaires du millénaire avec Galilée, Newton et Einstein.
Pauling est également exceptionnel pour la diversité de ses travaux : mécanique quantique, chimie inorganique, chimie organique, biochimie, biologie moléculaire et médecine. Ses contributions ont été très importantes dans chacune de ces disciplines et davantage encore aux frontières entre ces disciplines. Ses travaux sur la nature de la liaison chimique ont marqué les débuts de la chimie quantique, et certaines des notions dont il est l'initiateur comme l'électronégativité et l'hybridation des orbitales atomiques sont à la base de la chimie moderne, même si l'hybridation a été supplantée par la théorie des orbitales moléculaires de Robert Mulliken. Ses travaux sur la structure des cristaux ont contribué aux progrès dans la prédiction et la compréhension de structures de minéraux[note 1]. Sa découverte de l'hélice alpha et du feuillet bêta est à la base de la compréhension de la structure de l'ADN. À son époque, Pauling était fréquemment considéré comme le fondateur de la biologie moléculaire[45].
Publications
- (en) The Nature of the Chemical Bond, Cornell University Press (ISBN 0-8014-0333-2) ;
- (en) Avec E. B. Wilson, Introduction to Quantum Mechanics with Applications to Chemistry, Dover Publications (ISBN 0-486-64871-0) ;
- (en) Avec E. Cameron, Cancer and Vitamin C: A Discussion of the Nature, Causes, Prevention, and Treatment of Cancer With Special Reference to the Value of Vitamin C, Camino Books (ISBN 0-940159-21-X) ;
- (en) How to Live Longer and Feel Better, Avon Books (ISBN 0-380-70289-4) ;
- (en) Linus Pauling On Peace - A Scientist Speaks Out on Humanism and World Survival, Rising Star Press (ISBN 0-933670-03-6) ;
- (en) General Chemistry, Dover Publications (ISBN 0-486-65622-5) ;
- Avec Daisaku Ikeda, Toute une vie à la recherche de la paix, Éditions du Rocher, 2003 (ISBN 2-268-04549-8) ;
- (en) Sélection de publications scientifiques au format PDF.
Notes et références
Notes
- ↑ De nos jours, son opposition aux quasicristaux apparait comme une erreur de jugement, mais elle a amené les partisans de cette découverte à élaborer plus finement leurs données et la théorie correspondante.
Références
- (de) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en allemand intitulé « Linus Carl Pauling » (voir la liste des auteurs).
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Linus Pauling » (voir la liste des auteurs).
- 1 2 (en) « or his research into the nature of the chemical bond and its application to the elucidation of the structure of complex substances » in Personnel de rédaction, « The Nobel Prize in Chemistry 1954 », Fondation Nobel, 2010. Consulté le 18 août 2010
- 1 2
- Pauling L. 1969. Reflections on a New Biology:Forword. UCLA law Review 15 (2) 267-272.
- Il également possible qu'il n'ait pas eu connaissance des défauts des formes tautomériques présentées dans l'ouvrage de J. N. Davidson, The Biochemestry of Nucleid Acids. Le cristallographe américain Jerry Donohue avait en effet signalé à James Watson que ces reproductions étaient erronées (voir La Double Hélice, Paris, Laffont, Coll. « Pluriel », (trad. en 1968), p. 198).
- ↑ (en) Nobel Laureates Facts
- ↑ (en) Thomas Hager, Force of Nature: The Life of Linus Pauling, Simon & Schuster, (ISBN 0684809095), p. 22
- ↑ Goertzel et Goertzel 1995, p. 5
- ↑ (en) Clifford Mead et Thomas Hager, Linus Pauling: Scientist and Peacemaker, Oregon State University Press, (ISBN 0870714899), p. 9
- ↑ (en) Jack D. Dunitz, Linus Carl Pauling, 28 February 1901–19 August 1994, 1996, Biographical Memoirs of Fellows of the Royal Society vol.42, pages=316–338, DOI:10.1098/rsbm.1996.0020
- ↑ Goertzel et Goertzel 1995, p. 17
- ↑ (en) Biographie de Linus Pauling
- ↑ Goertzel et Goertzel 1995, p. 22
- ↑ Goertzel et Goertzel 1995, p. 23-24
- 1 2 Goertzel et Goertzel 1995, p. 29
- ↑ (en) Linus Carl Pauling: A Biographical Timeline
- ↑ The Langmuir Prize, Tom Hager, décembre 2004, Oregon State University Libraries Special Collections
- ↑ The nature of the chemical bond. III. The transition from one extreme bond type to another., Linus Pauling, mars 1932, Journal of the American Chemical Society
- ↑ The Nature of the Chemical Bond, Thomas Hager, décembre 2004, Oregon State University Libraries Special Collections
- ↑ London's paper. General ideas on bonds, Linus Pauling, 1928, Oregon State University Libraries Special Collections.
- ↑ Notes and Calculations re: Electronegativity and the Electronegativity Scale, Linus Pauling, 1930, Oregon State University Libraries Special Collections.
- ↑ Benzene, Linus Pauling, 06-01-1934, Oregon State University Libraries Special Collections.
- ↑ Resonance, Linus Pauling, 29-07-1946, Oregon State University Libraries Special Collections.
- ↑ (en) L Pauling, RB Corey et HR Branson, « The structure of proteins : two hydrogen-bonded helical configurations of the polypeptide chain », Proc. Natl. Acad. Sci. USA, vol. 37, , p. 205-211 (PMID 14816373)
- ↑ Linus Pauling's DNA Model
- ↑ The Linus Pauling Papers: Biographical Information, dans United States National Library of Medicine.
- ↑ Pauling's Prizes, John Allen Paulus, dans le New York Times, 5 novembre 1995.
- ↑ Einstein, Thomas Hager, Oregon State University Libraries Special Collections.
- ↑ Linus Pauling
- ↑ The Department of State and the Structure of Proteins, Linus Pauling, mai 1952, Oregon State University Libraries Special Collections.
- ↑ Russell/Einstein, Thomas Hager, Oregon State University Libraries Special Collections
- ↑ Strontium-90 Thomas Hager, Oregon State University Libraries Special Collections.
- ↑ The Right to Petition, Thomas Hager, Oregon State University Libraries Special Collections
- ↑ Teller vs. Pauling, Linus Pauling, Oregon State University Libraries Special Collections
- ↑ Notes by Linus Pauling. October 10, 1963, Linus Pauling, Oregon State University Libraries Special Collections.
- ↑ Le site quackwatch.org présente une méta-analyse (1997) de Charles W. Marshall niant les effets de la vitamine C.
- ↑ Plos publie une méta-analyse australienne (2005) confirmant les effets bénéfique de la vitamine C. Plos
- ↑ Une étude de 2007 WebMD montre un effet curatif immédiat en regardant les effets de la vitamine C sur les cellules immunitaires.
- ↑ La méta-analyse Cochrane actualisée
- ↑ Publications sur le site du centre The Bright Spot For Health qui montreraient un effet positif de la vitamine C pour lutter contre le cancer.
- ↑ Résumé de la controverse
- ↑ L'étude en cours
- ↑ http://www.johnweisnagelmd.com/pauling.html
- ↑ http://www.universalis.fr/encyclopedie/linus-carl-pauling/
- ↑ (en) [PDF] List of fellows of the Royal Society, 1600-2007. K-Z, p. 80
- ↑ (pl) Doktorzy honoris causa, sur le site de l'université jagellonne de Cracovie
- ↑ (PMID 11100703)
- ↑ Crick, Francis. « The Life and Work of Linus Pauling (1901-1994): A Discourse on the Art of Biography » : « How should we summarize Linus' contribution? […] he was one of the founders of molecular biology. […] In addition, therefore, to his enormous contributions to chemistry and his humanitarian work, I think we should celebrate him as one of the founders of molecular biology […] »
Annexes
Bibliographie
- Thomas Hager :
- (en) Force of Nature : The Life of Linus Pauling, Simon & Schuster, 1995 (ISBN 978-0-684-80909-0),
- (en) Linus Pauling and the Chemistry of Life, Oxford University Press, 1998 (ISBN 0-19-513972-0),
- (en) avec Clifford Mead, Linus Pauling : Scientist and Peacemaker, Oregon State University Press, 2001 (ISBN 0-87071-489-9) ;
- Barbara Marinacci :
- (en) Linus Pauling in His Own Words: Selections from His Writings, Speeches, and Interviews, Touchstone Books, 1995,
- (en) Avec Ramesh Krishnamurthy, Linus Pauling on Peace, Rising Star Press, 1998 (ISBN 0-933670-03-6) ;
- (en) Ted Georges Goertzel et Ben Goertzel, Linus Pauling: a life in science and politics, Basic Books, (ISBN 9780465006724) ;
- (en) Anthony Serafini, Linus Pauling : A Man and His Science, Paragon House, 1989 (ISBN 1-55778-440-X) ;
- Mohamed Larbi Bouguerra (dir.), Linus Pauling, Belin, 2002 (ISBN 2-7011-2658-4).
Articles connexes
- Règles de Pauling
- Matthias Rath
- Médecine orthomoléculaire
- Irwin Stone
Liens externes
- (en) Biographie sur le site de L'Institut Linus Pauling
- (en) Biographie sur le site de la Fondation Nobel (la page propose plusieurs liens relatifs à la remise du prix, dont un document rédigé par le lauréat — le Nobel Lecture — qui détaille ses apports)
- (en) Fond Linus et Ava Pauling de l'université de l'Oregon
- (en) The Pauling Catalogue
- Notices d’autorité : Fichier d’autorité international virtuel • International Standard Name Identifier • Bibliothèque nationale de France • Système universitaire de documentation • Bibliothèque du Congrès • Gemeinsame Normdatei • Bibliothèque nationale de la Diète • WorldCat
- Portail de la chimie
- Portail du prix Nobel
- Portail de la médecine
- Portail de la physique
- Portail des États-Unis
- Portail de Portland
