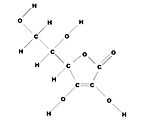
Vitamine C
| Vitamine C | |
|---|---|
   | |
| Identification | |
| Nom UICPA | (R)-3,4-dihydroxy-5-((S)-1,2-dihydroxyéthyl)furan-2(5H)-one |
| Synonymes | Acide L-ascorbique |
| No CAS | |
| No EINECS | |
| Code ATC | A11 |
| No E | E300 |
| FEMA | |
| SMILES | |
| InChI | |
| Apparence | Poudre ou cristaux blancs à légèrement jaune, inodore[1] |
| Propriétés chimiques | |
| Formule brute | C6H8O6 [Isomères] |
| Masse molaire[2] | 176,1241 ± 0,0072 g/mol C 40,92 %, H 4,58 %, O 54,5 %, |
| pKa | 4,70 (10 °C)[1] |
| Propriétés physiques | |
| T° fusion | 190 à 192 °C (décomposition)[1] |
| Solubilité | 0,33 g·ml-1 (eau), 0,033 g·ml-1 (éthanol 95 %), |
| Masse volumique | 1,65[1] |
| Pression de vapeur saturante | 7,9179 Pa à 465,15 K[1] |
| Point critique | 509,85 °C 5,29×106 Pa[1] |
| Propriétés optiques | |
| Indice de réfraction | 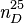 1,5101-1,5204[1] 1,5101-1,5204[1] |
| Spectre d’absorption | Absorption max : 245 nm (solution acide), |
| Pouvoir rotatoire | 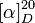 +24° (10 g·l-1 eau), +24° (10 g·l-1 eau),
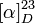 +48° (10 g·l-1 méthanol)[1] +48° (10 g·l-1 méthanol)[1] |
| Précautions | |
Phrases S : 24/25,
| |
| Écotoxicologie | |
| LogP | -2,15 à 23 °C, -2,00 à 37 °C[1] |
La vitamine C est une vitamine hydrosoluble sensible à la chaleur et à la lumière jouant un rôle important dans le métabolisme de l'être humain et de nombreux autres mammifères. Chimiquement parlant, il s'agit de l'acide L-ascorbique, un des stéréoisomères de l'acide ascorbique, et de ses sels, les ascorbates. Les plus courants sont l'ascorbate de sodium et l'ascorbate de calcium).
Propriétés chimiques
Voir Acide ascorbique.
Action chez l'humain
La vitamine C est un cofacteur enzymatique impliqué dans un certain nombre de réactions physiologiques (hydroxylation). Elle est requise dans la synthèse du collagène et des globules rouges et contribue au système immunitaire[3]. Elle joue également un rôle dans le métabolisme du fer en tant que promoteur de son absorption; son utilisation est donc déconseillée chez les patients porteurs d'une surcharge en fer et particulièrement d'une hémochromatose. Sous forme oxydée (acide déshydroascorbique), elle traverse la barrière hémato-encéphalique pour accéder au cerveau[4] et à plusieurs organes à forte concentration en vitamine C. Les muscles squelettiques répondent rapidement à la prise de vitamine C, mais la perdent également rapidement si l'apport de la vitamine est insuffisant[5]. Il s'agit d'un antioxydant, molécule capable de contrer l'action néfaste d'oxydants comme les radicaux. À cet effet, on emploie également l'acide-D-ascorbique qui, à l'inverse de l'acide-L-ascorbique, ne présente pas d'activité vitaminique.
Conservation
Très fragile en solution, elle est détruite au contact de l'air (par oxydation) ou sous l'exposition à la lumière (par action des ultraviolets) et la chaleur accélère ces processus. La chaleur de la cuisson des aliments détruit la vitamine C[6],[7].
Synthèse
Alors que la plupart des mammifères sont capables de la synthétiser dans leur foie ou dans leurs reins (ce n'est donc pas une vitamine pour eux), la majorité des primates (dont l'être humain), le cochon d'Inde et certains oiseaux et poissons en sont incapables. Ceci serait le résultat d'une mutation génétique, survenue il y a 40 millions d'années, bloquant la transformation du glucose en acide ascorbique. Les animaux dépourvus de cette capacité de synthèse de la vitamine C doivent donc la puiser dans leur alimentation.
Plusieurs hypothèses ont été formulées pour expliquer la perte, chez l'ancêtre de l'humain et des grands singes, de la capacité à produire la vitamine C. Richard J. Johnson, un spécialiste des maladies cardio-vasculaires, et de l'uricémie humaine (une autre erreur génétique pratiquement caractéristique des grands primates, dont l'Humain), suggère que l'acide urique et le manque de vitamine C, deux facteurs pro-inflammatoires, auraient accordé un avantage évolutif en promouvant la rétention des graisses (effet reconnu du stress oxydatif et de l'inflammation), utile durant les famines de l'Éocène tardif et du Miocène moyen, contemporaines de ces mutations génétiques[8].
Apports conseillés
Apports journaliers recommandés
Les recommandations européennes conseillent un apport quotidien de 75 mg pour une femme et de 90 mg pour un homme. À titre d'exemple, une orange apporte en moyenne 53 mg de vitamine C (40 à 80 mg par 100 g).

En France, l'AFSSA recommande un apport quotidien de 110 mg pour un adulte de 20 à 60 ans[9]. Les personnes exposées davantage aux effets nocifs des oxydants, comme les fumeurs, ont des besoins accrus en vitamine C (125 mg selon le Conseil supérieur d'hygiène de Belgique)[10]. Certains scientifiques, comme Linus Pauling (prix Nobel de chimie en 1954), considèrent que les apports nutritionnels recommandés devraient être d'au moins 6 000 mg, voire 18 000 mg[11].
Chez les primates en liberté, les analyses nutritionnelles font état d'une consommation quotidienne de 2 000 à 8 000 mg par jour[12] pour des primates d'un poids comparable (chimpanzés) ou légèrement supérieur (gorilles) à celui de l'homme. On recommande 25 mg de vitamine C par kilogramme de poids chez tous les primates en captivité, soit, pour un chimpanzé de poids moyen (70 kg), 1 750 mg par jour[13].
Les vétérinaires des NAC recommandent 20 mg de vitamine C pour les cochons d'Inde et 30 à 60 mg pour les femelles gestantes[14],[15], soit à peu près la moitié de l'apport recommandé pour un être humain ayant une masse corporelle 80 fois plus élevée (la masse corporelle moyenne du cochon d'Inde adulte est de 1 kg, celle de l'humain de sexe masculin varie autour de 80 kg).
Carence
Une importante carence en vitamine C, très rare, provoque le scorbut, lorsque l'apport est de moins de 10 mg par jour. Les hypovitaminoses plus discrètes sont très répandues et se traduisent par de l'asthénie, un amaigrissement, des maux de tête, des douleurs osseuses, une plus grande sensibilité aux infections et parfois des problèmes hémorragiques[16].
Toxicité
La vitamine C est non toxique aux doses usuellement absorbées pour un individu en bonne santé.
Depuis sa synthèse dans les années 1930, la vitamine C est utilisée à toutes les doses à travers le monde. Les seuls effets secondaires associés à son utilisation et qui soient établis sont la diarrhée bénigne et une action diurétique. Celles-ci surviennent lorsqu'elle est consommée trop rapidement et en trop grande quantité. L'organisme ne pouvant la stocker, il en élimine ainsi l'excès.
Des études cliniques montrent :
- que la consommation de vitamine C n'augmente pas[17],[18],[19] et même réduit[20] l'incidence de calculs rénaux ;
- que la vitamine C n'a pas d'effet mutagène (étude sur des doses allant jusqu’à 5 000 mg par jour)[21],[22].
Les études in vivo montrent que la vitamine C, même en présence de métaux de transition n'a pas d'effet mutagène et qu'au contraire elle protège les cellules de l'action mutagène du peroxyde d'hydrogène[23].
Les symptômes d'un surdosage en vitamine C peuvent être : (et/ou) nausée, vomissements, céphalées, éruptions cutanées, asthénie[24].
Pour des doses supérieures à 500 mg/j, une augmentation de production d'acide oxalique pourrait induire un risque de calculs rénaux d'oxalate[25],[26]. Cet effet secondaire est controversé par certaines études[27]. En effet, les végétaux qui apportent de la vitamine C apportent aussi des oxalates[28], d'où la confusion.
Usages thérapeutiques
En tant que traitement médical, la vitamine C a quelques indications reconnues[29] : la prévention ou le traitement du scorbut, l'avitaminose C, la méthémoglobinémie idiopathique du nourrisson et la méthémoglobinémie chez les sujets déficients en G6PD.
Il s'agit d'une molécule utilisée couramment en automédication : plus de 10 % des Américains en consomment[30].
En décembre 2007, la cour d'appel de Poitiers a estimé que les produits à base de vitamine C 500 et C 180 devaient être considérés comme des médicaments par fonction, restreignant ainsi leur distribution au sein des officines de pharmacie. Cette décision s'appuyait sur une interprétation de l’article 5111-1 du code français de la santé publique. Cependant, la cour de cassation a annulé cette décision en janvier 2009. En effet, celle-ci a estimé que la cour d'appel avait privé sa décision de base légale en ne procédant pas à l'examen de l’ensemble des caractéristiques du produit, comme l'indique une jurisprudence de la Cour de justice des Communautés européennes[31],[32]. De fait, il n'est pas dit si la vitamine C est un médicament ou pas. Simplement l'arrêt interdisant la commercialisation a été annulé car la détermination de son appartenance à la classe des médicaments n'a pas été faite conformément à la jurisprudence communautaire.
Épuisement et fatigue
La vitamine C administrée par voie intraveineuse soulagerait la fatigue en deux heures, effet qui s'est prolongé au moins jusqu'au jour suivant l'administration, ce qui est notable étant donné que la pharmacocinétique de la vitamine C par voie intraveineuse prédit une augmentation des concentrations sanguines de vitamine C pendant seulement quatre à six heures. Le stress oxydatif, tel qu'évalué par la méthode Free Oxygen Radicals Test (FORT), a également diminué[33].
Par voie orale, une dose modérée de vitamine C (500 mg) pourrait diminuer les sensations de fatigue et d'effort chez des personnes obèses suivant un régime hypocalorique[34].
Une idée reçue voudrait que la vitamine C empêche de dormir mais cela pourrait s'avérer inexact[35].
C'est la supplémentation ponctuelle suivant un long déficit qui provoquerait cet effet[réf. nécessaire], une supplémentation suffisante à plus long terme aurait même l'effet contraire c'est-à-dire aiderait à s'endormir[réf. souhaitée].
Rhume
Cette vitamine est largement utilisée en automédication dans le rhume banal. Elle semble raccourcir la durée des symptômes et les améliorer, du moins chez l'adulte, l'efficacité chez l'enfant semblant non démontrée[36].
Dans les années 1970, l'Américain Linus Pauling (prix Nobel de chimie en 1954 et prix Nobel de la paix en 1962) préconisait 1 g de vitamine C par heure dès les premiers symptômes pour faire régresser l'infection. Mais aujourd’hui, les études tendent à montrer que la vitamine C n'a pas d'effet préventif contre le rhume[37]. Certains auteurs observent que les méta-analyses, telles que celle de la Collaboration Cochrane de 2004[38], qui n'incluent que des études où la vitamine n'a été administrée qu'une fois par jour, ne réfutent pas les affirmations de Pauling[39]. Depuis 2013, le groupe Cochrane reconnaît que des essais randomisés sont nécessaires et recommande, malgré cela, la supplémentation, étant donné son faible coût, les bienfaits potentiels et le poids de la preuve accumulée[40].
Vitamine C et plomb
En 1939, on a signalé que 34 travailleurs ayant absorbé du plomb avaient été traités au moyen de la vitamine C[41]. Récemment, une étude sur des animaux a montré que la vitamine C avait un effet protecteur contre l’intoxication au plomb sur les plans des fonctions nerveuses et musculaires[42]. Chez des fumeurs, l’administration de 1 000 mg de vitamine C a permis une réduction moyenne de 81 % des concentrations sanguines de plomb, tandis que 200 mg sont restés sans effet. Les auteurs ont donc conclu que la supplémentation de vitamine C pourrait représenter une façon économique et pratique de faire baisser les concentrations de plomb dans le sang. Une étude publiée dans le journal de l’association médicale américaine conclut que, si le lien de causalité était bien démontré, la corrélation inverse entre le plomb et la vitamine C dans le sang constatée dans une enquête d’envergure nationale, aurait un impact sur le plan de la santé publique en général[43].
Syndrome d’immunodéficience acquise (SIDA)
Une des maladies dont le traitement éventuel par des doses pharmacologiques d’ascorbate est le plus controversé est le SIDA. La controverse dure depuis plus de 16 ans, c’est-à-dire depuis la publication d’une étude tendant à montrer que l’ascorbate, en doses non toxiques pour l’homme, arrêtait la réplication du VIH, dans le journal Proceedings of the National Academy of Sciences des États-Unis[44]. D’autres études des mêmes auteurs ont suivi et ont étayé ces résultats[45],[46],[47], mais aucune étude clinique d’envergure n’a été entreprise.
Cancer
Dans le cadre du traitement contre le cancer, Linus Pauling s'inspirant des travaux d'Irwin Stone, donne l'idée d'un apport en acide ascorbique beaucoup plus important que suggéré par les AJR (de l'ordre de 10 à 20 grammes par jour). Un effet favorable semble exister chez les cultures cellulaires ou chez des animaux, en particulier une inhibition de la prolifération cellulaire[48] mais aucune preuve satisfaisante n'existe chez l'être humain à titre curatif[49],[50] ou préventif[51],[52]. La Société suisse de lutte contre le cancer souligne, en particulier, les faiblesses du dossier scientifique de Matthias Rath, autre promoteur de l'usage de la vitamine C contre le cancer[53]. Matthias Rath a de plus été condamné pour essais thérapeutiques non autorisés[54] et accusé d'avoir fait mourir des patients atteints du VIH en utilisant des vitamines comme traitement anti-VIH à la place d'antirétroviraux[55].
Selon une étude parue en 2008 de l'Institut américain de la santé, l'acide ascorbique injecté par voie intraveineuse à fortes doses réduirait de moitié la croissance des tumeurs de souris de laboratoire[56].
À l'inverse une étude menée par le docteur Mark Heaney de l'Université Columbia conclut qu'un apport complémentaire en vitamine C pourrait diminuer de 30 à 70 % l'efficacité des traitements de chimiothérapie. Pour Fatima Mechta-Grigoriou, directeur de recherche à l'Inserm et chef de l'équipe stress et cancer à l'Institut Curie, il s'agit, d'une analyse « très préliminaire » qui ne permet en rien de dire quel impact a la vitamine C sur les effets thérapeutiques des anticancéreux[57].
En 2010, une méta-analyse[58] passant en revue 33 ans de recherches sur la relation entre vitamine C et cancer conclut : « nous devons conclure que nous ne savons toujours pas si la vitamine C a une quelconque activité antitumorale cliniquement significative. Nous ne savons non plus quels types de cancers, s'il y en a, sont susceptibles de réagir à la vitamine C. Enfin, nous ne savons pas quelle est la dose recommandable, si une telle dose existe, afin de produire une réponse antitumorale. »
Cette analyse fut critiquée par le Dr Andrew W. Saul[59]. Les points principaux de sa réplique sont :
- il est faux de dire que nous ne savons pas combien de vitamine C combat efficacement le cancer et les médecins ont un devoir envers leurs patients de recommander la vitamine C comme traitement de complément ;
- les résultats positifs obtenus par Pauling et Cameron, soulignés par Cabanillas, n'ont pas été contredits par ceux de Moertel et de la Clinique Mayo :
- les traitements ont été interrompus au premier signe d'une aggravation, ce qui n'est jamais fait lors des chimiothérapies,
- l'administration a été faite par voie orale et non intraveineuse, ce qui diminue la dose effectivement absorbée[62],( Pour autant, l'étude initiale de de Pauling et Cameron incluait aussi des doses par voie orale [63], et leur étude n'était pas randomisée, à l'inverse de celle faite par la Clinique Mayo. Le protocole, mis en place par la Clinique Mayo, l'a été fait en accord avec Pauling. Celui-ci a d'ailleurs plutôt réfuté les résultats en arguant que la chimio et la radiothérapie pouvait "endommager" le système immunitaire , mais n'a jamais attaqué le protocole sur les doses orales[64])
- les résultats de Pauling et Cameron ont en fait été confirmés par Murata et Lasagna :
- l'oncologue Victor Marcial rapporte que :
- 75 % des tumeurs ont diminué de 50 % ou plus avec la vitamine C en intraveineuse chez 40 patients au stade 4 (avec métastases) n'ayant pas répondu aux traitements conventionnels (radiothérapie, chimiothérapie),
- la vitamine C augmente les effets de la radiothérapie et en diminue les effets indésirables[66].
Ces quelques résultats favorables ne doivent pas occulter tous les autres, défavorables, non cités par Andrew W. Saul, mis en valeur dans la méta-analyse[58].
Maladie de Charcot-Marie-Tooth
Des quantités entre 1 000 mg et 3 000 mg/jour (fractionnées en plusieurs prises du fait d'un risque de toxicité rénale) sont proposées à titre d'essai thérapeutique dans le traitement d'une maladie neurologique héréditaire, la maladie de Charcot-Marie-Tooth type 1A[67]. L'essai clinique mené chez ces patients n'a pu être envisagé qu'après la réalisation d'un essai pré-clinique, mené sur un modèle murin de la maladie montrant des résultats encourageants[68],[69].
Utilisation en médecine orthomoléculaire
La médecine orthomoléculaire prônée notamment par Linus Pauling, prix Nobel de chimie, recommande une consommation de vitamine C de 2 à 20 g/jour[11] qui peut être augmentée en cas de maladie, en se basant sur les premiers travaux d'Irwin Stone. Linus Pauling a étudié le rôle de la vitamine C dans la prévention du rhume et le traitement du cancer. Cette vitamine, administrée « sous une forme adéquate, au moyen de techniques appropriées, en doses suffisamment fréquentes, en doses suffisamment élevées, en conjonction avec certains agents et pour une période suffisante »[70], serait capable de prévenir voire de guérir un grand nombre de maladies, notamment la grippe[71], le cancer[63],[72] ou les maladies coronariennes[73]. Ces hypothèses n'ont pas été confirmées par d'autres études de plus grande ampleur et plus récentes, que ce soit pour la grippe[74],[75], pour le cancer[76],[77] ou pour les maladies cardio-vasculaires[78].
Autres
Elle pourrait être protectrice au niveau rénal, avec une fréquence moindre d'insuffisance rénale en cas d'injection d'un produit de contraste iodé au cours d'un examen radiologique[79].
En association avec d'autres antioxydants, elle pourrait contribuer à la prévention de la dégénérescence maculaire liée à l'âge[80], voire, des maladies coronariennes[81].
La vitamine C pourrait avoir un rôle important dans la régulation de la synthèse du cholestérol[82].
La prise de vitamine C pourrait diminuer le risque de survenue de goutte[83].
La vitamine C, injectée précocement par voie intraveineuse, fait partie du traitement de l’intoxication phalloïdienne proposé par le docteur Pierre Bastien[84].
Les maladies liées à l’âge et les dysfonctionnements immunitaires qui y sont associés pourraient être limités par l’absorption de suppléments de vitamine C[85].
Chez des hommes infertiles, on a montré qu’un supplément de vitamine C améliorait la qualité du sperme (morphologie et mobilité des spermatozoïdes) et augmentait le nombre de spermatozoïdes[86].
Le médecin australien Archie Kalokerinos (en), adhérant des thèses de Linus Pauling sur la médecine orthomoléculaire et la vitamine C, émet en 1981 l'hypothèse que la forte mortalité infantile observée chez les enfants aborigènes, et notamment la mort subite du nourrisson, seraient dues à un manque de vitamine C et donc au scorbut. Et que cette mortalité serait de plus aggravée par les vaccinations[87]. Cette hypothèse n'a depuis jamais été validée par la communauté scientifique.
Le docteur américain Claus Washington Jungeblut (en) avait émis en 1935 l'hypothèse que la vitamine C puisse inactiver le virus de la poliomyélite. Il publia une série de papiers entre 1936 et 1939 dans lesquels il montrait que l'administration d'acide ascorbique chez des singes infectés diminuait la sévérité de la maladie. Albert Sabin essaya de reproduire ces résultats mais n'y parvint pas, ce qui mit un terme à cette voie de recherche[88]. Le docteur Fred R. Klenner déclara devant l'Association de nutrition appliquée des États-Unis que Sabin avait refusé de suivre les conseils de Jungleblut sur la dose de vitamine C nécessaire et avait imposé à ses singes rhésus une charge virale bien plus importante que dans les expériences initiales. Klenner, quant à lui, annonça des résultats cliniques obtenus notamment lors de l'épidémie de 1948 confirmant les résultats de Jungleblut[89].
Selon des études réalisées en 1967 et 1993 une supplémentation en vitamine C diminuerait la sévérité des symptômes chez les enfants atteints d’autisme, mais la posologie optimale reste à déterminer[90].
L’apparition du syndrome de défaillance multiviscérale, qui pour les traumatologues est un des principaux signes annonciateurs du décès[91], apparaît moins souvent chez les patients recevant de la vitamine C ; cette vitamine diminue aussi les durées de séjour aux soins intensifs[92].
La vitamine C aurait un effet protecteur vis-à-vis de la nicotine sur les poumons en formations d'un foetus. Une supplémentation chez la femme enceinte fumeuse améliore ainsi la fonction respiratoire du nouveau-né et diminue le risque de respiration sifflante[93].
Tolérance intestinale
La tolérance intestinale désigne la quantité de vitamine C qui peut être absorbée par l'intestin dans un temps donné[94]. Lorsque cette quantité est atteinte, la vitamine C non absorbée est éliminée dans les selles. Durant son trajet, elle attire de l'eau dans l'intestin ce qui produit une diarrhée passagère. Ceci est une des raisons pour lesquelles on ne peut pas s'intoxiquer avec de la vitamine C. Certains scientifiques proposent l'hypothèse que la vitamine C étant une vitamine hydrosoluble, une ingestion insuffisante d'eau de dilution au moment de la prise de vitamine C pourrait être à l'origine des troubles intestinaux.
Les quantités produites par les animaux varient en fonction de leur état de stress et santé. Un animal stressé ou malade peut produire plusieurs dizaines de grammes par jour. On peut mettre en parallèle cette production variable d'ascorbate chez les animaux avec la variabilité de la tolérance intestinale chez l'être humain. Lorsqu'un humain est malade ou stressé, sa tolérance intestinale à la vitamine C augmente, ce qui lui permet d'absorber plus de vitamine C qu'en temps normal. La variabilité de la tolérance intestinale suggère un besoin accru de l'organisme en vitamine C dans les périodes de stress ou de maladies, comme on l'observe chez les animaux qui synthétisent la vitamine C.
Histoire
- Au Ve siècle av. J.-C., Aristote connaissait déjà les symptômes du scorbut[95].
- En 1227, Gilbertus de Aguila recommande aux marins d'embarquer des stocks de fruits et de légumes frais pour prévenir le scorbut[96].
- Ce n'est qu'au XVIIIe siècle qu'on découvre que la consommation de citrons prévient cette maladie. Le médecin écossais James Lind mena ce qui est considéré comme le premier essai scientifique : après avoir formé six groupes constitués chacun de deux marins scorbutiques, il administra une substance différente selon le groupe, leur nutrition étant par ailleurs identique. Ces substances étaient : le cidre, de l'acide sulfurique, du vinaigre, une concoction d'herbes et d'épices, de l'eau de mer et des oranges et citrons. Seul le dernier groupe a rapidement guéri du scorbut[97]. L'utilisation de conserves alimentaires mises au point par Nicolas Appert en 1795, conservant la vitamine C, régla définitivement le problème pour la marine.
- En 1919, Jack Cecil Drummond compris que le facteur antiscorbutique faisait partie de ces nouveaux nutriments indispensables qui n'étaient ni sucrés, ni gras, ni protéiques, comme les substances "fat-soluble A", "water-soluble B" déjà connues (découvertes chez le rat), il le nomma d'abord le "water-soluble C"[98], puis recommanda de la nommer vitamine C, dénomination moins "encombrante"[99].
- En 1928, Albert Szent-Gyorgyi voulut comprendre les différences d'oxydation biologique entre des animaux auxquels on avait enlevé les glandes surrénales et d'autres avec leur glandes surrénales. Il s'aperçut que le cortex surrénalien était fortement concentré en une substance très réductrice (antioxydante). Il observa également par ailleurs que des ajouts de jus de plantes pressées à des réactions de peroxydation d'eau oxygénée par des peroxydases inhibait la réaction d'oxydation, il en avait conclut que les plantes contenaient également un élément fortement antioxydant qui détournait l'eau oxygénée. Il isola alors le même agent réducteur dans le cortex surrénalien, dans les oranges et dans les choux. Il le nomma "acide hexuronique" du fait de ses 6 carbones et 6 oxygènes ; il fit alors immédiatement le parallèle avec la fameuse vitamine C, qui était connue pour être antioxydante aussi[100]. Mais ce n'est qu'en 1931 qu'il l'identifia comme étant la vitamine C[101], en même temps que W. A. Waugh et Charles Glen King[102]. Szent-Gyorgyi décida de d'abandonner le nom d'acide hexuronique pour le nom d'acide ascorbique (contraction de anti-scorbutique)[103] ; il obtint le prix Nobel de physiologie ou médecine en 1937.
- Cette molécule a été synthétisée en 1933 par Tadeusz Reichstein puis en 1934, par Walter Norman Haworth qui reçut le prix Nobel de chimie en 1937 pour cette découverte.
Production
La production mondiale annuelle d'acide L-ascorbique est de 80 000 tonnes[104], dont la moitié est utilisée dans les industries pharmaceutiques et parapharmaceutiques, 25 % dans l'agroalimentaire comme conservateur (E300, E301, E302), 15 % dans la fabrication de boissons, le reste étant utilisé pour la nutrition des animaux.
Chez les végétaux, la synthèse de la vitamine C a lieu indifféremment dans toutes les cellules de la plante (voir ci-dessous la liste des aliments possédant les plus hautes concentrations de vitamine C). Dans plusieurs régions du monde, notamment en Europe où sa consommation est importante, la pomme de terre, malgré une teneur moyenne très modérée, est la source principale de vitamine C dans le régime alimentaire moyen. Elle représentait ainsi en 1992 de 15 à 20 % de l'apport journalier moyen au Royaume-Uni[105].
Chez les animaux qui en sont capables, la synthèse a lieu majoritairement dans le foie, mais toutes les autres cellules en ont la capacité, qui reste cependant très limitée.
Teneurs en vitamine C
Les teneurs ci-dessous sont des valeurs moyennes qui peuvent varier notablement selon les variétés des fruits et légumes indiqués.
| Aliment | Teneur (mg/100 g) |
|---|---|
| Terminalia ferdinandiana | 3 000[106],[107] |
| Camu-camu (baie d'Amazonie) | 2 400-3 000[108] |
| Acérola (petite cerise du Brésil( | 1 000-1 677,6[109],[110],[111] |
| Baie d'églantier ou Cynorrhodon | 426-1 250[112],[113] |
| Argousier | 400[114] |
| Amla (ou "groseille indienne") | 445[115] |
| Ortie (Urtica dioica) (ou "grande ortie") | 333[116] |
| Goyave | 228[117] |
| Cassis | 200[118],[119] |
| Persil | 190[118],[119] |
| Poivron rouge cru (cuit) | 162 (81)[118] |
| Lycium barbarum (Baie de Goji) séchée | 73-200[120],[121] |
| Herbes aromatiques fraîches | 143[119] |
| Navet (fanes) | 139[122] |
| Poivrons vert et jaune crus (cuits) | 120 (69)[118] |
| Litchi | 71[118],[119] |
| Fraise | 67[118],[119] |
| Citron | 65[118],[119] |
| Kiwi | 59[123] |
| Chou de Bruxelles cuit | 58,2[118] |
| Cresson cru et cerfeuil | 56,5[118],[119] |
| Chou rouge cru (cuit) | 55 (32)[118] |
| Oseille cru | 48[118] |
| Cerfeuil | 44 7[118] |
| Orange | 39,7[118] |
| Épinard cru (cuit) | 39,3 (5,05)[118] |
| Chou vert cuit | 20[118] |
| Pomme de terre cuite au four (à l'eau) | 12,8 (7,96)[118] |
| Cerise | 9,33[118] |
| Fenouil cru (cuit) | 5-12 (1,6)[124] |
Divers
La vitamine C fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en avril 2013)[125].
Notes et références
- 1 2 3 4 5 6 7 8 9 10 11 « Hazardous Substances Data Bank », sur http://toxnet.nlm.nih.gov (consulté le 17 septembre 2009)
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ Natalie Courret, « Les aliments qui renforcent notre système immunitaire », (consulté le 27 mai 2015)
- ↑ (en) Judy Huang, David B. Agus, Christopher J. Winfree, Szilard Kiss, William J. Mack, Ryan A. McTaggart, Tanvir F. Choudhri, Louis J Kim, J Mocco, David J. Pinsky, William D. Fox, Robert J. Israel, Thomas A. Boyd, David W. Golde, et E. Sander Connolly, Jr. « Dehydroascorbic acid, a blood–brain barrier transportable form of vitamin C, mediates potent cerebroprotection in experimental stroke » Proc Natl Acad Sci U S A. 2001;98(20):11720–11724.
- ↑ (en) AC. Carr, SM. Bozonet, JM. Pullar, JW. Simcock et MC. Vissers, « Human skeletal muscle ascorbate is highly responsive to changes in vitamin C intake and plasma concentrations », Am J Clin Nutr., vol. 97, no 4, , p. 800-7. (PMID 23446899, DOI 10.3945/ajcn.112.053207)
- ↑ (de) Spanyár, P. & P. Kevei, « Über die Stabilisierung von Vitamin C in Lebensmitteln », Zeitschrift für Lebensmittel-Untersuchung und Forschung, vol. 120, no 1, , p. 1-17. (ISSN 1438-2385, DOI 10.1007/BF02425696)
- ↑ (en) Hallberg L, Rossander L, Persson H, Svahn E, « Deleterious effects of prolonged warming of meals on ascorbic acid content and iron absorption », Am J Clin Nutr, vol. 36, no 5, , p. 846-50. (PMID 7137071, lire en ligne [PDF])
- ↑ (en) Johnson RJ, Andrews P, Benner SA, Oliver W, « Theodore E. Woodward award. The evolution of obesity: insights from the mid-Miocene », Trans. Am. Clin. Climatol. Assoc., vol. 121, , p. 295–305; discussion 305–8 (PMID 20697570, PMCID 2917125, lire en ligne)
- ↑ AFSSA, « Apports nutritionnels conseillés en vitamine C pour la population française » [PDF] (consulté le 27 mai 2015)
- ↑ Conseil Supérieur d'Hygiène de Belgique, « Recommandations nutritionnelles pour la Belgique_fr.pdf » [PDF], (consulté le 27 mai 2015), p. 60
- 1 2 (en) Pauling, Linus. My Love Affair with Vitamin C
- ↑ (en) Milton K. (2003) « Micronutrient intakes of wild primates: are humans different? » Comp Biochem Physiol A Mol Integr Physiol. 2003 Sep;136(1):47-59.
- ↑ (en) Portman, O. W., 1970, « Nutritional requirements of non-human primates », dans Feeding and nutrition of non-human primates (éd. R. S. Harris), p. 87-115, New York, Academic Press.
- ↑ Marie-Sophie Germain, « Vitamine C pour cochon d'Inde - Alimentation du cochon d'Inde » (consulté le 27 mai 2015)
- ↑ Dr Didier Boussarie, « Vitamine C dosage cobaye » (consulté le 27 mai 2015)
- ↑ Pharamacorama - L'acide ascorbique ou vitamine C (paragraphe carence)
- ↑ (en) Curhan GC, Willett WC, Speizer FE, Stampfer MJ. « Intake of vitamins B6 and C and the risk of kidney stones in women » J Am Soc Nephrol. 1999 Apr;10(4):840-5.
- ↑ (en) Gerster H. « No contribution of ascorbic acid to renal calcium oxalate stones » Ann Nutr Metab. 1997;41(5):269-82.
- ↑ (en) Curhan GC, Willett WC, Rimm EB, Stampfer MJ. « A prospective study of the intake of vitamins C and B6, and the risk of kidney stones in men » J Urol. 1996 Jun;155(6):1847-51.
- ↑ (en) Hoffer A. « Ascorbic acid and kidney stones » Can Med Assoc J. 1985 Feb 15;132(4):320.
- ↑ (en) Vojdani A, Bazargan M, Vojdani E, Wright J. « New evidence for antioxidant properties of vitamin C » Cancer Detect Prev. 2000;24(6):508-23.
- ↑ (en) « The effects of iron and vitamin C co-supplementation on oxidative damage to DNA in healthy volunteers », Biochemical and Biophysical Research Communications, 8 mai 1998, 246(1):293-8.
- ↑ (en) Suh J, Zhu BZ, Frei B, « Ascorbate does not act as a pro-oxidant towards lipids and proteins in human plasma exposed to redox-active transition metal ions and hydrogen peroxide », Free Radic. Biol. Med., vol. 34, no 10, , p. 1306–14 (PMID 12726918)
- ↑ http://www.inchem.org/documents/jecfa/jecmono/v05je20.htm
- ↑ Dossier Vitamine C sur doctissimo.fr, consulté le 21 mai 2008
- ↑ Fiche acide ascorbique sur le répertoire BIAM, consulté le 21 mais 2008
- ↑ Dossier Calculs rénaux sur passeportsante.net, consulté le 21 mai 2008
- ↑ Les aliments les plus riches en oxalate, La Nutrition.fr
- ↑ « ascorbique acide », sur www.biam2.org
- ↑ (en) Timbo BB, Ross MP, McCarthy PV, Lin CT, « Dietary supplements in a national survey : prevalence of use and reports of adverse events » J Am Diet Assoc. 2006;106(12):1966-1974
- ↑ Voir son jugement.
- ↑ http://www.gazette-sante-social.fr/juridique/jurisprudence-decrypte-la-vente-libre-de-la-vitamine-c-fait-debat-2367.html?recherche=1
- ↑ (en) SY. Suh, WK. Bae, HY. Ahn, SE. Choi, GC. Jung et CH. Yeom, « Intravenous Vitamin C administration reduces fatigue in office workers: a double-blind randomized controlled trial », Nutr. J., vol. 11, no 1, , p. 7 (PMID 22264303, DOI 10.1186/1475-2891-11-7)
- ↑ (en) CJ. Huck, CS. Johnston, BL. Beezhold et PD. Swan, « Vitamin C status and perception of effort during exercise in obese adults adhering to a calorie-reduced diet », Nutrition, vol. 29, no 1, , p. 42-5 (PMID 22677357, DOI 10.1016/j.nut.2012.01.021)
- ↑ (en) Kerxhalli JS, Vogel W, Broverman DM, Klaiber EL., « Effect of ascorbic acid on the human electroencephalogram », J Nutr., vol. 105, no 10, , p. 1356-8. (PMID 1099176, lire en ligne [PDF])
- ↑ (en) Hemilä H, Chalker E, « Vitamin C for preventing and treating the common cold » Cochrane Database Syst Rev. 2013;1:CD000980
- ↑ L'échec des vitamines antioxydantes : une mise au point
- ↑ (en) RM. Douglas, H. Hemila, R. D'Souza, EB. Chalker et B. Treacy, « Vitamin C for preventing and treating the common cold », Cochrane Database Syst Rev, no 4, , CD000980 (PMID 15495002, DOI 10.1002/14651858.CD000980.pub2)
- ↑ (en) « Vitamin C ». Micronutrient Information Center. Linus Pauling Institute.
- ↑ (en) H. Hemilä et E. Chalker, « Vitamin C for preventing and treating the common cold », Cochrane Database Syst. Rev., vol. 1, , CD000980 (PMID 23440782, DOI 10.1002/14651858.CD000980.pub4)
- ↑ (en) Harry N. Holmes, Kathryn Campbell, Edward J. Amberg, « The Effect of Vitamin C on Lead Poisoning », The Journal of Laboratory and Clinical Medicine, vol. 24, no 11, , p. 1119-1127 (lire en ligne)
- ↑ (en) Hasan MY, Alshuaib WB, Singh S, Fahim MA, « Effects of ascorbic acid on lead induced alterations of synaptic transmission and contractile features in murine dorsiflexor muscle », Life Sci., vol. 73, no 8, , p. 1017-25 (PMID 12818354)
- ↑ (en) Simon JA, Hudes ES, « Relationship of ascorbic acid to blood lead levels », JAMA, vol. 281, no 24, , p. 2289-93 (PMID 10386552)
- ↑ (en) Harakeh S, Jariwalla R, Pauling L, « Suppression of human immunodeficiency virus replication by ascorbate in chronically and acutely infected cells », Proc. Natl. Acad. Sci. USA, vol. 87, no 18, , p. 7245-9 (PMID 1698293)
- ↑ (en) Harakeh S, Jariwalla R, « Comparative study of the anti-HIV activities of ascorbate and thiol-containing reducing agents in chronically HIV-infected cells », Am. J. Clin. Nutr., vol. 54, no 6 Suppl, , p. 1231S-1235S (PMID 1720598)
- ↑ (en) Harakeh S, Jariwalla R, « NF-kappa B-independent suppression of HIV expression by ascorbic acid », AIDS Res. Hum. Retroviruses, vol. 13, no 3, , p. 235-9 (PMID 9115810)
- ↑ (en) Harakeh S, Jariwalla R, « Ascorbate effect on cytokine stimulation of HIV production », Nutrition, vol. 11, no 5 Suppl, , p. 684-687 (PMID 8748252)
- ↑ (en) Belin S, Kaya F, Duisit G, Giacometti S, Ciccolini J et al. « Antiproliferative Effect of Ascorbic Acid Is Associated with the Inhibition of Genes Necessary to Cell Cycle Progression » PLoS ONE 2009;4(2): e4409. DOI:10.1371/journal.pone.000440
- ↑ (en) Block KI. Koch Amanda, Mead MN. « Impact of antioxidant supplementation on chemotherapeutic efficacy: A systematic review of the evidence from randomized controlled trials » Cancer Treatment Reviews 2007;33:407-18
- ↑ Anticancéreux naturels : La vitamine C intraveineuse - Dictionnaire sceptique
- ↑ (en) Bjelakovic G, Nikolova D, Gluud LL, Simonetti RG, Gluud C, « Antioxidant supplements for prevention of mortality in healthy participants and patients with various diseases » Cochrane Database of Systematic Reviews 2008;2 DOI:10.1002/14651858.CD007176
- ↑ (en) Gaziano JM, Glynn RJ, Christen WG. et al. « Vitamins E and C in the prevention of prostate and total Cancer in men, The Physicians' Health Study II Randomized Controlled Trial » JAMA 2009;301:52-62
- ↑ (en) Swiss Study Group for Complementary and Alternative Methods in Cancer, « Dr. Matthias Rath's Cellular Health » [PDF], Ligue suisse contre le cancer, 2003 (consulté le 27 mai 2015)
- ↑ (en) Independent Online, « TAC hails ruling on Rath - South Africa », (consulté le 27 mai 2015)
- ↑ (en) Sarah Boseley, « Matthias Rath: Fall of the doctor who said his vitamins would cure Aids », (consulté le 27 mai 2015)
- ↑ (en) Chen Q, Espey MG, Sun AY et al., « Pharmacologic doses of ascorbate act as a prooxidant and decrease growth of aggressive tumor xenografts in mice », Proc. Natl. Acad. Sci. USA, vol. 105, no 32, , p. 11105–9 (PMID 18678913, PMCID 2516281, DOI 10.1073/pnas.0804226105)
- ↑ Le Figaro, « Cancer: la vitamine C réduirait l'efficacité des traitements », (consulté le 27 mai 2015)
- 1 2 (en) Cabanillas F, « Vitamin C and cancer: what can we conclude--1,609 patients and 33 years later? », P. R. Health Sci. J., vol. 29, no 3, , p. 215–7 (PMID 20799507)
- ↑ Andrew W. Saul, « Vitamin C and cancer: what can we conclude--1,609 patients and 33 years later: comment on the article by Cabanillas », P. R. Health Sci. J., vol. 29, no 4, , p. 409-10; author reply 411-2 (PMID 21261183, lire en ligne)
- 1 2 (en) A. Murata, F. Morishige et H. Yamaguchi, « Prolongation of survival times of terminal cancer patients by administration of large doses of ascorbate », Int. J. Vitam. Nutr. Res. Suppl., vol. 23, , p. 103-13 (PMID 6811475)
- ↑ (en) Riordan Clinic Research Institute, « The Riordan IVC Protocol for Adjunctive Cancer Care » [PDF], (consulté le 27 mai 2015)
- ↑ (en) SJ. Padayatty, H. Sun, Y. Wang, HD. Riordan, SM. Hewitt, A. Katz, RA. Wesley et M. Levine, « Vitamin C pharmacokinetics: implications for oral and intravenous use », Ann. Intern. Med., vol. 140, no 7, , p. 533-7 (PMID 15068981, lire en ligne)
- 1 2 (en) Cameron E, Pauling L. « Supplemental ascorbate in the supportive treatment of cancer: prolongation of survival times in terminal human cancer » Proceedings of the National Academy of Sciences 1976, 73:3685-3689. PMID 1068480
- ↑ (en) « Linus Pauling Rebuts New Mayo Study on Vitamin C (September 28, 1979) », sur profiles.nlm.nih.gov (consulté le 23 mars 2015)
- ↑ (en) Louis C. Lasagna Papers. Department of Rare Books, Special Collections and Preservation. River Campus Libraries, University of Rochester
- ↑ [vidéo] Dr Victor Marcial. Vidéo.
- ↑ AFM - Essai vitamine C dans la maladie de Charcot-Marie-Tooth : recrutement réussi des 180 patients, 28 novembre 2007 (consulté le 12 octobre 2008).
- ↑ (en) Passage E, Norreel JC, Noack-Fraissignes P, Sanguedolce V, Pizant J, Thirion X, Robaglia-Schlupp A, Pellissier JF, Fontés M, « Ascorbic acid treatment corrects the phenotype of a mouse model of Charcot-Marie-Tooth disease », Nat. Med., avril 2004, 10(4):396-401
- ↑ (en) « Therapy of Genetic Disorders » (consulté le 29 mars 2013)
- ↑ (en) Levy, Thomas E. Curing the Incurable: Vitamin C, Infectious Diseases, and Toxins. Livon Books, 2002, ISBN 1-4010-6963-0, p. 36.
- ↑ (en) Pauling L (1971) « The significance of the evidence about ascorbic acid and the common cold » Proc Natl Acad Sci U S A 68:2678–2681. PMID 4941984
- ↑ (en) Cameron E, Pauling L. « Supplemental ascorbate in the supportive treatment of cancer: reevaluation of prolongation of survival times in terminal human cancer » Proceedings of the National Academy of Sciences 1978;75:4538-4542. PMID 279931
- ↑ (en) Rath MW, Pauling LC. (en) Brevet U.S. 5,278,189 Prevention and treatment of occlusive cardiovascular disease with ascorbate and substances that inhibit the binding of lipoprotein(a). USPTO, 11 janvier 1994.
- ↑ (en) RM Douglas, H Hemilä, E Chalker, B Treacy. « Vitamin C for preventing and treating the common cold » Cochrane Database Syst Rev. 2007;(3):CD000980. PMID 17636648
- ↑ Vitamin C for Preventing and Treating the Common Cold. Robert M. Douglas, Harri Hemilä (2005) PLoS Med 2(6): e168 doi:10.1371/journal.pmed.0020168.
- ↑ Creagan ET et al., Failure of high-dose vitamin C (ascorbic acid) therapy to benefit patients with advanced cancer. A controlled trial, New England Journal of Medicine, 301:687-690, 1979, résumé
- ↑ Stephen Barrett, M.D., « High Doses of Vitamin C Are Not Effective as a Cancer Treatment »
- ↑ Sesso HD, Buring JE, Christen WG et al., Vitamins E and C in the prevention of cardiovascular disease in men: The Physicians' Health Study II Randomized Controlled Trial, JAMA, 2008, 300:2123-2133
- ↑ Sadat U, Usman A, Gillard JH, Boyle JR, Does ascorbic acid protect against contrast-induced acute kidney injury in patients undergoing coronary angiography: a systematic review with meta-analysis of randomized, controlled trials, J. Am. Coll. Cardiol, 2013;62:2167–2175
- ↑ Evans JR, Lawrenson JG, Antioxidant vitamin and mineral supplements for slowing the progression of age-related macular degeneration, Cochrane Database Syst Rev, 2012;11:CD000254
- ↑ Ye Z, Song H, Antioxidant vitamins intake and the risk of coronary heart disease: meta-analysis of cohort studies, Eur. J. Cardiovasc. Prev. Rehabil., 2008, 15:26–34
- ↑ (en) Harwood H, Greene Y, Stacpoole P, « Inhibition of human leukocyte 3-hydroxy-3-methylglutaryl coenzyme A reductase activity by ascorbic acid. An effect mediated by the free radical monodehydroascorbate », J. Biol. Chem., vol. 261, no 16, , p. 7127-35 (PMID 3711081)
- ↑ Choi HK, Gao X, Curhan G, Vitamin C intake and the risk of gout in men, a prospective study, Arch. Intern. Med., 2009, 169:502-507
- ↑ Médecine générale : Intoxication par les champignons vénéneux
- ↑ (en) de la Fuente M, Ferrández M, Burgos M, Soler A, Prieto A, Miquel J, « Immune function in aged women is improved by ingestion of vitamins C and E », Can. J. Physiol. Pharmacol., vol. 76, no 4, , p. 373-80 (PMID 9795745)
- ↑ (en) Akmal M, Qadri J, Al-Waili N, Thangal S, Haq A, Saloom K, « Improvement in human semen quality after oral supplementation of vitamin C », J. Med. Food, vol. 9, no 3, , p. 440-2 (PMID 17004914)
- ↑ Joseph G. Hattersley, « The Answer to Crib Death Sudden Infant Death Syndrome (SIDS) », sur seanet.com, Journal of Orthomolecular Medicine, (consulté le 15 mai 2008), p. 229-245
- ↑ Andrew W. Saul, « Taking the cure: Claus Washington Jungeblut, M.D.: Polio pioneer; ascorbate advocate », sur doctoryourself.com, Journal of Orthomolecular Medicine, (consulté le 15 mai 2008)
- ↑ Klenner, Fred R. The Use of Vitamin C as an Antibiotic, Journal of Applied Nutrition, 1953, Vol. 6, pp. 274–278
- ↑ (en) Peter Baxter, Vitamin Responsive Conditions in Paediatric Neurology, Londres, MacKeith Press, (ISBN 978-1-898683-28-5, LCCN 2002391668), p. 24
- ↑ (en) Rocker G, Cook D, Sjokvist P et al., « Clinician predictions of intensive care unit mortality », Crit. Care Med., vol. 32, no 5, , p. 1149-54 (PMID 15190965)
- ↑ (en) Nathens A, Neff M, Jurkovich G, Klotz P, Farver K, Ruzinski J, Radella F, Garcia I, Maier R, « Randomized, prospective trial of antioxidant supplementation in critically ill surgical patients », Ann. Surg., vol. 236, no 6, , p. 814-22 (PMID 12454520, lire en ligne)
- ↑ McEvoy CT, Schilling D, Clay N et al., Vitamin C supplementation for pregnant smoking women and pulmonary function in their newborn infants: a randomized clinical trial, JAMA, 2014, 311 DOI:10.1001/jama.2014.5217
- ↑ (en) Robert F. Cathcart III, « "Vitamin C, Titrating To Bowel Tolerance, Anascorbemia, And Acute Induced Scurvy" », (consulté le 27 mai 2015)
- ↑ Vitamine C sur Passeport Santé
- ↑ (en) Lester Packer, Vitamin C in Health and Disease, CRC Press, (ISBN 9780824793135, lire en ligne), p. 2
- ↑ Simon Singh et Edzard Ernst « La naissance de la médecine scientifique (1) », SPS no 295, avril 2011 (consulté le 18 février 2013).
- ↑ Jack Cecil Drummond, « Note on the Rôle of the Antiscorbutic Factor in Nutrition », Biochemical Journal, vol. 13, , p. 77-80 (ISSN 0264-6021, PMID 16742843, PMCID 1258850, lire en ligne)
- ↑ (en) Louis Rosenfeld, « Vitamine—vitamin. The early years of discovery », Clinical Chemistry, vol. 43, , p. 680-685 (ISSN 0009-9147 et 1530-8561, PMID 9105273, lire en ligne)
- ↑ « NCBI - WWW Error Blocked Diagnostic », sur www.ncbi.nlm.nih.gov (consulté le 8 juillet 2015)
- ↑ Joseph Louis Svirbely et Albert Szent-Györgyi, « The chemical nature of vitamin C », Biochemical Journal, vol. 26, 1932, p. 865-870 (ISSN 0264-6021, PMID 16744896, PMCID 1260981, lire en ligne)
- ↑
- ↑ Joseph Louis Svirbely et Albert Szent-Györgyi, « The chemical nature of vitamin C », Biochemical Journal, vol. 27, 1933, p. 279-285 (ISSN 0264-6021, PMID 16745082, PMCID 1252872, lire en ligne)
- ↑ L’ACIDE ASCORBIQUE ET SON UTILISATION EN TANT QU’ADDITIF DANS LES INDUSTRIES ALIMENTAIRES - page 7
- ↑ (en) « Positioning the Potato as a Primary Food Source of Vitamin C », sur SpringerLink, American Journal of Potato Research (DOI 10.1007/s12230-008-9030-6, consulté le 1er décembre 2010).
- ↑ (en) Wild Harvest NT, « http://www.kakaduplum.com.au/index.php/kakadu-plum » (consulté le 27 mai 2015)
- ↑ News Medical, « Sources de vitamine c », (consulté le 27 mai 2015)
- ↑ Justi, Karin Cristiane, Visentainer, Jesuí Vergílio et de Souza, N Evelázio, « Nutritional composition and vitamin C stability in stored camu-camu (Myrciaria dubia) pulp », Archivos latinoamericanos de nutrición, vol. 50, no 4, , p. 374--379 (PMID 11464674, lire en ligne [PDF])
- ↑ (en) Département de l'Agriculture des États-Unis, « Show Foods » (consulté le 28 mai 2015)
- ↑ (en) Percival, Susan S et Findley, Brooke, « FSHN 07-08/FS144: What's in Your Tropical Fruit? », Food Science and Human Nutrition, 2013 (consulté le 28 mai 2015)
- ↑ (en) Wolters Kluwer, « Acerola Uses, Benefits & Side Effects - Drugs.com Herbal Database », 2009 (consulté le 28 mai 2015)
- ↑ (en) Département de l'Agriculture des États-Unis, « Show Foods » (consulté le 28 mai 2015)
- ↑ (en) Wolters Kluwer, « Rose Hips Uses, Benefits & Side Effects - Drugs.com Herbal Database », (consulté le 28 mai 2015)
- ↑ (en) Gutzeit D, Baleanu G, Winterhalter P et Jerz G., « Vitamin C content in sea buckthorn berries (Hippophaë rhamnoides L. ssp. rhamnoides) and related products: a kinetic study on storage stability and the determination of processing effects », Journal of food science, Wiley Online Library, vol. 73, no 9, , C615--C620 (PMID 19021790, lire en ligne)
- ↑ K. Tarwadi et V. Agte, « Antioxidant and micronutrient potential of common fruits available in the Indian subcontinent. », International Journal of Food Sciences and Nutrition, vol. 58, no 5, , p. 341-9 (PMID 17558726, DOI 10.1080/09637480701243905)
- ↑ Xavier Gerbeaud, « Ortie - urtica dioica - urticacées », (consulté le 28 mai 2015)
- ↑ (en) Département de l'Agriculture des États-Unis, « Show Foods » (consulté le 28 mai 2015)
- 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 (fr) La vitamine C sur Aprifel (d’après le Répertoire général des aliments, REGAL (1995) ; "Composition des aliments", Souci, Fachmann et Kraut ; The composition of foods, Mac Cance et Widdowson et différentes études scientifiques).
- 1 2 3 4 5 6 7 Emma, « Les aliments riches en vitamine C », (consulté le 28 mai 2015)
- ↑ (en) Ming, Ma, Guanhua, Liu, Zhanhai, Yu, Guang, Chen et Xuan, Zhang, « Effect of the Lycium barbarum polysaccharides administration on blood lipid metabolism and oxidative stress of mice fed high-fat diet in vivo », Food Chemistry, Elsevier, (consulté le 28 mai 2015), p. 872--877
- ↑ oumshaina, « La baie de Goji : supercherie commerciale » (consulté le 28 mai 2015)
- ↑ (en) John Vaughan et Catherine Geissler, The New Oxford Book of Food Plants, Oxford university press, , 249 p. (ISBN 978-0-19-954946-7, lire en ligne), p. 194
- ↑ Anses, « Anses Table Ciqual 2012 Composition nutritionnelle des aliments » (consulté le 28 mai 2015)
- ↑ (en) Département de l'Agriculture des États-Unis, « Show Foods » (consulté le 28 mai 2015)
- ↑ WHO Model List of Essential Medicines, 18th list, avril 2013
Voir aussi
Reportages télévisés
- Canadian Broadcasting Corporation, Fighting Cancer, John Hoffer, du Jewish General Hospital de Montréal.
- 60 Minutes, Farmer given up for dead by hospital after getting swine flu saved by intravenous vitamin C.
- Suivi : Entrevue avec l'avocate de la famille, au sujet des difficultés de la famille avec l'hôpital.
- HealthWatch, Denise Nakano, NBC 10, « High dose vitamin C reduces tumor growth by half according to a recent study (...) », Reportage.
- HealthWatch, Laura Wilson, NBC, Reportage.
Bibliographie
- (en) Irwin Stone, The Healing Factor: « Vitamin C » Against Disease, Éd. Putnam Pub Group, 1974 (ISBN 0-448-11693-6)
- (en) Linus Pauling avec E. Cameron, Cancer and Vitamin C: A Discussion of the Nature, Causes, Prevention, and Treatment of Cancer With Special Reference to the Value of Vitamin C, Camino Books (ISBN 0-940159-21-X)
- Portail de la biochimie
- Portail de la médecine
- Portail de la chimie
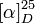 +20,5 à +21,5° (
+20,5 à +21,5° (