
La vitesse de r??action
Renseignements g??n??raux
Cette s??lection ??coles a ??t?? choisi par SOS Enfants pour les ??coles dans le monde en d??veloppement ne ont pas acc??s ?? Internet. Il est disponible en t??l??chargement intranet. SOS Children travaille dans 45 pays africains; pouvez-vous aider un enfant en Afrique ?


La vitesse de r??action ou la vitesse de r??action pendant une r??actif ou produit dans un particulier r??action est intuitivement d??fini comme la vitesse ?? laquelle une r??action se produit. Par exemple, le oxydation du fer dans l'atmosph??re est une r??action lente qui peut prendre de nombreuses ann??es, mais la combustion de butane dans un incendie est une r??action qui se d??roule en quelques fractions de seconde.
Cin??tique chimique est la part de chimie physique qui ??tudie les taux de r??action. Les concepts de la cin??tique chimique sont appliqu??s dans de nombreuses disciplines, telles que g??nie chimique, enzymologie et ing??nierie de l'environnement .
D??finition formelle de la vitesse de r??action
Consid??rons un typique r??action chimique :
- aA + bB → PP + qQ
Les lettres minuscules (a, b, p et q) repr??sentent coefficients stoechiom??triques, tandis que les lettres majuscules repr??sentent la r??actifs (A et B) et le produits (P et Q).
Selon IUPAC de Livre d'or de la d??finition v la vitesse de r??action (??galement R ou R) pour une r??action chimique qui se produit dans un syst??me en vase clos dans des conditions ?? volume constant, sans accumulation de interm??diaires de r??action, est d??fini comme:
Le IUPAC recommande ?? l'unit?? de temps doit toujours ??tre la seconde. Dans un tel cas, la vitesse de r??action diff??rente de la vitesse d'augmentation de la concentration d'un produit P par un facteur constant (l'inverse de son nombre stoechiom??trique) et ?? un r??actif A moins par l'inverse du nombre stoechiom??trique. La vitesse de r??action a g??n??ralement les unit??s de mol dm -3 s -1. Il est important de garder ?? l'esprit que la d??finition pr??c??dente est valable que pour une seule r??action, dans un syst??me ferm?? de volume constant. Cette hypoth??se le plus souvent implicite doit ??tre d??clar?? explicitement, sinon la d??finition est incorrecte: Si l'eau est ajout?? ?? un pot contenant de l'eau sal??e, la concentration de sel diminue, bien qu'il n'y ait pas de r??action chimique.
Pour tout syst??me en g??n??ral la pleine bilan de masse doit ??tre prise en compte: IN - OUT + G??N??RATION = ACCUMULATION
Lorsqu'il est appliqu?? au cas simple indiqu?? pr??c??demment cette ??quation se r??duit ??: ![v = \ frac {d [A]} {dt}](../../images/163/16346.png)
Pour une seule r??action dans un syst??me ferm?? de volume variable le taux dite de conversion peut ??tre est utilis??, afin d'??viter de manipuler des concentrations. Elle est d??finie comme la d??riv??e de la ??tendue de la r??action par rapport au temps.

 est le coefficient stoechiom??trique pour la substance i,
est le coefficient stoechiom??trique pour la substance i, 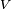 est le volume de r??action et
est le volume de r??action et  est la concentration de substance i.
est la concentration de substance i.
Lorsque des produits secondaires ou des interm??diaires de r??action sont form??s, l'IUPAC recommande l'utilisation des termes vitesse d'apparition et le taux de disparition des produits et des r??actifs, respectivement.
Les vitesses de r??action peuvent ??galement ??tre d??finis sur une base qui ne est pas le volume du r??acteur. Quand un catalyseur est utilis??, la vitesse de r??action peut ??tre indiqu?? sur le poids de catalyseur (g mol -1 s -1) ou de la surface (m mol -2 s -1) base. Si la base est un site de catalyseur sp??cifique qui peut ??tre rigoureusement compt?? par une m??thode d??termin??e, le taux est donn??e en unit??s de s -1 et est appel?? une fr??quence de rotation.
Facteurs influant sur la vitesse de r??action
Les facteurs qui affectent la vitesse de r??action:
- Concentration: hausses de taux de r??action de concentration, tel que d??crit par le loi de vitesse et expliqu??e par la th??orie de la collision. Comme r??actifs concentration augmente, la fr??quence de collision augmente.
- La nature de la r??action: Certaines r??actions sont naturellement plus rapidement que d'autres. Le nombre d'esp??ces r??actives, de leur ??tat physique (les particules solides qui se forment d??place beaucoup plus lentement que ceux des gaz ou celles en solution ), la complexit?? de la r??action et d'autres facteurs peuvent influencer consid??rablement la vitesse d'une r??action.
- Temp??rature : G??n??ralement la r??alisation d'une r??action ?? une temp??rature sup??rieure fournit plus d'??nergie dans le syst??me et augmente la vitesse de r??action en provoquant davantage de collisions entre les particules, comme expliqu?? par la th??orie de la collision. Toutefois, la principale raison pourquoi il augmente la vitesse de r??action, ce est que plusieurs des particules en collision auront la n??cessaire ??nergie d'activation r??sultant de collisions plus de succ??s (o?? les obligations sont form??s entre des r??actifs). L'influence de la temp??rature est d??crit par la ??quation d'Arrhenius. Comme un r??gle g??n??rale, les taux de r??action pour de nombreuses r??actions doubles ou triples pour chaque 10 degr??s Celsius augmentation de la temp??rature, bien que l'effet de la temp??rature peut ??tre tr??s grande ou plus petite que cela (dans la mesure que les taux de r??action peut ??tre ind??pendante de la temp??rature ou diminuent avec augmentation de la temp??rature!)
Par exemple, le charbon br??le dans une chemin??e en pr??sence d'oxyg??ne, mais ce ne est pas quand il est stock?? ?? la temp??rature ambiante. La r??action est spontan??e ?? des temp??ratures basses et ??lev??es, mais ?? la temp??rature ambiante son taux est si lent qu'il est n??gligeable. L'augmentation de la temp??rature, comme r??alis?? par une correspondance, permet ?? la r??action de commencer et ensuite elle se r??chauffe, parce que ce est exothermique. Ce est valable pour d'autres combustibles, tels que le m??thane , butane, de l'hydrog??ne ...
- Solvant : de nombreuses r??actions ont lieu en solution et les propri??t??s du solvant affectent la vitesse de r??action. Le la force ionique a aussi un effet sur la vitesse de r??action.
- Pression: Le taux de r??actions gazeux augmente avec la pression, qui est, en fait, correspond ?? une augmentation de la concentration du gaz. Pour les r??actions en phase condens??e, le dependendence de pression est faible.
- Rayonnement ??lectromagn??tique : Le rayonnement ??lectromagn??tique est une forme d'??nergie de sorte qu'il peut acc??l??rer le rythme ou m??me faire une r??action spontan??e, car il fournit les particules des r??actifs avec plus d'??nergie. Cette ??nergie est d'une mani??re ou d'une autre stock?? dans les particules r??agissant (il peut rompre les liaisons, de promouvoir mol??cules aux Etats ??lectronique ou vibrationnel excit?? ...) la cr??ation d'esp??ces interm??diaires qui r??agissent facilement.
Par exemple, lorsque le m??thane r??agit avec le chlore dans l'obscurit??, la vitesse de r??action est tr??s lente. Il peut ??tre acc??l??r?? lorsque le m??lange est mis sous lumi??re diffuse. En plein soleil, la r??action est explosive.
- Un catalyseur : La pr??sence d'un catalyseur augmente la vitesse de r??action (?? la fois en avant et en arri??re de la r??action) en fournissant une voie alternative avec une faible ??nergie d'activation .
Par exemple, le platine catalyse la combustion de l'hydrog??ne avec l'oxyg??ne ?? temp??rature ambiante.
- Isotopes : Le effet isotopique cin??tique consiste en une vitesse de r??action diff??rents pour la m??me mol??cule si elle a, en g??n??ral des diff??rents isotopes d'hydrog??ne isotopes, en raison de la diff??rence de masse entre l'hydrog??ne et le deuterium.
- Surface: En r??actions sur les surfaces, qui ont lieu par exemple pendant la catalyse h??t??rog??ne, la vitesse de r??action augmente ?? mesure que la zone de surface fait. Cela est d?? au fait que plus de particules du solide sont expos??s et peuvent ??tre frapp??s par des mol??cules de r??actif.
- Ordre: L'ordre des commandes de r??action comment la concentration de r??actif affecte la vitesse de r??action.
- Agitation: agitation peut avoir un effet important sur la vitesse de r??action pour r??actions h??t??rog??nes.
Tous les facteurs qui influent sur la vitesse de r??action sont prises en compte dans l'??quation de la r??action de vitesse.
Taux ??quation
Pour une r??action chimique n A + B → m C + D, l'??quation de vitesse ou loi de vitesse est un expression math??matique utilis??e dans la cin??tique chimique de relier la vitesse d'une r??action de la concentration de chaque r??actif. Il est du genre:
Dans cette ??quation k (t) est le coefficient de vitesse de r??action ou la vitesse constante, m??me se il ne est pas vraiment une constante, car elle comprend tous les param??tres qui affectent la vitesse de r??action, ?? l'exception de la concentration, qui est explicitement prise en compte. Parmi tous les param??tres d??crits pr??c??demment, la temp??rature est normalement la plus importante.
Les exposants n  et m
et m  sont appel??s r??action ordres et d??pendent de la m??canisme de r??action. Ils sont parfois le m??me que le les coefficients stoechiom??triques de A et B, mais pas n??cessairement.
sont appel??s r??action ordres et d??pendent de la m??canisme de r??action. Ils sont parfois le m??me que le les coefficients stoechiom??triques de A et B, mais pas n??cessairement.
Stoechiom??trie, mol??cularit?? (le nombre r??el de mol??cules entrent en collision) et Afin de r??action ne co??ncide n??cessairement dans les r??actions ??l??mentaires, ce est-?? ces r??actions qui ont lieu en une seule ??tape. L'??quation de r??action pour les r??actions ??l??mentaires co??ncide avec le processus qui se d??roule ?? l'??chelle atomique, ce est ?? dire n mol??cules de type A sont collision avec m mol??cules de type B (n plus m est la mol??cularit??).
Pour les gaz la loi de vitesse peut aussi ??tre exprim??e en unit??s de pression en utilisant par exemple la loi des gaz parfaits.
En combinant la loi de vitesse avec un bilan massique pour le syst??me dans lequel la r??action se produit, une expression de la vitesse de variation de concentration peut ??tre d??riv??. Pour un syst??me ferm?? ?? volume constant une telle expression peut ressembler
Influence de la temp??rature
Chaque coefficient de vitesse de r??action k a une d??pendance ?? la temp??rature, qui est g??n??ralement donn??e par la ??quation d'Arrhenius:
E a est l' ??nergie d'activation et R est le constante des gaz. Comme ?? la temp??rature T les mol??cules ont des ??nergies fournies par un Distribution de Boltzmann, on peut se attendre le nombre de collisions avec une ??nergie sup??rieure ?? E un ??tre proportionnelle ??  . A est le facteur pr??-exponentiel ou facteur de fr??quence.
. A est le facteur pr??-exponentiel ou facteur de fr??quence.
Les valeurs de A et E un d??pendent de la r??action. Il existe ??galement des ??quations plus complexes possibles, qui d??crivent la d??pendance de la temp??rature d'autres constantes de vitesse qui ne suivent pas cette tendance.
la d??pendance de la pression
La d??pendance de la pression de la constante de vitesse de r??sum??s r??actions Phase (ie, quand les r??actifs et produits sont des solides ou liquides) est g??n??ralement suffficiently faible dans la gamme de pressions normalement rencontr??es dans l'industrie qu'elle est n??glig??e dans la pratique.
La d??pendance de la pression de la constante de vitesse est associ?? avec le volume d'activation. Pour la r??action de proc??der par le biais d'un complexe de l'??tat-activation:
le volume d'activation, 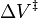 , Est:
, Est:
o??  d??signer les volumes molaires partielles des r??actifs et des produits, et
d??signer les volumes molaires partielles des r??actifs et des produits, et 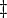 indique le complexe de l'??tat d'activation.
indique le complexe de l'??tat d'activation.
Pour la r??action ci-dessus, on peut se attendre le changement de la constante de vitesse de r??action (bas?? soit sur fraction molaire ou molal-concentration) avec la pression ?? temp??rature constante d'??tre:
En pratique, la question peut ??tre compliqu?? car les volumes molaires partielles et le volume d'activation peuvent ??tre eux-m??mes une fonction de la pression.
Les r??actions peuvent augmenter ou diminuer leurs taux avec la pression, depeding sur la valeur de 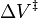 . A titre d'exemple de l'importance possible de l'effet de pression, certaines r??actions organiques ont ??t?? pr??sent??s au double de la vitesse de r??action lorsque la pression a ??t?? augment??e de atomospheric (0,1 MPa) ?? 50 MPa (ce qui donne
. A titre d'exemple de l'importance possible de l'effet de pression, certaines r??actions organiques ont ??t?? pr??sent??s au double de la vitesse de r??action lorsque la pression a ??t?? augment??e de atomospheric (0,1 MPa) ?? 50 MPa (ce qui donne 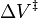 = -0,025 L / mol).
= -0,025 L / mol).
Exemples
Pour la r??action
L'??quation de taux est de:
L'??quation de taux ne refl??te pas simplement les r??actifs coefficients stoechiom??triques dans la r??action globale: il est premier ordre en H 2, bien que le coefficient stoechiom??trique est deux et il est le deuxi??me ordre dans NO.
Dans la cin??tique chimique de la r??action globale est g??n??ralement propos?? de se produire ?? travers un certain nombre d'??tapes ??l??mentaires. Toutes ces ??tapes affecte pas la vitesse de r??action; normalement ce ne est que l'??tape la plus lente ??l??mentaire qui affectent le taux de r??ation. Par exemple, dans:
 (??quilibre rapide)
(??quilibre rapide)  (Ralentir)
(Ralentir)  (Rapide)
(Rapide)
Les r??actions 1 et 3 sont tr??s rapide par rapport ?? la seconde, il est donc plus lente que la r??action se traduit par l'??quation de vitesse. L'??tape lente est consid??r?? comme l'??tape de la d??termination de taux. Les ordres de l'??quation de vitesse sont celles de l'??tape de la d??termination de taux.

![v = - \ frac {1} {a} \ frac {d [A]} {dt} = - \ frac {1} {b} \ frac {d [B]} {dt} = \ frac {1} { p} \ frac {d [P]} {dt} = \ frac {1} {q} \ frac {d [Q]} {dt}](../../images/163/16344.png)
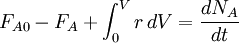
![\, R = k (T) [A] ^ {n '} [B] m ^ {'}](../../images/163/16350.png)
![\ Frac {d [C]} {} dt = k (T) [A] ^ {n '} [B] ^ {m'}](../../images/163/16352.png)

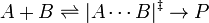

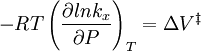

![r = k [H_2] ^ 1 [NO] ^ 2 \,](../../images/163/16362.png)
