Phénylalanine
|
|
Cet article est une ébauche concernant la biochimie. Vous pouvez partager vos connaissances en l’améliorant (comment ?) selon les recommandations des projets correspondants.
Consultez la liste des tâches à accomplir en page de discussion. |
| Phénylalanine | |
|---|---|
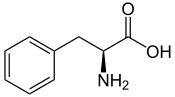 L ou S(–)-phénylalanine  D ou R(+)-phénylalanine | |
| Identification | |
| Nom UICPA | acide 2-amino-3-phénylpropanoïque |
| Synonymes | F, Phe |
| No CAS | (racémique) (L) ou S(–) (D) ou R(+) |
| No EINECS | (L) (D) |
| DrugBank | |
| PubChem | |
| FEMA | |
| SMILES | |
| InChI | |
| Apparence | poudre blanche |
| Propriétés chimiques | |
| Formule brute | C9H11NO2 [Isomères] |
| Masse molaire[1] | 165,1891 ± 0,0088 g/mol C 65,44 %, H 6,71 %, N 8,48 %, O 19,37 %, |
| pKa | 1,83 (fonction acide) 9,13 (fonction amine) |
| Propriétés physiques | |
| T° fusion | 275 à 283 °C |
| Propriétés biochimiques | |
| Codons | UUC, UUU |
| pH isoélectrique | 5,48[2] |
| Acide aminé essentiel | oui |
| Occurrence chez les vertébrés | 4,0 %[3] |
| Précautions | |
Produit non contrôlé | |
La phénylalanine (abréviations IUPAC-IUBMB : Phe et F) est un acide α-aminé dont l'énantiomère L est l'un des 22 acides aminés protéinogènes, et l'un des 9 acides aminés essentiels pour l'homme. Elle est encodée sur les ARN messagers par les codons UUU et UUC. Elle est caractérisé par un groupe phényle, ce qui en fait un résidu apolaire aromatique, dont le cycle benzénique lui confère un spectre d'absorption particulier dans l'U.V, autour de 260 nm de longueur d'onde.
L'action de la phénylalanine hydroxylase la transforme en un autre acide aminé, la tyrosine.
La phénylalanine est un précurseur de l'adrénaline, de la noradrénaline et de la mélanine. L'aspartame en dérive également.
Chimie industrielle
La phénylalanine est, avec l'aspartate, l'un des deux constituants de l'aspartame, un dipeptide utilisé comme édulcorant dans les boissons et les aliments dits « légers » (notamment les sodas light) pour son pouvoir sucrant 200 fois supérieur à celui du saccharose et sa faible valeur énergétique.
Biochimie
La phénylcétonurie est une maladie génétique caractérisée par des troubles neurologiques et comportementaux graves. Elle est due à la progression d'une version non efficiente de l'enzyme dégradant la phénylalanine, la phénylalanine hydroxylase, à la suite d'une mutation d'un gène situé sur le chromosome 12. Cela entraine une concentration sanguine en phénylalanine trop élevée chez l'individu malade. Toxique à forte concentration, celle-ci s'accumule alors dans l'organisme, provoquant des lésions de la myéline et de la substance blanche. Le dépistage néonatal permet l'instauration rapide d'une diète alimentaire stricte permettant d'éliminer la plupart des symptômes.
Phénylpropanoïdes
La phénylalanine joue un rôle majeur dans le monde végétal : il s'agit de la molécule dont dérivent tous les phénylpropanoïdes, qui comprennent entre autres les coumarines, les flavonoïdes, les stilbénoïdes, ainsi que les monolignols, les monomères de la lignine et de la lignane qui constituent les parois des cellules végétales.
La phénylalanine est d'abord transformée en acide cinnamique par l'action de l'enzyme phénylalanine ammonia-lyase (PAL). Ce dernier est ensuite converti par des séries d'hydroxylation, méthylation et réductions enzymatiques en différents précurseurs de chacune des classes de phénylpropanoïdes.
Alimentation
On retrouve de la phénylalanine dans la plupart des aliments communs[5] :
- Céréales et produits céréaliers
- Racines féculentes, tubercules
- Légumineuses et produits dérivés
- Noix et graines
- Légumes
- Fruits
- Viande et volaille
- Œufs
- Poisson, crustacés, mollusques et produits à base de poisson
- Lait et produits laitiers
- chewing-gum
- Levures et algues
Les graines et légumes sont les aliments contenant le plus de phénylalanine, suivis de près par certains fromages (à pâte sèche en particulier).
Médicale
La phénylalanine est présente notamment dans les chewing-gums contenant en grande majorité de l'aspartame (peptide édulcorant). Si cet aminoacide n'a pas d'effets dans les proportions de quelques gommes mâchées par jour, elle aura par contre un effet laxatif à des quantités plus grandes (à partir de 2 voire 3 paquets de gommes à mâcher par jour). En effet à forte dose, la phénylalanine accélère le transit intestinal.
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ (en) Francis A. Carey, « Table of pKa and pI values », sur Département de chimie de l'université de Calgary, (consulté le 26 juillet 2015)
- ↑ (en) M. Beals, L. Gross, S. Harrell, « Amino Acid Frequency », sur The Institute for Environmental Modeling (TIEM) à l'université du Tennessee (consulté le 26 juillet 2015)
- ↑ « Phénylalanine (d-) » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009
- ↑ http://www.fao.org/docrep/005/ac854t/AC854T00.htm
Liens externes
- http://www.chups.jussieu.fr/polys/biochimie/STbioch/POLY.Chp.11.14.html
- (en) http://www.chemie.fu-berlin.de/chemistry/bio/aminoacid/phe_en.html
- Portail de la biochimie
- Portail de la chimie
