Enthalpie de changement d'état
|
|
Cet article est une ébauche concernant la thermodynamique et la chimie. Vous pouvez partager vos connaissances en l’améliorant (comment ?) selon les recommandations des projets correspondants.
|
L'enthalpie de changement d'état d'un corps pur est par définition la variation d'enthalpie 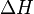 =
= 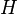 2 -
2 - 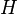 1 qui accompagne le passage du système d'un état physique 1 à un état physique 2. On définit l'enthalpie de changement d'état molaire ou massique.
1 qui accompagne le passage du système d'un état physique 1 à un état physique 2. On définit l'enthalpie de changement d'état molaire ou massique.

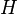 d'un système au cours de ses changements d'état (l'axe est orienté dans le sens des
d'un système au cours de ses changements d'état (l'axe est orienté dans le sens des 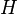 croissantes)
croissantes)L'enthalpie de changement d'état, molaire exprimée en J/mol ou massique exprimée en J/kg, notée 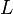 , est la quantité d'énergie nécessaire à l'unité de quantité de matière (mole) ou de masse (kg) d'un corps pur pour qu'il change d'état, cette transformation ayant lieu à pression constante. Par exemple pour le passage de l'état liquide à l'état de vapeur on parlera d'enthalpie de vaporisation.
, est la quantité d'énergie nécessaire à l'unité de quantité de matière (mole) ou de masse (kg) d'un corps pur pour qu'il change d'état, cette transformation ayant lieu à pression constante. Par exemple pour le passage de l'état liquide à l'état de vapeur on parlera d'enthalpie de vaporisation.
L'enthalpie échangée lors du changement d'état résulte de la modification (rupture ou établissement) de liaisons interatomiques ou intermoléculaires. Il existe trois états physiques principaux pour tout corps pur: l'état solide, l'état liquide et l'état gazeux. Les liaisons sont plus fortes dans l'état solide que dans l'état liquide et ces liaisons sont quasi-absentes dans l'état gazeux. Il existe un quatrième état obtenu à très haute température où la matière se trouve sous la forme d'un plasma d'ions et d'électrons.
Par exemple, l'eau bout à 100 °C sous la pression d'1 atmosphère ( 1atm = 101325 Pascal). L'enthalpie de vaporisation de l'eau, égale à la quantité de chaleur fournie pour transformer l'eau liquide en vapeur, est de 2257 kJ/kg.
Le changement d'état s'effectuant à pression 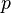 constante, la quantité d'énergie échangée avec le milieu extérieur lors du passage de l'état 1 à l'état 2 est
constante, la quantité d'énergie échangée avec le milieu extérieur lors du passage de l'état 1 à l'état 2 est 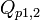 =
= 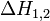 (voir enthalpie).
(voir enthalpie). 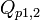 est encore parfois appelée chaleur latente de changement d'état ; l'adjectif « latente » indique que cette quantité est « cachée » avant d'être absorbée ou dégagée lors du changement d'état. À l'expression « chaleur latente de changement d'état » (molaire ou massique), on préfère aujourd'hui celle d'« enthalpie de changement d'état » (molaire ou massique), le terme de chaleur étant réservé au transfert d'énergie (transfert d'énergie thermique ou transfert thermique).
est encore parfois appelée chaleur latente de changement d'état ; l'adjectif « latente » indique que cette quantité est « cachée » avant d'être absorbée ou dégagée lors du changement d'état. À l'expression « chaleur latente de changement d'état » (molaire ou massique), on préfère aujourd'hui celle d'« enthalpie de changement d'état » (molaire ou massique), le terme de chaleur étant réservé au transfert d'énergie (transfert d'énergie thermique ou transfert thermique).
Changement d'état
Au cours d'un changement d'état d'un corps pur, il y a une variation d'enthalpie et d'entropie du corps.
Par exemple pour un corps de masse m passant de l'état 1 à l'état 2 à la température 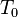
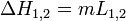 et
et 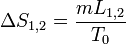
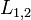 Enthalpie de changement d'état massique exprimée en J/kg
Enthalpie de changement d'état massique exprimée en J/kg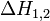 Variation d'enthalpie en J
Variation d'enthalpie en J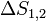 Variation d'entropie en J/K
Variation d'entropie en J/K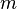 masse en kg
masse en kg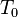 Température en K
Température en K
L'enthalpie de changement d'état massique de fusion des métaux est comprise entre 4 et 16 kJ/kg, sauf rare exception. Cette règle permet de connaître une valeur approchée de l'enthalpie de fusion, connaissant la température de fusion :
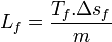
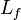 enthalpie de changement d'état massique exprimée en J/kg
enthalpie de changement d'état massique exprimée en J/kg
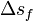 variation d'entropie molaire lors de la fusion en J/(mol.K)
variation d'entropie molaire lors de la fusion en J/(mol.K)
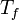 température de fusion en K
température de fusion en K
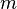 masse en kg
masse en kg
Enthalpie de fusion
L'enthalpie de fusion est l'énergie absorbée par chaleur par un corps lorsqu'il passe de l'état solide à l'état liquide à température et pression constantes.
L'enthalpie de solidification (transformation inverse de la précédente) est l'opposée de l'enthalpie de fusion :
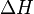 (solidification) = -
(solidification) = - 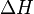 (fusion)
(fusion)
Enthalpie de vaporisation
L'enthalpie de vaporisation d'un composé chimique est la différence d'enthalpie mise en jeu lors de la vaporisation d'une mole de ce composé.
L'enthalpie de liquéfaction (transformation inverse de la précédente) est l'opposée de l'enthalpie de vaporisation :
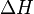 (liquéfaction) = -
(liquéfaction) = - 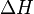 (vaporisation)
(vaporisation)
Enthalpie de sublimation
L'enthalpie de sublimation, anciennement chaleur latente de sublimation, est l'énergie absorbée par chaleur par un corps lorsqu'il passe de l'état solide à l'état gazeux à température et pression constantes.
L'enthalpie de déposition (transformation inverse de la précédente) est l'opposée de l'enthalpie de sublimation :
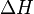 (déposition) = -
(déposition) = - 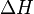 (sublimation)
(sublimation)
Histoire
On nommait autrefois chaleur latente cette grandeur, en référence à la vision substantialiste de la chaleur (considérée comme un fluide, une substance, immatérielle) qui était largement répandue jusqu'au XIXe siècle avec notamment les travaux de Joseph Fourier sur cette dernière.
Données[1]
| Substance | Chaleur latente de fusion kJ/kg |
Point de fusion °C |
Chaleur latente de vaporization kJ/kg |
Point d'ébullitino °C |
|---|---|---|---|---|
| Ethanol | 108 | −114 | 855 | 78.3 |
| Ammoniac | 332.17 | −77.74 | 1369 | −33.34 |
| Dioxyde de carbone | 184 | −78 | 574 | −57 |
| Hélium | 21 | −268.93 | ||
| Dihydrogène(2) | 58 | −259 | 455 | −253 |
| Plomb[2] | 23.0 | 327.5 | 871 | 1750 |
| Diazote | 25.7 | −210 | 200 | −196 |
| Dioxygène | 13.9 | −219 | 213 | −183 |
| Réfrigérant R134a | −101 | 215.9 | −26.6 | |
| Réfrigerant R152a | −116 | 326.5 | -25 | |
| Toluène | 72.1 | −93 | 351 | 110.6 |
| Térébentine | 293 | |||
| Eau | 334 | 0 | 2264.76 | 100 |
Voir aussi
- Chaleur massique
- Règle de Trouton (calcul empirique de l'enthalpie de vaporisation)
- Formule de Clapeyron
- Chaleur
- Calorimétrie
Références
- Jean-Claude Guibet et Emmanuelle Faure-Birchem (collaboratrice) (préf. Raymond Lévy), Carburants et moteurs, Paris, Éditions Technip, coll. « Publications de l'Institut Français du Pétrole », (ISBN 2-7108-0704-1)
- Jean-Marie Donnini et Lucien Quaranta, Dictionnaire de physique expérimentale, t. II, Sarreguemines, Éditions Pierron, coll. « Thermodynamique et Applications », (ISBN 2-7085-0168-2)
Références
- ↑ D'après l'article en anglais
- ↑ Yaws' Handbook of Properties of the Chemical Elements 2011 Knovel
- Portail de la physique
- Portail de la chimie
- Portail de l’énergie
- Portail des sciences des matériaux