Cycle de Krebs
Le cycle de Krebs, également appelé cycle de l'acide citrique, est une voie métabolique produisant des intermédiaires énergétiques conduisant à la production d'ATP à travers la chaîne respiratoire. Il s'agit d'un cycle car le dernier métabolite, l'oxaloacétate, est aussi impliqué dans la première réaction. Le cycle peut se résumer par l'oxydation de deux atomes de carbone en CO2 ; l'énergie dégagée par ces réactions génère du GTP (équivalent à l'ATP en termes d'énergie), des électrons, du NADH et un équivalent de la coenzyme Q10, l'ubiquinol CoQ10H2, qui peuvent être métabolisés par la chaîne respiratoire pour former de l'ATP.
Point de convergence de plusieurs réactions de catabolismes du métabolisme cellulaire, il a été découvert par le biologiste Hans Adolf Krebs en 1937. Le cycle de Krebs peut aussi servir à la production d'intermédiaires utilisés pour certaines réactions d'anabolisme.
Il est le point final et commun du catabolisme des glucides (glycolyse, voie des pentoses phosphates), des lipides (β-oxydation) et des acides aminés, car tous ces catabolismes aboutissent à la formation d'acétyl-coenzyme A. L'acétyl-CoA est une forme de transport des groupes acétyle qui proviennent du pyruvate. La première étape du cycle consiste à transférer ce groupe acétyle sur l'oxaloacétate pour former du citrate. Le reste du cycle consiste en des transformations catalysées. La dernière étape produit de l'oxaloacétate, qui peut ensuite réagir à nouveau dans la première étape avec un groupe acétyle et recommencer le cycle. Il existe toutefois des réactions d'échappement au cycle de Krebs qui permettent d'utiliser certains intermédiaires pour d'autres fonctions cellulaires.
Le cycle de Krebs se déroule dans la matrice mitochondriale des eucaryotes et dans le cytoplasme des bactéries, en conditions aérobies (présence d'oxygène). Les enzymes catalysant cette suite de réactions sont localisées dans la matrice mitochondriale (cytoplasme chez les bactéries) ou au niveau de la membrane mitochondriale interne (membrane interne chez les bactéries).
Avec la chaîne respiratoire, qui oxyde à nouveau les coenzymes NADH et CoQ10H2 produites par le cycle, le cycle de Krebs est le processus ultime de dégradation des différents métabolites en dioxyde de carbone et en eau.

Étapes du cycle de Krebs
| Substrats | Produits | Enzyme | Type de réaction | Remarques | |
|---|---|---|---|---|---|
| 1 | Oxaloacétate + Acétyl-CoA + H2O |
Citrate + CoA-SH |
Citrate synthase | Crotonisation | Irréversible, allonge l'oxaloacétate (4C) en une molécule à six atomes de carbone |
| 2 | Citrate | cis-Aconitate + H2O |
Aconitase | Déshydratation | Isomérisation réversible |
| 3 | cis-Aconitate + H2O |
Isocitrate | Hydratation | ||
| 4 | Isocitrate + NAD+ |
Oxalosuccinate + NADH + H+ |
Isocitrate déshydrogénase | Oxydation | Produit du NADH (équivalent à 2,5 ATP) |
| 5 | Oxalosuccinate | α-Cétoglutarate + CO2 |
Décarboxylation | Réaction limitante, étape irréversible, produisant une molécule à cinq atomes de carbone. | |
| 6 | α-Cétoglutarate + NAD+ + CoA-SH |
Succinyl-CoA + NADH + H+ + CO2 |
Complexe α-cétoglutarate déshydrogénase | Décarboxylation oxydative |
Étape irréversible, produisant du NADH (équivalent à 2,5 ATP), conduisant à une molécule à quatre atomes de carbone (hors coenzyme A) |
| 7 | Succinyl-CoA + GDP + Pi |
Succinate + CoA-SH + GTP |
Succinyl-CoA synthétase | Phosphorylation | ou ADP → ATP à la place de GDP → GTP, produit une molécule d'ATP ou d'un équivalent La réaction de condensation du GDP avec le Pi et l'hydrolyse de la succinyl-CoA implique la molécule d'H2O requise pour l'équilibre de la réaction. |
| 8 | Succinate + CoQ10 |
Fumarate + Ubiquinol (CoQ10H2) |
Succinate déshydrogénase | Oxydation | Utilise le FAD comme groupe prosthétique (FAD → FADH2 à la première étape de la réaction), équivalent à 1,5 ATP |
| 9 | Fumarate + H2O |
L-malate | Fumarase | Hydratation | |
| 10 | L-malate + NAD+ |
Oxaloacétate + NADH + H+ |
Malate déshydrogénase | Oxydation | Réversible (en réalité, l'équilibre favorise la formation du L-malate), produit du NADH (équivalent à 2,5 ATP) |
Synthèse du citrate
La citrate synthase condense l'oxaloacétate et l'acétyl-CoA en citrate avec libération de la coenzyme A. Il se forme un intermédiaire transitoire, la citroyl-CoA. La liaison thioester de l'acétyl-CoA est une liaison à haut potentiel d'hydrolyse. Le couplage des activités hydrolase et synthase rend la réaction de synthèse thermodynamiquement possible. Cette réaction est une étape régulatrice du cycle, avec comme effecteur négatif sur la vitesse de réaction la succinyl-CoA, le NADH, l'acétyl-CoA, le citrate et l'ATP.

Déshydratation du citrate
L'aconitase, une lyase, catalyse la déshydratation du citrate en cis-aconitate. Bien que la molécule de citrate semble être symétrique, on a montré que le départ d'eau a lieu entre les atomes de carbone issus de l'oxaloacétate :

Hydratation du cis-aconitate
L'aconitase catalyse également l'hydratation du cis-aconitate en isocitrate :

Les deux étapes précédentes, catalysées par l'aconitase, aboutissent à l'isomérisation du citrate en isocitrate :
- {| align="left"
|- align="center" valign="middle"
|  |
|  H2O +
|
H2O +
| ![]() |
|  |
|  |- align="center" valign="middle"
| Citrate
|
| cis-aconitate
|
| Isocitrate
|- align="center" valign="middle"
| Citrate
|
| cis-aconitate
|
| Isocitrate
|}
Oxydation de l’isocitrate
L'isocitrate déshydrogénase, une oxydoréductase, catalyse l'oxydation de l'isocitrate en oxalosuccinate :
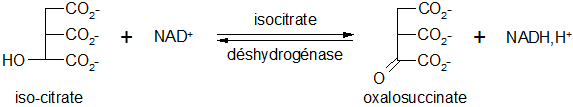
L'isocitrate déshydrogénase NAD+ dépendante exige également comme cofacteur des ions Mn2+ ou Mg2+.
Décarboxylation de l'oxalosuccinate
L'isocitrate déshydrogénase catalyse également la décarboxylation de l'oxalosuccinate, instable, en α-cétoglutarate avec dégagement de CO2, en une réaction irréversible :
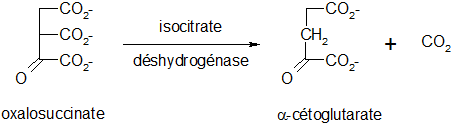
C'est également une étape régulatrice du cycle, avec comme effecteurs négatifs le NADH et l'ATP. La présence d'ADP favorise au contraire l'activité de l'isocitrate déshydrogénase, et ainsi la vitesse de cette réaction.
Décarboxylation oxydative de l'α-cétoglutarate
Le complexe α-cétoglutarate déshydrogénase catalyse la décarboxylation oxydative de l'α-cétoglutarate en succinyl-CoA avec production de NADH+H+ et dégagement de CO2. C'est une réaction semblable à celle convertissant le pyruvate en acétyl-CoA, catalysée par le complexe pyruvate déshydrogénase. Ce complexe enzymatique fait intervenir successivement trois enzymes — l'α-cétoglutarate déshydrogénase, la dihydrolipoamide S-succinyltransférase et la dihydrolipoyl déshydrogénase — et cinq cofacteurs : le TPP, la lipoamide, la coenzyme A, le FAD et le NAD+. Cette réaction est irréversible.

Le NADH, le GTP et la succinyl-CoA sont des effecteurs négatifs sur l'activité du complexe enzymatique.
Formation du succinate
La succinyl-CoA synthétase, ou succinate thiokinase, convertit la succinyl-CoA en succinate et coenzyme A avec formation d'une molécule de GTP chez les animaux ou d'ATP chez les plantes et les bactéries. Cette réaction est réversible.

Oxydation du succinate
La succinate déshydrogénase, une oxydoréductase, catalyse l'oxydation du succinate en fumarate avec réduction concomitante de l'ubiquinone (coenzyme Q10) en ubiquinol (CoQ10H2). Cette enzyme flavoprotéique à FAD est le complexe II de la chaîne respiratoire. Elle est inhibée par le malonate. Le FAD étant un groupe prosthétique lié de manière covalente à l'enzyme, il ne fait que transmettre les électrons et protons au « vrai » substrat CoQ10.

Cette réaction est la quatrième et dernière réaction régulatrice du cycle. Le malonate est ici l'inhibiteur compétitif.
Hydratation du fumarate
La fumarase, une lyase, catalyse l'hydratation du fumarate en L-malate.

Oxydation du malate : fermeture du cycle
La malate déshydrogénase, une oxydoréductase, convertit le L-malate en oxaloacétate avec formation de NADH+H+.
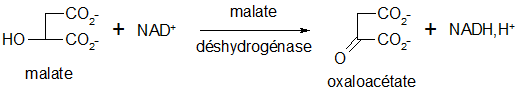
Bilan du cycle de Krebs
Le cycle de Krebs est composé de 10 étapes catalysées par huit enzymes différentes. Au cours du cycle sont produites, à partir d'une mole d'acétate et jusqu'au stade CO2 et H2O :
- 2 moles de CO2
- 3 moles de NADH + H+
- 1 mole de CoQ10H2
- 1 mole de GTP
On constate que le cycle de Krebs ne produit qu'un seul équivalent ATP (une GTP), soit moins que la glycolyse (quatre molécules d'ATP pour une molécule de glucose dont deux sont utilisées lors de la phase « d'activation » de la glycolyse — étapes 1 et 3, qui correspondent à des phosphorylations). L'essentiel de l'énergie chimique potentielle est produite sous forme de pouvoir réducteur (NADH + H+ et CoQ10H2). Ce pouvoir réducteur est ultérieurement utilisé dans la chaîne respiratoire des mitochondries pour produire 11 autres molécules d'ATP via un gradient de protons et une ATP synthase qu'on attribue parfois de façon erronée au cycle de Krebs.
| Description | Substrats | Produits |
| La somme de toutes les réactions d'oxydation de l'acétyl-CoA par le cycle de Krebs (hors chaîne respiratoire) correspond à : | Acétyl-CoA + 3 NAD+ + CoQ10 + GDP + Pi + 2 H2O | → CoA-SH + 3 (NADH + H+) + CoQ10H2 + GTP + 2 CO2 |
| En remontant jusqu'à la décarboxylation du pyruvate, le bilan devient : | Pyruvate + 4 NAD+ + CoQ10 + GDP + Pi + 2 H2O | → 4 (NADH + H+) + Q10H2 + GTP + 3 CO2 |
| En remontant jusqu'à l'oxydation du glucose par la glycolyse, le bilan devient : | Glucose + 10 NAD+ + 2 CoQ10 + 2 ADP + 2 GDP + 4 Pi + 2 H2O | → 10 (NADH + H+) + 2 CoQ10H2 + 2 ATP + 2 GTP + 6 CO2 |
Ce qui correspond, au total, pour l'ensemble de la respiration aérobie (glycolyse, cycle de Krebs, réduction des coenzymes NAD+ et CoQ10 par la chaîne respiratoire) entre 30 et 38 ATP pour une molécule de glucose selon les estimations[1], dépendant en partie de la navette mitochondriale ATP-dépendante utilisée pour transporter le NAD+ de la glycolyse.
L’utilisation du glucose par respiration aérobie est plus énergétique que les fermentations.
En présence d'une grande quantité d'acétyl-CoA, le cycle de Krebs peut être débordé, en particulier chez les diabétiques ayant un déficit sévère en insuline ou après un jeûne prolongé (cf. cétoacidose diabétique pour de plus amples détails).
Régulation du cycle
Les étapes irréversibles du cycle de Krebs peuvent être régulées : étape de la citrate synthase, de l'isocitrate déshydrogénase et de α-cétoglutarate déshydrogénase.
- La citrate synthase est activée par l'ADP mais inhibée par le NADH, l'ATP et le citrate. Elle est donc respectivement inhibée par le pouvoir réducteur, la charge énergétique et le produit de la réaction qu'elle catalyse.
- L'isocitrate déshydrogénase est activée par le calcium, l'ADP et inhibée par le NADH et l'ATP.
- L'α-cétoglutarate déshydrogénase est activée par le calcium et inhibée par le NADH, l'ATP et son produit le succinyl-CoA.
Il y a donc une régulation selon la disponibilité du substrat, le pouvoir réducteur, la concentration en produit et la charge énergétique. On peut noter qu'il n'y a pas de régulation par covalence (phosphorylation des protéines).
Notes et références
- ↑ (en) R. K. Porter et M. D. Brand, « Mitochondrial proton conductance and H+/O ratio are independent of electron transport rate in isolated hepatocytes », Biochemical Journal, vol. 310, , p. 379–382 (lire en ligne)
Voir aussi
Articles connexes
- Chaîne respiratoire : le devenir des NADH,H+
- Respiration cellulaire
- Glycolyse
- Les principales voies du métabolisme (sur wikibooks)
- Hans Adolf Krebs
Liens externes
- (en) Le cycle de Krebs
- (fr) Le cycle de Krebs / Médecine PCEM
- Portail de la biochimie
- Portail de la biologie cellulaire et moléculaire
- Portail de la biologie
- Portail de la microbiologie
