
Fenol
Acerca de este escuelas selección Wikipedia
SOS Children produjo este sitio web para las escuelas, así como este sitio web video sobre África . El patrocinio de los niños ayuda a los niños en el mundo en desarrollo para aprender también.
| Fenol | |
|---|---|
 |  |
 |  |
Fenol | |
Otros nombres Ácido carbólico | |
| Identificadores | |
| CAS | 108-95-2 |
| Número RTECS | SJ3325000 |
| Imágenes-Jmol 3D | Image 1 |
SONRISAS
| |
InChI
| |
| Propiedades | |
| Fórmula molecular | C 6 H 5 OH |
| Masa molar | 94.11 g / mol |
| Apariencia | Sólido cristalino blanco |
| Densidad | 1,07 g / cm³ |
| Punto de fusion | 40.5 ° C |
| Punto de ebullicion | 181.7 ° C |
| Solubilidad en agua | 8,3 g / 100 ml (20 ° C) |
| Acidez (p K a) | 9.95 |
| Momento bipolar | 1.7 D |
| Peligros | |
| Clasificación de la UE | Tóxico (T) Muta. Gato. 3 Corrosivo (C) |
| NFPA 704 |  2 4 0 |
| Punto de inflamabilidad | 79 ° C |
| Compuestos relacionados | |
| Compuestos relacionados | Bencenotiol |
| Excepto cuando se indique lo contrario, los datos se den materiales en su condiciones normales (25 ° C, 100 kPa) | |
| Exenciones y referencias | |
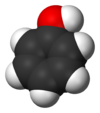
El fenol, también conocido bajo el nombre anterior de ácido carbólico, es un tóxico, incoloro cristalino sólido con un olor alquitranado dulce. Su fórmula química es C 6 H 5 O H y su estructura es la de una hidroxilo grupo (-OH) unido a una anillo de fenilo; es por lo tanto una compuesto aromático.
Los fenoles
La palabra de fenol también se utiliza para referirse a cualquier compuesto que contiene una de seis miembros anillo aromático, unido directamente a una grupo hidroxilo (-OH). En efecto, los fenoles son una clase de compuestos orgánicos de los cuales el fenol descrito en este artículo es el miembro más simple.
Propiedades
El fenol tiene una limitada solubilidad en agua (8,3 g / 100 ml). Es ligeramente ácida: La molécula de fenol tiene tendencias débiles de perder el ion H + del grupo hidroxilo, lo que resulta en el altamente soluble en agua fenóxido anión C 6 H 5 O -. En comparación con alifáticos alcoholes , fenol muestra mucha mayor acidez; incluso reacciona con NaOH acuoso perder H +, mientras que alifáticos alcoholes no lo hacen. Una explicación para el aumento de la acidez es estabilización por resonancia del anión fenóxido por el anillo aromático. De esta manera, la carga negativa sobre el oxígeno es compartida por los orto y para átomos de carbono. En otra explicación, el aumento de la acidez es el resultado de la superposición orbital entre pares libres del oxígeno y el sistema aromático. En una tercera, el efecto dominante es la la inducción de la sp² carbonos híbridas; la comparativamente más potente retirada inductiva de densidad de electrones que se proporciona por el sistema sp² en comparación con un sistema de sp³ permite una gran estabilización del oxianión. Al hacer esta conclusión, se puede examinar la pK a de la enol de la acetona , que es 10,9 en comparación con fenol con un pKa de 10,0.
Producción
El fenol se puede hacer de la parcial oxidación de benceno o ácido benzoico, por el proceso de cumeno, o por el Proceso de Raschig. También se puede encontrar como un producto de carbón de oxidación.
Usos
El fenol tiene propiedades antisépticas, y fue utilizado por Sir Joseph Lister (1827-1912) en su técnica pionera de la cirugía antiséptica, aunque la irritación de la piel causada por la exposición continua al fenol finalmente llevó a la sustitución de las técnicas asépticas (libres de gérmenes) en la cirugía. También es el ingrediente activo en algunos anestésicos orales tales como Aerosol Chloraseptic. El fenol fue también el ingrediente principal de la Bola de humo carbólico, un dispositivo que se vende en Londres diseñado para proteger al usuario contra la influenza y otras enfermedades.
También se utiliza en la producción de medicamentos (es el material de partida en la producción industrial de la aspirina ), herbicidas, y sintético resinas ( Baquelita, una de las primeras resinas sintéticas que se fabrican, es un polímero de fenol con formaldehído). La exposición de la piel para soluciones concentradas de fenol causas quemaduras químicas que pueden ser graves; en laboratorios en los que se utiliza, por lo general se recomienda que solución de polietilenglicol se mantiene disponible para lavarse de salpicaduras. Lavar con grandes cantidades de llanura de agua (la mayoría de los laboratorios cuentan con una ducha de seguridad o de lavado de ojos) y la eliminación de la ropa contaminada son obligatorios, y el tratamiento ER inmediata para grandes salpicaduras; particularmente si el fenol se mezcla con cloroformo (una mezcla utilizado comúnmente en la biología molecular de ADN de purificación). A pesar de los efectos de las soluciones concentradas, que también se utiliza en cirugía cosmética como una exfoliante, para eliminar las capas de piel muerta. También se utiliza en fenolización, un procedimiento quirúrgico utilizado para tratar una uña encarnada, en la que se aplica a la punta del pie para evitar el recrecimiento de uñas.
Las inyecciones de fenol de vez en cuando se han utilizado como un medio de rápida la ejecución. En particular, el fenol se utilizó como medio de exterminio por los nazis antes y durante la Segunda Guerra Mundial . Originalmente usado por los nazis en la década de 1930 como parte de su programa de eutanasia, fenol, barato y fácil de hacer y rápidamente eficaz, se convirtió en el medicamento inyectable de elección a través de los últimos días de la guerra. Aunque Zyklon-B se utilizaron en las cámaras de gas cuando grandes grupos de personas que se necesitan para ser asesinados, los nazis aprendieron cuando pequeños grupos necesitan exterminando que era más económico para inyectar a sus víctimas una a la vez con fenol en lugar. Inyecciones de fenol se les dio a miles de personas en campos de concentración, sobre todo en Auschwitz-Birkenau. Las inyecciones se administraron por médicos, su ayudantes, oa veces los médicos de prisioneros; tales inyecciones fueron dadas originalmente por vía intravenosa, más comúnmente en el el brazo, pero la inyección directamente en el corazón , a fin de inducir casi instantáneo muerte , fue más tarde preferido. Uno de los más famosos de los internos de Auschwitz para ser ejecutado por inyección de ácido carbólico era San Maximiliano Kolbe, un sacerdote católico que se ofreció voluntariamente a someterse a tres semanas de hambre y deshidratación en el lugar de otro recluso y que finalmente fue inyectado con ácido carbólico para que los nazis podían hacer más espacio en sus celdas de detención. Un uso de fenol en la biología molecular es la separación de material genético (ácidos nucleicos) ( ADN y ARN) a partir de proteínas.
Química Hidrotermal
En condiciones de laboratorio imitación circulación hidrotermal (agua, 200 ° C, 1,9 GPa), el fenol se encuentra para formar a partir de carbonato de hidrógeno de sodio y hierro en polvo (1,8% rendimiento químico). Este descubrimiento realizado en 2007 puede ser relevante para la origen de cuestión de vida como fenol es un fragmento de la biomolécula tirosina. Sin embargo, como se conoce a la tirosina a resultar directamente de la hidroxilación de la fenilalanina en los sistemas biológicos modernos, las implicaciones de fenol prebiótica son cuestionables en el mejor.
