Glycine (acide aminé)
| Glycine | |
|---|---|
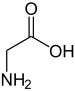  La glycine (à gauche) et son zwitterion (à droite).  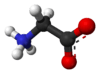 Modèle 3D de la glycine et de son zwitterion | |
| Identification | |
| Nom UICPA | acide aminoacétique |
| Synonymes | G, Gly, acide 2-aminoéthanoïque |
| No CAS | |
| No EINECS | |
| Code ATC | B05 |
| No E | E640 |
| FEMA | |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule brute | C2H5NO2 [Isomères] |
| Masse molaire[1] | 75,0666 ± 0,0028 g/mol C 32 %, H 6,71 %, N 18,66 %, O 42,63 %, |
| pKa | 2,4 9,7 |
| Propriétés physiques | |
| T° fusion | 232 °C à 236 °C |
| Solubilité | 225 g·L-1 dans l'eau, Soluble dans l'éthanol |
| Masse volumique | 1,607 g·cm-3 |
| Propriétés biochimiques | |
| Codons | GGU, GGC, GGA, GGG |
| pH isoélectrique | 5,97[2] |
| Acide aminé essentiel | Non |
| Occurrence chez les vertébrés | 7,4 %[3] |
| Propriétés optiques | |
| Pouvoir rotatoire | 0 ° |
| Précautions | |
Produit non contrôlé | |
La glycine (abréviations IUPAC-IUBMB : Gly et G) est un acide α-aminé et l'un des 22 acides aminés protéinogènes. Elle est encodée sur les ARN messagers par les codons GGU, GGC, GGA et GGG. C'est le plus simple des acides α-aminés, et elle ne possède aucun atome de carbone asymétrique. Son rayon de Van der Waals est égal à 48 Å.
Jadis appelée glycocolle ou acide aminoacétique, la glycine possède un goût sucré et peut être utilisée pour améliorer le goût d'édulcorants ou comme exhausteur de goût (E640).
Fonctions biologiques
- La molécule de glycine joue un rôle de neurotransmetteur inhibiteur au niveau de la moelle épinière.
- Ce n'est pas une molécule chirale (c'est une exception pour les acides aminés).
- La glycine est un précurseur des porphyrines, mais aussi de la créatine (dans le foie), de l'acide urique (forme d'excrétion de l'ammoniac chez les oiseaux), du glutathion (composé qui participe à la réduction des radicaux libres), de l'acétylcholine (neurotransmetteur).
- La synthèse du collagène[5].
- Elle entre dans la composition des acides biliaires primaires : elle se conjugue aux sels biliaires les rendant plus solubles.
- Ajoutée au succinyl-CoA elle forme l'hème, de l'hémoglobine par exemple.
- Elle s'interconvertit avec la sérine et la thréonine, et constitue la molécule finale de la dégradation de la choline :
Catabolisme
La glycine déshydrogénase catalyse la réaction suivante, qui est réversible :
- glycine + tétrahydrofolate + NAD+
 CO2 + 5,10-méthylènetétrahydrofolate + NADH + H+ + NH4+.
CO2 + 5,10-méthylènetétrahydrofolate + NADH + H+ + NH4+.
Présence dans l'espace
De la glycine a été identifiée sur une comète[6]. Cette découverte renforce l'hypothèse selon laquelle la vie pourrait s'être formée sur Terre grâce à l'apport de molécules d'origine extraterrestre.
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ (en) Francis A. Carey, « Table of pKa and pI values », sur Département de chimie de l'université de Calgary,‎ (consulté le 26 juillet 2015)
- ↑ (en) M. Beals, L. Gross, S. Harrell, « Amino Acid Frequency », sur The Institute for Environmental Modeling (TIEM) à l'université du Tennessee (consulté le 26 juillet 2015)
- ↑ « Glycine » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ « La science dévoile le secret de la longévité », sur Julien Venesson ♣ Site Officiel - Informations nutrition, micronutrition, santé, sports (consulté le 20 octobre 2015)
- ↑ De la glycine d'origine extra-terrestre découverte sur une comète.
Lien externe
- (en) http://www.chemie.fu-berlin.de/chemistry/bio/aminoacid/glycin_en.html
- (en) ChemSub Online : Glycine
Articles connexes
- Liste d'acides
- Acide aminé
- Portail de la biochimie
- Portail de la pharmacie
- Portail de la chimie
