Carbonate de magnésium
|
|
Cet article est une ébauche concernant les composés inorganiques. Vous pouvez partager vos connaissances en l’améliorant (comment ?) selon les recommandations des projets correspondants.
|
| Carbonate de magnésium | |
|---|---|
 | |
| Identification | |
| Nom UICPA | carbonate de magnésium |
| Synonymes | magnésite |
| No CAS | |
| No EINECS | |
| Code ATC | A02 A06 |
| PubChem | |
| ChEBI | |
| SMILES | |
| InChI | |
| Apparence | poudre blanche |
| Propriétés chimiques | |
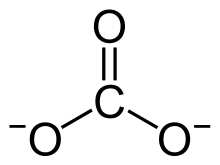
| Formule brute | MgCO3 |
| Masse molaire[1] | 84,3139 ± 0,0023 g/mol C 14,25 %, Mg 28,83 %, O 56,93 %, |
| Propriétés physiques | |
| T° fusion | 350 °C (décomposition) [2] |
| Solubilité | 0,106 g·l-1 (eau,20 °C) [2] |
| Masse volumique | 2,96 g·cm-3 à 20 °C [2] |
| Thermochimie | |
| S0solide | 65,84 J·K-1·mol-1 [3] |
| ΔfH0solide | -1 111,69 kJ·mol-1 [3] |
| Précautions | |
0 1 0 | |
Le carbonate de magnésium (MgCO3) est un solide de couleur blanche, qui se trouve à l'état minéral dans la nature. C'est un composant de la magnésite. Sous forme de poudre, le carbonate de magnésium est utilisé comme anti-transpirant dans de nombreux sports, connu sous le nom de magnésie.
Propriétés physico-chimiques
A des températures supérieures à 400 °C, une décarboxylation a lieu et forme l'oxyde de magnésium
Utilisation
Sous forme de poudre appelée couramment « magnésie » — même si en chimie, la magnésie désigne de fait l'oxyde de magnésium — le carbonate de magnésium est utilisé dans certains sports comme la gymnastique artistique, l'escalade ou l'haltérophilie pour assécher les mains. La formule de cette poudre est plus précisément 4MgCO2Mg(OH)24H2O. Elle peut contenir une faible proportion de silice qui, inhalée, peut avoir des effets sur les poumons.

Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- 1 2 3 Entrée de « Magnesium(II) carbonat » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 4 mai 2010 (JavaScript nécessaire)
- 1 2 (en) « Magnesium carbonate » sur NIST/WebBook, consulté le 4 mai 2010
- ↑ UCB Université du Colorado
- Portail de la chimie
- Portail de la gymnastique
- Portail de l’alpinisme et de l’escalade

![MgCO_3 \ \xrightarrow[]{\Delta} \ MgO \ + \ CO_2](../i/m/1431b259c8270478a991061e0b4f7549.png)