Pression partielle
|
|
Cet article est une ébauche concernant la thermodynamique. Vous pouvez partager vos connaissances en l’améliorant (comment ?) selon les recommandations des projets correspondants.
|
La pression partielle d'un gaz parfait i dans un mélange de gaz parfaits de pression totale 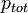 est définie comme la pression
est définie comme la pression 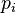 qui serait exercée par les molécules du gaz i si ce gaz occupait seul tout le volume offert au mélange, à la température de celui-ci.
Elle correspond donc à la contribution de ce gaz i à la pression totale du mélange.
qui serait exercée par les molécules du gaz i si ce gaz occupait seul tout le volume offert au mélange, à la température de celui-ci.
Elle correspond donc à la contribution de ce gaz i à la pression totale du mélange.
Définition mathématique
La loi de Dalton, valable rigoureusement pour un mélange idéal de gaz parfaits, relie la pression partielle 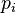 et la pression totale
et la pression totale 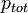 par l'intermédiaire de la fraction molaire
par l'intermédiaire de la fraction molaire 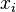 du constituant considéré dans le mélange :
du constituant considéré dans le mélange :
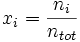
- où
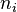 est le nombre de moles d'un constituant quelconque repéré par l'indice
est le nombre de moles d'un constituant quelconque repéré par l'indice 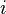 dans le mélange et
dans le mélange et 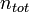 le nombre total de moles dans le mélange.
le nombre total de moles dans le mélange.
- La pression partielle du constituant i est égale au produit de sa fraction molaire par la pression totale.
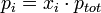
La pression d'un mélange idéal de gaz parfaits est la somme des pressions partielles de chacun de ses constituants.
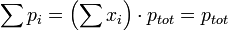
- car
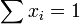 .
.
Voir aussi
- Les grandeurs hygrométriques: La pression partielle de vapeur sur le site energieplus-lesite.be de Architecture et Climat de l'Université catholique de Louvain
- Portail de la chimie
- Portail de la physique