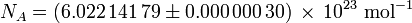Constante d'Avogadro
Contexte des ??coles Wikip??dia
SOS Enfants produite ce site pour les ??coles ainsi que ce site de vid??o sur l'Afrique . Visitez le site Web d'enfants SOS au http://www.soschildren.org/
La constante d'Avogadro (symboles: L, N A), appel??e aussi le nombre d'Avogadro est le nombre de ??entit??s?? (en g??n??ral, des atomes ou mol??cules) dans une en mole, qui est, le nombre de carbone-12 atomes de 12 grammes (0,012 kg ) de carbone-12 non li??e ?? l'??tat du sol. La meilleure estimation actuelle de ce nombre est:
La valeur du nombre a d'abord ??t?? signal??e par Johann Josef Loschmidt, qui en 1865, a calcul?? le nombre de particules dans un centim??tre cube de gaz dans des conditions standard. Le terme Loschmidt constant est donc plus correctement appliqu?? pour cette derni??re valeur, qui peut ??tre dit ??tre proportionnelle au nombre d'Avogadro. Cependant, dans la langue allemande litt??rature, "Loschmidt constante" est utilis?? pour d??signer ?? la fois cet usage, ainsi que le nombre d'entit??s dans un grain de beaut??.
Histoire et ??tymologie
La constante d'Avogadro est nomm?? d'apr??s le d??but du XIXe si??cle italien scientifique Amedeo Avogadro, qui est cr??dit?? (1811) d'??tre le premier ?? se rendre compte que le volume d'un gaz (strictement, d'une gaz id??al) est proportionnelle au nombre d' atomes ou de mol??cules . Le chimiste fran??ais Jean Perrin en 1909 a propos?? de nommer la constante d'Avogadro en l'honneur. Manuels de chimie am??ricains ramass??rent dans les ann??es 1930, suivie par les manuels du secondaire ?? partir dans les ann??es 1950.
Loschmidt: mesurer le nombre d'Avogadro
Avogadro n'a jamais tent?? de mesurer la constante: la valeur num??rique a ??t?? estim?? par le premier autrichienne physicien Johann Josef Loschmidt en 1865 en utilisant le th??orie cin??tique des gaz. Dans les pays germanophones, la constante est parfois d??sign?? sous le nom Loschmidt constante ou le num??ro de Loschmidt, mais ce Loschmidt r??ellement mesur??e est le nombre de particules par unit?? de volume d'un gaz parfait, ?? savoir la densit?? en nombre de particules dans un gaz parfait. Ainsi, le terme Loschmidt constante est plus appropri?? au nombre de particules par unit?? de gaz, Symbole: n o:
??gal ?? (2,686 ?? 7,774 0,000 0047) ?? 10 25 m -3 ?? 273,15 K et 101,325 avec k B kPa le Constante de Boltzmann, T la temp??rature et la p pression.
Cette constante est li??e ?? la constante d'Avogadro par la relation:
avec k B la Constante de Boltzmann, et R le constante des gaz, donc
Cependant, dans allemand litt??rature scientifique, le terme Loschmidt constante est utilis?? de fa??on ambigu?? - il se r??f??re souvent ?? ce qui est venu pour ??tre connu comme nombre d'Avogadro. Cependant, Boltzmann avait d'abord utilis?? le terme pour le sens dans lequel Loschmidt avait mesur?? elle - le nombre de particules dans un volume unitaire de gaz. Ainsi, son utilisation dans r??f??rant au nombre de Avogadro li??s pr??te ?? confusion et est g??n??ralement d??conseill??e. Pour la m??me raison, le nombre d'Avogadro parfois est d??sign??e par L par rapport ?? N A dans les textes allemands.
Normalisation de la taupe
Avant 1960, il y avait conflit d??finitions du taupe, et donc du nombre d'Avogadro (comme on l'appelait ?? l'??poque), bas?? sur 16 grammes d'oxyg??ne: les physiciens g??n??ralement utilis??s oxyg??ne-16 tandis chimistes utilis??s g??n??ralement "naturellement" rapport isotopique.
Commutation, en 1960, ?? 12 grammes de carbone-12 de base termin?? ce diff??rend et a eu d'autres avantages. A ce moment, le nombre d'Avogadro a ??t?? d??finie comme le nombre d'atomes dans 12 g de carbone-12, qui est aussi un quantit?? sans dimension, tandis que la taupe a ??t?? d??finie comme une Avogadro nombre d'atomes, de mol??cules ou d'autres entit??s.
Lorsque la taupe est entr?? dans la Syst??me international d'unit??s (SI), en 1971, les d??finitions ont ??t?? ??chang??s.
En 1971, un grain de beaut?? a ??t?? d??fini comme le nombre d'atomes dans 12 grammes de carbone-12, avec sa propre dimension, ??quantit?? de mati??re??, ?? savoir. Le nombre d'Avogadro est devenu un constante physique avec l'unit?? de moles r??ciproques (mol -1).
Application
La constante d'Avogadro peut ??tre appliqu??e ?? ne importe quelle substance. Il correspond au nombre d'atomes ou de mol??cules n??cessaires pour constituer une masse ??gale ?? la substance de atomique ou mol??culaire de masse , en grammes. Par exemple, la masse atomique du fer est 55,847 g / mol, de sorte N A atomes de fer (ce est ?? dire une mole d'atomes de fer) a une masse de 55,847 g. Inversement, 55,847 g de fer contient N A atomes de fer. La constante d'Avogadro entre ??galement dans la d??finition de la unit?? de masse atomique unifi??e, u:
Relations physiques suppl??mentaires
En raison de son r??le en tant que facteur d'??chelle, le nombre d'Avogadro assure le lien entre un certain nombre de constantes physiques utiles lors du d??placement entre le ??chelle atomique et l'??chelle macroscopique. Par exemple, elle fournit la relation entre:
- la R constante et le gaz Boltzmann k constante B:
- en J mol -1 K -1
- la Constante de Faraday F et le charge ??l??mentaire e:
- en C mol -1
Mesure de la constante d'Avogadro

Un certain nombre de m??thodes peuvent ??tre utilis??es pour mesurer la constante d'Avogadro. Une m??thode moderne consiste ?? calculer la constante d'Avogadro ?? partir de la densit?? (ρ) d'un cristal, la masse atomique relative (M), et la longueur de cellule unitaire (a) d??termin?? ?? partir de cristallographie aux rayons X. Des valeurs tr??s pr??cises de ces quantit??s pour le silicium ont ??t?? mesur??es ?? la National Institute of Standards and Technology (NIST) et utilis?? pour obtenir la valeur de la constante d'Avogadro:
 .
.
- ?? base de silicium.