Tautomère
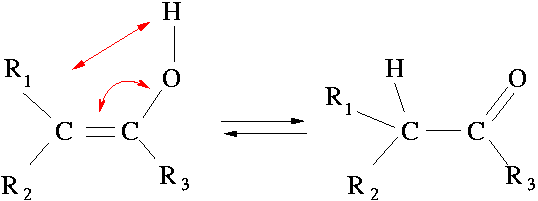 Les tautomères sont des couples d'isomères de constitution interconvertibles par la réaction chimique réversible appelée tautomérisation. Dans la plupart des cas, la réaction se produit par migration d'un atome d'hydrogène accompagnée d'un changement de localisation d'une double liaison[1],[2].
Dans une solution d'un composé capable de tautomérisation, un équilibre entre les deux tautomères se crée. Le rapport entre tautomères est alors fonction du solvant, de la température et du pH.
Les tautomères sont des couples d'isomères de constitution interconvertibles par la réaction chimique réversible appelée tautomérisation. Dans la plupart des cas, la réaction se produit par migration d'un atome d'hydrogène accompagnée d'un changement de localisation d'une double liaison[1],[2].
Dans une solution d'un composé capable de tautomérisation, un équilibre entre les deux tautomères se crée. Le rapport entre tautomères est alors fonction du solvant, de la température et du pH.
La tautomérie est donc la transformation d'un groupement fonctionnel en un autre, le plus souvent par déplacement concomitant d'un atome d'hydrogène et d'une liaison π (liaison double ou triple). Contrairement à la mésomérie, les liaisons σ (liaisons simples) peuvent être déplacées avec le proton. Les prototropies ne sont pas des tautoméries, elles n'induisent pas un remaniement du système π et l'hydrogène ne provient pas forcément de la même molécule (solvant).
La tautomérisation est catalysée par :
- les bases
Le mécanisme se décompose en :
- une déprotonation,
- la formation d'un anion délocalisé,
- la protonation à un autre endroit de l'anion;
- ou les acides
Le mécanisme se décompose en :
- une protonation,
- la formation d'un cation délocalisé,
- la déprotonation à un autre endroit du cation.
Des tautomères courants sont :
- aldéhydes / cétones - alcools ou plus précisément énol : l'acétone par exemple ;
- amides - acides imidiques : l'hydrolyse du nitrile ;
- lactames - lactimes : les tautomérismes des bases nucléiques de l'ADN : adénine, guanine, thymine et cytosine ;
- imines - énamines ;
- énamines - énamines.
Notes et références
Voir aussi
- Isomérie
- Portail de la chimie